Isoamilico -alkoholirakenne, ominaisuudet, käytöt ja riskit
- 3619
- 503
- Eddie Hackett
Hän Isoamyylialkoholi Se on orgaaninen yhdiste, jonka kaava on (ch3-A2Shakki2CH2vai niin. Kemiallisesti puhuminen on haarautunut primaarinen alkoholi, ja se muodostaa yhden pentanoli -isomeereistä, nimeltään Amyyylialkoholiksi (C5H12JOMPIKUMPI).
Kuten monet pienimolekyylipainoiset alkoholit, se on väritön neste huoneenlämpötilassa. Tämä mahdollistaa ja helpottaa sitä, että sitä käytetään liuottimena eri sovelluksille; Lisäksi, kun sillä ei ole liian monta kielteistä vaikutusta ekosysteemiin hävittämisen jälkeen.
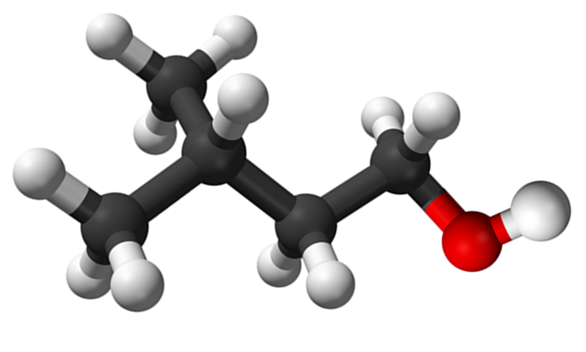
 Isoamiilinen alkoholimolekyyli. Lähde: Claudio Pistilli de Wikipedia.
Isoamiilinen alkoholimolekyyli. Lähde: Claudio Pistilli de Wikipedia. Vaikka se on välittäjäaine Amilo -asetaatin synteesissä banaanin tuoksujen kehittämisessä, sen oma haju on epämiellyttävä ja samanlainen kuin päärynöiden.
Sen lisäksi, että se toimii useiden biologisten aineiden liuottimena ja välittäjänä muiden asettien synteesissä, se vähentää tiettyjen teollisuusformulaatioiden pintajännitystä estäen vaahtoja muodostamasta. Siksi sitä käytetään mikro -emulgoituneissa järjestelmissä.
Sen luonnollisen alkuperän suhteen isoamiilinen alkoholia on löydetty Hornetsin horomonoista ja mustista tryffeleistä, eräänlaisista sienistä, jotka sijaitsevat Euroopan kaakkoon.
[TOC]
Isoamilico -rakenne
Yläkuvassa isoamyylialkoholimolekyyli esitettiin palloilla ja baarimallilla. Saman oikealla puolella punertava pallo vastaa OH -ryhmän happiatomia, joka on ominainen kaikille alkoholille; Vasemmalla puolella on hiilihapotettu luuranko, jossa on metyyliryhmä, Cho3, rakennetta.
Molekyylin näkökulmasta tämä yhdiste on dynaaminen atomien kanssa SP -hybridaatioilla3, helpottaa niiden linkkien kiertoa; Niin kauan kuin se ei aiheuta OH: n ja CH: n pimennystä3.
On myös syytä mainita sen amfifiilinen ominaisuus: sillä on apolaarinen tai hydrofobinen pää, jonka muodostuu ketjusta (CH3-A2Shakki2CH2-, ja polaarinen tai hydrofiilinen pää, OH -ryhmä. Tämä kahden tietyn polaarisuuksien erityisalueen määritelmä tekee tästä alkoholista tenseaktiivisen; Ja täältä on johdettu sen soveltamisen mikroemulsioihin.
Voi palvella sinua: Lever -sääntöMolekyylien väliset vuorovaikutukset
OH -ryhmän läsnäolon vuoksi isoamiilinen alkoholimolekyyli esittelee pysyvän dipolin hetken. Näin ollen dipoli-dipoli.
Vaikka pääketjujen haara vähentää molekyylien välisiä tehokkaita vuorovaikutuksia, tässä alkoholin vety sillat kompensoivat tämän laskeutumisen aiheuttaen nesteen kiehumisen 131 ° C: ssa, lämpötila korkeampi kuin kiehumispiste vesipisteenä.
Sitä ei tapahdu sen kiinteällä tai ”jäällä”, joka sulaa -117 ° C: seen, mikä osoittaa, että sen molekyylien väliset vuorovaikutukset eivät ole riittävän vahvoja pitämään niiden molekyylien järjestäytyneinä; varsinkin jos CHO -ryhmä3 joka haarat pääketju estää paremman kontaktin molekyylien välillä.
Ominaisuudet
Fyysinen ulkonäkö
Väritön neste.
Haju ja maku
Hylkää epämiellyttävän hajun, joka on samanlainen kuin päärynän, ja sillä on terävä maku.
Moolimassa
88 148 g/mol.
Tiheys
0,8104 g/ml 20 ° C: ssa. Siksi se on vähemmän tiheä kuin vesi.
Höyryn tiheys
Se on 3,04 kertaa tiheämpi kuin ilma.
Höyrynpaine
2,37 mmHg 25 ° C: ssa.
Kiehumispiste
131,1 ° C.
Sulamispiste
-117,2 ° C.
sytytyspiste
43 ° C (suljettu kuppi).
Itsensuuntainen lämpötila
340 ° C.
Liukoisuus
Se on suhteellisen liukeneva veteen: 28 g/l. Tämä johtuu siitä, että veden erittäin polaariset molekyylit eivät tunne erityistä affiniteettia hiilihapotettuun isoamyylialkoholiketjuun. Jos se sekoitetaan, havaitaan kaksi vaihetta: alempi, vastaa vettä ja ylivoimainen, isoamyylialkoholi.
Sitä vastoin se on paljon liukoisempi vähemmän polaarisiin liuottimiin, kuten asetoni, eetteri, kloroformi, etanoli tai jääetikkahappo; ja jopa öljyeetterissä.
Se voi palvella sinua: laboratoriolämpömittari: Ominaisuudet, mitä se on, käytä, esimerkkejäGoo
3 738 CP 25 ° C: ssa.
Pintajännitys
24,77 DINS/cm 15 ° C.
Taitekerroin
1 4075 - 20 ° C.
Lämpökapasiteetti
2 382 kJ/g · k.
Sovellukset
Raaka materiaali
Isoamiilisesta alkoholista muut esterit, tiofeeni ja huumeet, kuten amilo -nitriitti, pätevä (iavalasere -majainen), bromisoval (bromobalerilurea), corvalol (callerian tranquanar) ja barbamil (amobarbital) (ambarbital).
Tuoksut
Sen lisäksi, että sitä käytetään Amilo -asetaatin synteesiin, jolla on banaaniaromi, siitä saadaan myös muita hedelmätuoteita, kuten aprikoosi, appelsiinit, luumut, kirsikka ja mallas. Siksi se on välttämätön alkoholi lukuisten syötävien tai kosmetiikkatuotteiden kehittämisessä.
Antipumatontti
Vähentämällä pintajännitystä se edistää sen käyttöä mikro -emulgoituneissa järjestelmissä. Vältä käytännössä kiihdytettyä kuplan muodostumista, pienentämällä niitä kooltaan niiden katkaisemiseksi.
Se auttaa myös paremmin määrittelemään vesipitoisten ja orgaanisten faasien välinen rajapinta uuttojen aikana; Esimerkiksi se lisätään fenolikloroform-uuttoseokseen 25: 1-suhteessa. Tämä tekniikka on tarkoitettu DNA: n uuttamiseen.
Poistot
Isoamyylialkoholi antaa sinun myös poimia rasvoja tai öljyjä eri näytteistä, esimerkiksi maidosta. Liuota myös parafiinivaha, musteet, kumi, lakko ja selluloosaesterit.
Jatkamalla uuttoja, sillä sen avulla voit saada fosforihappoa rautafosfaattisista mineraaliliuoksista.
Riskejä
Varastointi ja reaktiivisuus
Kuten kaikki hajujen aiheuttavat nesteet, se voi edustaa välitöntä tulen riskiä, jos paikka, jossa sen lämpötila on liian varastoitu, vielä enemmän, jos lämmönlähde on jo.
Näissä olosuhteissa se toimii vain polttoaineena, liekkien ruokinta ja jopa sen säiliön hyödyntäminen. Kun poltetaan, vapauta höyryt, jotka voivat vaikuttaa terveyteen ja aiheuttaa tukehtumista.
Voi palvella sinua: kvantitatiivinen analyysi kemiassa: mittaukset, valmisteluMuut syyt, jotka isoamiilinen alkoholi on tulossa.
Terveys
Kosketuksessa ihon kanssa voit ärsyttää ja kuivata sen. Oireet ovat kuitenkin vakavampia, jos sitä hengitetään liian kauan (yskä, nenän palovamma, kurkku ja keuhkot) tai nielty (päänsärky, pahoinvointi, ripuli, oksentelu, huimaus ja tiedon menetys).
Ja lopuksi, kun se vuotaa silmissä, ärsyttää heitä ja voi jopa vahingoittaa niitä peruuttamattomasti. Onneksi sen "alkoholipäränten" haju antaa sinun havaita sen poistumisen tai vuotojen tapauksessa; Tämän lisäksi se on yhdiste, jota on manipuloida kunnioittavasti.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5. painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. Amiini. (10. painos.-A. Wiley Plus.
- Wikipedia. (2019). Isoamyylialkoholi. Haettu: vuonna.Wikipedia.org
- Kansallinen bioteknologiatietojen keskus. (2019). Isoamyylialkoholi. Pubchem -tietokanta. CID = 31260. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- Zhang Yu & Muhammed Mamoun. (17. syyskuuta 2008). Fosforihapon uutto nitraattiliuoksista isoamyylialkoholilla. Liuotinuutto ja ioninvaihto Volume 6, 1988 - numero 6. doi.org/10.1080/07366298808917973
- New Jerseyn terveysministeriö. (2008). Isoamyylialkoholi. [PDF]. Palautettu: NJ.Hallitus
- Kat Chem. (2019). Isoamyylialkoholi. Toipunut: Kat-Chem.Huijari
- Chemoxy International Ltd. (S.F.-A. Isoamyylialkoholi. Talteenotettu: kemoksi.com

