Aldehydit
- 2343
- 374
- Dr. Travis Reichert
Mitkä ovat aldehydit?
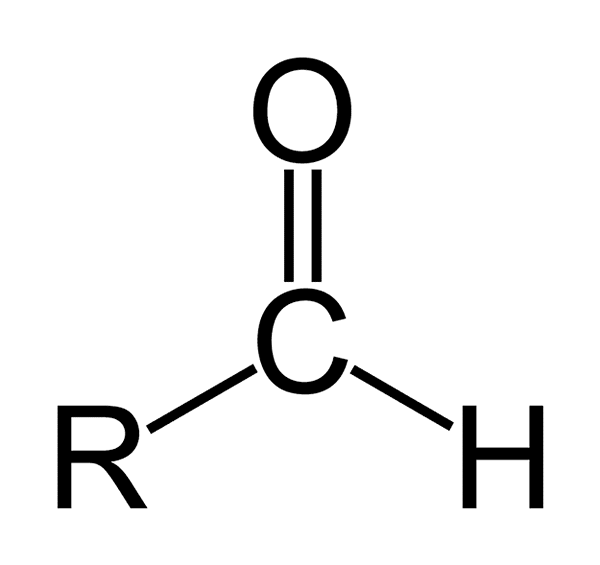
Se aldehydit Ne ovat orgaanisia yhdisteitä, joilla on yleinen kaava RCHO. R edustaa alifaattista tai aromaattista ketjua; C hiili; Tai happi ja H -vety. Niille on ominaista karbonyyliryhmän, kuten ketonien ja karboksyylihappojen, hallussapito, joten aldehydejä kutsutaan myös karbonyyliyhdisteiksi.
Karbonyyliryhmä antaa aldehydille monia sen ominaisuuksia. Ne ovat yhdisteitä, jotka ovat helposti hapettuneet ja ovat erittäin reaktiivisia nukleofiilisiin lisäyksiin. Karbonyyliryhmän kaksoissidos (C = O) esittelee kaksi atomia, joilla on eroja niiden aviditeetissä elektronien avulla (elektronegatiivisuus).
Happi houkuttelee elektroneja voimakkaammin kuin hiili, joten elektroninen pilvi siirtyy sitä kohti tekemällä kaksoissidoksen hiilen ja polaarisen luonteen välillä, tärkeällä dipolimomentillä. Tämä tekee aldehydoista.
Toisin sanoen, aldehydot ovat eräänlainen orgaaniset yhdisteet, jotka johtuvat tiettyjen alkoholien hapettumisesta.
Aldehydojen kemiallinen rakenne
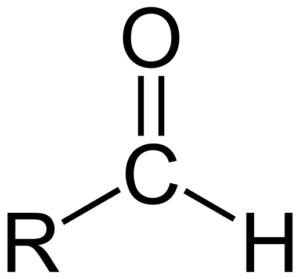 Aldehydojen kemiallinen rakenne
Aldehydojen kemiallinen rakenne Aldehydot koostuvat karbonyylistä (c = o), johon vetyatomi on suoraan kytketty. Tämä erottaa sen muista orgaanisista yhdisteistä, kuten ketoneista (R2C = O) ja karboksyylihappot (RCOOH).
Yläkuva näyttää molekyylirakenteen. Formiliryhmä on tasainen, koska hiilellä ja hapella on SP -hybridisaatio2. Tämä tasomaisuus tekee siitä alttiuden nukleofiililajien hyökkäykselle, ja siksi se on helposti hapettunut.
Mitä tällainen hapettuminen tarkoittaa? Yhteyden muodostumiseen muihin elektronegatiivisempiin atomiin kuin hiilen kanssa; Ja aldehydojen tapauksessa se on happi. Siten aldehydi hapettaa karboksyylihapon, -COH: n. Entä jos aldehydi väheni? Sen sijaan muodostuu ensisijainen alkoholi, Roh.
Aldehydoja esiintyy vain ensisijaisista alkoholeista: ne, joissa OH -ryhmä on ketjun lopussa. Samoin Formil -ryhmä aina Se on ketjun lopussa tai erottuu siitä tai rengas substituentina (jos on muita tärkeämpiä ryhmiä, kuten -COOH).
Aldehydien fysikaaliset ja kemialliset ominaisuudet
Polaariset yhdisteet, niiden sulamispisteet ovat suurempia kuin ei -polaaristen yhdisteiden kanssa. Aldehydos -molekyylit eivät pysty sitomaan molekyylien välistä vety silloja, sillä ne ovat vain hiiliatomeja, jotka ovat yhdistyneet vetyatomiin.
Yllä olevan johtuen aldehydeillä on alhaisemmat kiehumispisteet kuin alkoholilla ja karboksyylihapolla.
Fuusiopisteet
Formaldehydi -92; Asetaldehydi -121; Propionaldehydi -81; n- butiraldehydi -99; N -valeraldehydi -91; Caproaldehydi -; Hepldehydi - 42; Fenyyliasetaldehydi -; Bentsaldehydi -26.
Kiehumispisteet
Formaldehydi -21; Asetaldehydi 20; Hyd 49; N-butiraldehido 76; N-valeraldehydi 103; Caproaldehydi 131; Hepldehydi 155; Fenyyliasetaldehydi 194; Bentsaldehydi 178.
Voi palvella sinua: Aineen erityiset ominaisuudet: Mitkä ovat ja esimerkkejäVeden liukoisuus ilmaistuna g/100 g h: ta2JOMPIKUMPI
Formaldehydi, erittäin liukoinen; asetaldehydi, ääretön; Propionaldehydi, 16; N-butiraldehydi, 7; N-valeraldehydi, hieman liukoinen; Caproaldehydi, hieman liukoinen; Fenyyliasetaldehydi hieman liukoinen; Bentsaldehydi, 0,3.
Aldehydojen kiehumispisteillä on taipumus kasvaa suoraan molekyylipainon kanssa. Päinvastoin, on taipumus vähentää aldehydien liukoisuutta veteen, kun niiden molekyylipaino kasvaa. Tämä heijastuu vasta mainittujen aldehydien fyysisissä vakioissa.
Aldehydojen reaktiivisuus
Hapetusreaktio
Aldehydit voivat hapettua vastaavan karboksyylihappoa minkä tahansa näiden yhdisteiden läsnä ollessa: AG (NH3-A2, Kmno4 Okei2Cr2JOMPIKUMPI7.
Alkoholien vähentäminen
He voivat vedata itseään nikkeli-, platina- tai paladiumkatalyyttien avulla. Siten C = O muutetaan C-OH: ksi.
Vähennys hiilivetyihin
Zn: n (Hg) läsnä ollessa konsentroitu HCL tai NH: ssa2Nh2 Aldehydot menettävät karbonyyliryhmän ja niistä tulee hiilivetyjä.
Nukleofiilinen lisäys
Karbonyyliryhmään on lisätty useita yhdisteitä, joista on: Grignard, syanidireagenssit, ammoniakkijohdannaiset ja alkoholit.
Aldehydojen nimikkeistö
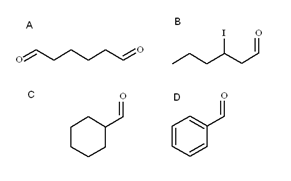 Neljä aldehydiä. Lähde: Gabriel Bolívar
Neljä aldehydiä. Lähde: Gabriel Bolívar Yläpuolella kuvassa on kuvattu neljä aldehydoja. Kuinka ne nimetään?
Koska ne ovat ruosteisia primaarisia alkoholeja, alkoholin nimeä muutetaan pääte -ol -al. Siten metanoli (valitse3OH) jos hapetetaan CHO: lle3CHO: ta kutsutaan metanaliksi (formaldehydi); CH3CH2Cho etanal (asetaldehydi); CH3CH2CH2Cho Propanal ja Cho3CH2CH2CH2Butanal cho.
Kaikilla äskettäin nimettyinä aldehydoissa on ryhmä -CHO ketjun lopussa. Kun tämä on molemmissa päissä, kuten A: ssa, lopussa -etuliite di lisätään hänelle-. Kuten kuusi hiilyä (laskee molempien formyyliryhmien ryhmät), se on peräisin 1-heksanolista, ja sen nimi on: heksaanivalinta.
Kun on substituentti, kuten alquilic -radikaali, kaksois- tai kolminkertainen linkki tai halogeeni, pääketjun hiilet luetellaan antamalla numero 1. Siten aldehydi b kutsutaan: 3-adhexanaaliksi.
Aldehydeissä C ja D ryhmä -CHO: lla ei kuitenkaan ole etusijalla näiden muiden yhdisteiden tunnistaminen. C on sykloalcano, kun taas d bentseeni, molemmat yhdellä H: stä, korvattu formil -ryhmällä.
Niissä, koska päärakenne on syklinen, formil -ryhmä on nimeltään Carbaldehydi. Siten C on sykloheksanokbaldehydi ja d bentsenokarbaldehydi (tunnetaan paremmin nimellä bentsaldehydi).
Aldehydojen käyttö
Luonnossa on aldehydejä, jotka kykenevät antamaan miellyttäviä makuja, kuten kanelimondehydin tapaus, joka on vastuussa kanelin ominaisesta mausta. Siksi niitä käytetään yleensä keinotekoisina aromeina monissa tuotteissa, kuten makeisia tai ruokia.
Formaldehydi
Formaldehydi on aldehydi, joka esiintyy teollisesti suuremmassa määrin. Metanolin hapettumisella saatua formaldehydia käytetään vedessä 37 -prosenttisessa kaasuliuoksessa Formaliinin nimellä. Tätä käytetään nahkojen parkituksessa sekä ruumiiden säilyttämisessä ja balmingissa.
Voi palvella sinua: Natriumasetaatti: rakenne, ominaisuudet, synteesi, käyttöFormaldehydiä käytetään myös kasvien ja vihannesten sukusoideksi, sienitarnaksi ja hyönteismyrkkiksi. Sen suurin hyödyllisyys on kuitenkin panos polymeerimateriaalin tuotantoon. Bakelita -niminen muovi syntetisoidaan formaldehydin ja fenolin välisellä reaktiolla.
Bakelita
Bakelita on suuri kova -koira -ulottuvuusrakennepolymeeri, jota käytetään lukuisissa kodinvälineissä, kuten kattilat, pannuissa, kahvinkeittimissä, veitsissä jne.
Bakelita samanlaiset polymeerit on valmistettu formaldehydistä yhdessä urean ja melamiiniyhdisteiden kanssa. Näitä polymeerejä käytetään paitsi muovina, myös niitä.
Vaneri
Vaneri on ohuiden puun arkkien muodostaman materiaalin kaupallinen nimi, joka liittyy formaldehydistä tuotetut polymeerit. Muodolliset ja Melmac -tuotemerkit valmistetaan tämän osallistumalla. Muodostaja on huonekalujen pinnoitteessa käytetty muovimateriaali.
MMLMAC -muovia käytetään levyjen, lasien, kuppien jne. Kehittämisessä. Formaldehydi on raaka-aine metyleeni-difeniili-diisocianate (MDI) -yhdisteen, polyuretaanin esiasteen synteesiin.
Polyuretaani
Polyuretaania käytetään eristimenä jääkaapissa ja pakastimissa, pehmustettuna huonekaluihin, patjoihin, pinnoitteisiin, liimat, pohjat jne.
Butiraldehydi
Butiraldehydi on 2-etyyliheksanolin synteesin tärkein edeltäjä, jota käytetään pehmittimenä. Sillä on miellyttävä omena -aromi, joka sallii sen käytön ruoassa aromina.
Sitä käytetään myös kumiskiihdyttimiin. Se puuttuu välituotteena liuottimien valmistukseen.
Asetaldehydi
Asetaldehydiä käytettiin etikkahapon tuotannossa. Mutta tämän asetaldehydin toiminnan merkitys on vähentynyt, koska metanolihiilenpoistoprosessi on siirtänyt sen syrjäyttämään sen.
Synteesi
Muita aldehydejä ovat oksoalkoholien esiasteet, joita käytetään pesuaineiden tuotannossa. SO -kekseliä oksoalkoholeja valmistetaan lisäämällä hiili- ja vety monoksidi olefiiniin aldehydin saamiseksi. Ja lopuksi aldehydi on vetyä alkoholin saamiseksi.
Joitakin aldehydoja käytetään hajusteiden valmistuksessa, kuten Chanel nro 5. Monilla luonnollisilla aldehydeillä on esimerkiksi miellyttäviä hajuja: heptanaalilla on vihreän ruohon haju; oktanaali, oranssin haju; Ei -anaalinen, ruusujen haju ja sitrraali, liman haju.
Esimerkkejä aldehydeistä
Glutaraldehydi
 Glutaraldehydi. Lähde: Jynto [CC0], Wikimedia Commons
Glutaraldehydi. Lähde: Jynto [CC0], Wikimedia Commons Glutaraldehydi esittelee rakenteessaan kaksi formyyliryhmää molemmissa päissä.
Markkinoidut nimellä Cidex tai Glutararal, sitä käytetään desinfiointiaineena kirurgisten instrumenttien steriloimiseksi. Sitä käytetään syylien käsittelyssä jaloissa, levitettäessä nestettä.
Sitä käytetään myös kankaan korjausaineena histologia- ja patologialaboratorioissa.
Se voi palvella sinua: kuparisulfaatti (CUSO4): rakenne, ominaisuudet, hankkiminen, käyttöBentsaldehydi
Se on yksinkertaisin aromaattinen aldehydi, joka muodostaa bentseenirenkaan, jossa formiliryhmä on linkitetty.
Sitä löytyy manteliöljystä, joten sen ominainen haju, joka mahdollistaa sen käytön ruoan aromina. Lisäksi sitä käytetään orgaanisten yhdisteiden synteesissä, jotka liittyvät lääkkeiden valmistukseen ja muovien kehittämiseen.
Glyseraldehydi
Se on aldotriosa, sokeri, joka muodostuu kolmesta hiiliatomista. Se esittelee kaksi isomeeriä, joita kutsutaan D- ja L -enantiomeereiksi. Glyseraldehydi on ensimmäinen fotosynteesissä saatu monosakkaridi pimeän vaiheen aikana (Calvin -sykli).
Glyseraldehydi-3-fosfaatti
 Glyseraldehydi. Lähde: Jynto ja Ben Mills
Glyseraldehydi. Lähde: Jynto ja Ben Mills Ylemmässä kuvassa havainnollistetaan glyseraldehydi-3-fosfaatin rakenne. Punaiset pallot keltaisen vieressä vastaavat fosfaattiryhmää, kun taas mustana hiilirunkoon. Blancaan kytketty punainen pallo on OH -ryhmä, mutta kun musta pallo on kytketty ja jälkimmäinen valkoiseen, niin se on CHO -ryhmä.
Glyseraldehydi-3-fosfaatti puuttuu glykolyysiin, aineenvaihduntaprosessiin, jossa glukoosi hajoaa pyruvihapona tuotannon ATP: n tuotannon, elävien olentojen energiasäiliön kanssa. NADH: n tuotannon lisäksi biologinen pelkistävä aine.
Glykoleraldehydi-3-fosfaattiglykolyysissä ja fosfaatti-dihydroasetonissa johtuu d-frucease-6-6-bifhary-fosfaatista.
Glyseraldehydi-3-fosfaatti puuttuu pentoosisyklin nimeltään metaboliseen prosessiin. Tässä syntyy NADPH, tärkeä biologinen pelkistin.
11 -cis -retinal
 11 -cis -retinal
11 -cis -retinal Β-karoteeni on luonnollinen pigmentti, jota esiintyy useissa vihanneksissa, etenkin porkkanassa. Koe maksassa oksidatiivinen tauko, muuttuen siten retinolialkoholiin tai A -vitamiiniin. A-vitamiinin hapettuminen ja sen myöhempi isomerointi sen kaksoissidoksista muodostaa 11-kis-reteninin aldehydin.
Pyridoksaalifosfaatti (B6 -vitamiini)
 Pyridoksaalinen fosfaatti tai B6 -vitamiini. Lähde: Jynto ja Ben Mills.
Pyridoksaalinen fosfaatti tai B6 -vitamiini. Lähde: Jynto ja Ben Mills. Se on proteesiryhmä, joka on kiinnitetty useisiin entsyymeihin, mikä on B6 -vitamiinin aktiivinen muoto ja osallistuu estävän välittäjän GABA: n synteesiprosessiin.
Missä on sen rakenteen muotoiluryhmä? Huomaa, että tämä eroaa muista aromaattisesta renkaaseen kytketyistä ryhmistä.
Salicilaldehydi
Se on raaka -aine asetyylisalisyylihapon, kipulääkkeiden ja aspiriinin, kipulääkkeiden ja 4.
Viitteet
- Robert C. Neuman, Jr. Luku 13, karbonyyliyhdisteet: Ketonit, aldehydit, karboksyylihappot. [PDF]. Otettu: Chem.Ucr.Edu
- Germán Fernández. (14. syyskuuta 2009). Aldehydojen nimikkeistö. Otettu: Chemicicaorganica.netto
- T.W -. Graham Solomons, Craight B. Freedle. Orgaaninen kemia. (Kymmenes painos, s. 729-731) Wiley Plus.
- Jerry March ja William H. Ruskea. (31. joulukuuta 2015). Aldehydi. Otettu: Britannica.com
- Wikipedia. (2018). Aldehydit. Otettu: https: // in.Wikipedia.org/wiki/aldehydi
- Morrison, r. T. Ja Boyd, R. N. (1990). Orgaaninen kemian viides painos. Toimitus Addison-Wesley Iberoamericana.
- Carey, f. -Lla. (2006). Orgaaninen kemian kuudes painos. MC Graw Hill -toimitus.
- Mathews, ch. K -k -., Van Holde, K. JA. Ja athern, k. G. (2002). Biokemia. Kolmas painos. Toimitus Pearson Adisson Wesley.

