Kaliumbentsoaattirakenne, ominaisuudet, hankkiminen, käyttö
- 916
- 216
- Shawn Stanton II
Hän Kaliumbentsoaatti Se on orgaaninen yhdiste, jonka muodostaa ionikalium k+ ja bentsooto c -ioni6H5Kujertaa-. Sen kemiallinen kaava on c6H5Keitä tai tiivistynyt kaava C7H5Koolainen2. Se on kiteinen valkoinen kiinteä aine. Se on hygroskooppista, mikä tarkoittaa, että se imee ilmaa ilmasta.
Kaliumbentsoaattivesiliuokset ovat hiukan alkaleja. Happamassa väliaineessa bentsoaatti -ioni (C6H5Kujertaa-) pyrkii ottamaan protonin ja siitä tulee bentsoehappo (C6H5Cooh).
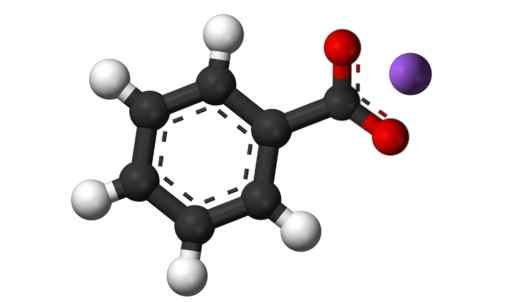
 Kaliumbentsoaatti6H5Vankka kokki. W -. OELEN [CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/3.0)]. Lähde: Wikimedia Commons.
Kaliumbentsoaatti6H5Vankka kokki. W -. OELEN [CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/3.0)]. Lähde: Wikimedia Commons. Kaliumbentsoaattia käytetään elintarvikevälityksenä, varsinkin kun niiden halutaan olevan natriumvapaa (NA). Estää ruokaa heikentymästä mikro -organismien takia.
Sitä käytetään makkaroissa, jalostetuissa virvoitusjuomissa ja leipomotuotteissa muun muassa. Todennäköisesti sen säilöntäaine johtuu bentsoehaposta (C6H5COOH), joka on muodostettu alhaisella pH: lla, joka estää sienten ja bakteerien lisääntymisen.
Vaikka terveysjärjestöt hyväksyvät kaliumbentsoaattia, on kätevää olla väärinkäyttämättä niiden käyttöä, koska on havaittu, että hiirien sikiöt voivat vaikuttaa.
[TOC]
Rakenne
Kaliumbentsoaatti on orgaaninen suola, toisin sanoen karboksyylihapon suola, koska se on bentsoehapon kaliumsuola. Se muodostuu K+ -kaliumkationista ja bentsoaatti -anionista C6H5Kujertaa-.
Bentsooto -anionin6H5Kujertaa- Se muodostuu bentseenirenkaasta C6H5- ja karboksylaatit -COO -ryhmä-.
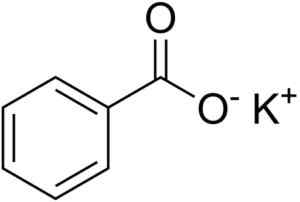 Kaliumbentsoaatin kemiallinen rakenne. Edgar181 [julkinen alue]. Lähde: Wikimedia Commons.
Kaliumbentsoaatin kemiallinen rakenne. Edgar181 [julkinen alue]. Lähde: Wikimedia Commons. Näiden kahden ionin välinen liitto on vahva sähköstaattinen liitto, joka pitää ne kiteisessä verkossa.
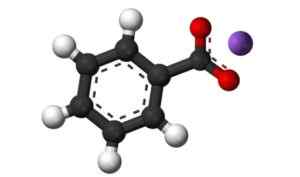 Kaliumbentsoaatin 3D -rakenne. Musta = hiili; Valkoinen = vety; punainen = happi; Violetti = kalium. Claudio Pistilli [CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0)]. Lähde: Wikimedia Commons.
Kaliumbentsoaatin 3D -rakenne. Musta = hiili; Valkoinen = vety; punainen = happi; Violetti = kalium. Claudio Pistilli [CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0)]. Lähde: Wikimedia Commons. Nimikkeistö
- Kaliumbentsoaatti
- Bentsoehapon suola
Ominaisuudet
Fyysinen tila
Kiteinen valkoinen kiinteä aine.
Molekyylipaino
160 212 g/mol
Liukoisuus
Liukeneminen veteen.
PHE
Kaliumbentsoaattivesiliuokset ovat hiukan emäksiä.
Kemialliset ominaisuudet
Se on hygroskooppinen, ts. Se on kiinteä, joka imee vettä ympäristöstä helposti.
Kaliumk -ionin välinen liitto+ ja bentsooto c -ioni6H5Kujertaa- Kuten useimmissa ionisissa yhdisteissä, se voidaan voittaa vain korkean lämpötilan tai erittäin polaarisen liuottimen kaltaisella vedellä.
Voi palvella sinua: tehokas ydinkuormaBentsooto -anionin6H5Kujertaa- Se on kohtalaisen yksinkertainen, ja siinä on huomattava taipumus yhdistää protoneihin. Reagoi veteen ottaen protonin H+ Bentsoehapon muodostamiseksi (c6H5Cooh) ja tämä johtaa OH -ionipitoisuuden lisääntymiseen-.
C6H5Kujertaa- + H2Tai ⇔ c6H5COOH + OH-
Tästä syystä vesipitoiset kaliumbentsoaattiliuokset ovat hieman alkaleja.
Saada
Kaliumbentsoaatin valmistamiseksi bentsoehappo neutraloidaan (C6H5Cooh) kaliumkarbonaatilla (k2Yhteistyö3) Veden vähimmäistilavuudessa kirkkaan liuoksen saamiseksi, josta suola kiteytyy.
2 c6H5Cooh + k2Yhteistyö3 → 2 c6H5Kujertaa-K -k -+ + H2Tai + Co2↑
Sitten kiteytetty kaliumbentsoaattisuola pestään useita kertoja eetterillä ja kuivua.
Sovellukset
Jalostetussa elintarviketeollisuudessa
Kaliumbentsoaattia käytetään laajasti antimikrobisena aineena juomien säilyttämisessä, hedelmäjohdannaisissa, leipomotuotteissa ja muissa aterioissa.
 Jotkut leipomotuotteet voivat sisältää kaliumbentsoaattia. Kirjoittaja: Andrew Martin. Lähde: Pixabay.
Jotkut leipomotuotteet voivat sisältää kaliumbentsoaattia. Kirjoittaja: Andrew Martin. Lähde: Pixabay. Se on elintarvikkeiden säilöntäaine, joka kykenee estämään, viivästymään tai lopettamaan ruoan käymisprosessia, joidenkin sienten ja bakteerien takia.
Ympäristönsuojelun tai EPA -viraston mukaan (lyhenne englanniksi Ympäristönsuojeluvirasto) Kaliumbentsoaatti on varmennettu yhdisteenä, joka on vähän huolestuttava ihmisten terveydelle.
Sieniä vastaan
Se on antimikoottinen aine, koska se voi tuhota ne tukahduttamalla heidän kykynsä kasvaa tai lisääntyä. Se ei ole eläinten tai ihmisten organismin kudoksille, vaan estäjä, joka viivästyy tai jarruttaa sienten etenemistä ruoassa tai juomissa.
Jotkut hometyypit tuottavat aflatoksiineja kutsuvia aineita, jotka ovat uhka sekä ihmisille että eläimille, koska ne ovat myrkyllisiä, ne voivat tuottaa syöpää ja mutaatioita.
Suurin osa muotista estetään pitoisuuksissa 0,05-0,10% kaliumbentsoaatista. Tämän suorituskyky riippuu pH: sta, koska pieni pH on tehokkaampi antihongos.
Voi palvella sinua: kalsiumhydroksidi (CA (OH) 2): rakenne, ominaisuudet, hankkiminen, käyttö Käsitellyt virvoitusjuomat voivat sisältää kaliumbentsoaattia. Kirjoittaja: Lisakara. Lähde: Pixabay.
Käsitellyt virvoitusjuomat voivat sisältää kaliumbentsoaattia. Kirjoittaja: Lisakara. Lähde: Pixabay. Tämä johtuu siitä, että todellisuudessa antimikoottinen vaikutus on bentsoehapossa C6H5COOH, joka on kaliumbentsoaatin konjugoitu happo. Tämä happo muodostuu pH: n alla, toisin sanoen suuren määrän vetyioneja H+-
Kaliumbentsoaatti + vety -ionit → bentsoehappo + kaliumioulit
C6H5Kokki + h+ → C6H5Cooh + k+
Joidenkin tutkijoiden mukaan niiden tehokkuus johtuu osittain bentsoehapon liukoisuudesta mikro -organismisolukalvoon. Tämäntyyppinen happo lisää protonien virtausta mainitun kalvon kautta.
Tämä aiheuttaa sienisolun tiettyjen toimintojen keskeyttämisen tai hajoamisen.
Bakteereja vastaan
Se on aine, joka toimii joitain bakteereja vastaan. Se lisätään ruokaan, kuten jalostettuihin makkaroihin, jalostettuihin kinkkuihin (valmiiksi syömään) ja joitain juomia.
On testattu Listeria monocytogenes, bakteeri, joka voi aiheuttaa tämän saastuneen ruoan kuluttavien ihmisten kuoleman. Tuottaa kuumetta, oksentelua ja ripulia, muun muassa oireita.
On havaittu, että ruokaa, jota on käsitelty kaliumbentsoaatilla ja jotka on saastunut Listeria Niitä on ylläpidettävä alle -2,2 ° C: n lämpötiloissa, jotta tällaisia bakteereja ei toisteta.
 Makkarat ja muut makkaralihat voivat sisältää kaliumbentsoaattia. Kirjoittaja: Valokuvien myynti StockGencesillä ei salli. Lähde: Pixabay.
Makkarat ja muut makkaralihat voivat sisältää kaliumbentsoaattia. Kirjoittaja: Valokuvien myynti StockGencesillä ei salli. Lähde: Pixabay. Toisaalta elektronisäteilyn käyttö on testattu kaliumbentsoaatin vaikutuksen tehostamiseksi bakteereja vastaan, mutta on määritetty, että bentseeni C on tuottanut6H6 joka on myrkyllinen yhdiste.
Siksi, vaikka ruoka sisältää kaliumbentsoaattia.
Useissa sovelluksissa
Kuultujen lähteiden mukaan kaliumbentsoaattia käytetään myös liimoissa ja sitoutumisaineissa moniin käyttötarkoituksiin. Se lisätään savukkeisiin ja tupakkaan tai liittyy näiden valmistukseen.
Voi palvella sinua: Neon: Historia, ominaisuudet, rakenne, riskit, käyttötarkoituksetSitä käytetään henkilökohtaisen hygienian tuotteissa, kuten kosmetiikka, shampoo, hajusteet, saippuat, voiteet jne. Se on myös osa maalauksia ja pinnoitteita.
Negatiiviset vaikutukset elintarvikkeiden nauttimiseen kaliumbentsoaatilla
Tietyt tutkijat havaitsivat, että kaliumbentsoaatti tuottaa haitallisia vaikutuksia hiirien sikiöihin.
Vaikka kaliumbentsoaatille altistuneisiin aikuisten hiiriin ei ollut vaikutuksia.
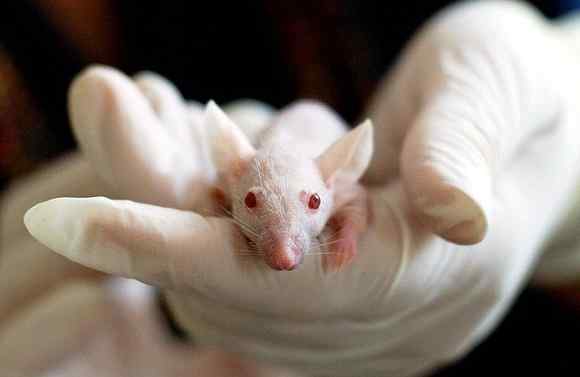 Laboratoriokokemusten mukaan äidin nauttimat kaliumbentsoaatti voi vaikuttaa hiirien sikiöihin. Kirjoittaja: Tibor Janosi Mozes. Lähde: Pixabay.
Laboratoriokokemusten mukaan äidin nauttimat kaliumbentsoaatti voi vaikuttaa hiirien sikiöihin. Kirjoittaja: Tibor Janosi Mozes. Lähde: Pixabay. Tämä tarkoittaa, että sikiöt ovat herkempiä kaliumbentsoaatille kuin aikuiset hiiret.
Viitteet
- Mandal, P.K -k -. et al. (1978). Bentsoehapon ja bentsoaatti -ionin viskositeettikäyttäytyminen vesiliuoksessa. Journal of Solution Chemistry, Vol. 7, ei. 1, 1978. Linkki palautettu.Jousto.com.
- Rusul, G. ja Marth, ja.H. (1987). Kasvu ja aflatoksiinin tuotanto Aspergillus parasiticus NRRL 2999 kaliumbnezaatin tai kaliumsorbaatin ja alkuperäisissä pH -arvoissa. J Food PR. 1987; 50 (10): 820-825. NCBI toipunut.Nlm.NIH.Hallitus.
- Valaistus. et al. (2005). Orgaanisten happasuolojen estäjävaikutukset Listeria monocytogenes Frankfurters. J Food PR. 2005; 68 (3): 499-506. NCBI toipunut.Nlm.NIH.Hallitus.
- Zhu, m.J -. et al. (2005). Antimikrobisten ainesosien ja säteilytyksen vaikutus Listeria monocytogenes -elokuvien selviytymiseen ja valmiste-e-our-kalkkuna-kinkun laatuun. Sci. 2005; 84 (4): 613-20. NCBI toipunut.Nlm.NIH.Hallitus.
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Kaliumbentsoaatti. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus.
- Afshar, m. et al. (2013). Kaliumbentsoaatin LONT -termin kulutus silmien kehitykseen BALB/C -sikiön hiirien LONT -termin kulutus. Iran J Basic Med Sci. 2013; 16 (4): 584-589. NCBI toipunut.Nlm.NIH.Hallitus.
- Lyijy, d.R -. (Toimittaja) (2003). CRC: n kemian ja fysiikan käsikirja. 85th CRC -lehdistö.
- Morrison, r.T. ja Boyd, R.N. (2002). Orgaaninen kemia. 6. painos. Prentice-sali.
- « Hallinnon institutionaaliset arvot, mitä he ovat, tärkeitä
- Magneettiset sokkiyksiköt, kaavat, laskelmat, esimerkit »

