Natrium boorihydridi (NABH4) rakenne, ominaisuudet, käytöt

- 1187
- 335
- Joshua Emmerich
Hän natriumboori Se on epäorgaaninen kiinteä aine, jonka kemiallinen kaava on Nabh4. Sitä voidaan pitää edustavan alkalista boorohydrurosta ja on yleisin näistä. Se on kiteinen valkoinen kiinteä aine.
Kosketuksessa veden kanssa, Nabh4 voi tuottaa lämpöä ja vetyä H2 mikä on polttoainetta, joten sitä on käsiteltävä varoen. Sillä helppous tuottaa hydridi -ionit H-, Natriumboori on kohtalaisen vähentävä yhdiste, joten sitä käytetään laajasti kemiallisissa reaktioissa tätä tarkoitusta varten.
 Natriumborohydridi, nabh4, kiinteä. Ondřej Mangl [julkinen alue]. Lähde: Wikimedia Commons.
Natriumborohydridi, nabh4, kiinteä. Ondřej Mangl [julkinen alue]. Lähde: Wikimedia Commons. Sen pelkistävää ominaisuutta käytetään myös paperiteollisuudessa, koska se mahdollistaa massan ja paperin kirkkauden ja stabiilisuuden ominaisuuksien parantamisen, kun se on selluloosan hapettumista, paperin pääkomponenttia.
Koska veden läsnä ollessa se voi helposti muodostaa vetyä, myös mahdollisuutta käyttää sitä palautuvana vetylähteenä polttokennoissa.
Siinä on muita käyttöä kaikkia sen pelkistävän omaisuuden, kuten lääketeollisuuden, perusteella.
[TOC]
Rakenne
Natriumboori on ioninen yhdiste. Se muodostuu boorihydridianionilla [bh4-- yhdessä natriumkationin kanssa+.
Anioni [bh4-- Se on tetraedrinen.
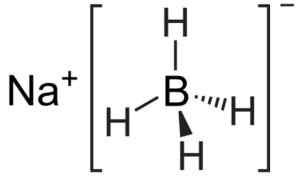 Natrium boorihydridirakenne. Kemikungen [julkinen alue]. Lähde: Wikimedia Commons.
Natrium boorihydridirakenne. Kemikungen [julkinen alue]. Lähde: Wikimedia Commons. Sen Lewisin rakenne on seuraava:
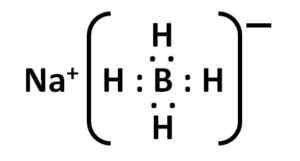 Nabh Lewisin elektroninen rakenne4. Kirjoittaja: Marilú Stea.
Nabh Lewisin elektroninen rakenne4. Kirjoittaja: Marilú Stea. Nimikkeistö
-Natriumboori
-Natriumtetrahydroaatti
-Natriumtetrahydrurorat
Fyysiset ominaisuudet
Fyysinen tila
Kiteinen valkoinen kiinteä aine.
Molekyylipaino
37,84 g/mol
Itsensuuntainen lämpötila
∼ 220 ºC
Hajoamislämpötila
> 250 ºC
Tiheys
1 074 g/cm3 20 ºC
Voi palvella sinua: Grignard Reagenssi: valmistelu, sovellukset, esimerkitLiukoisuus
Nabh4 Se on melko liukoinen veteen (55 g/100 ml 25 ° C: ssa), missä osittain hydrolysoivat. Se liukenee tetrahydrofuranoon (THF) ja on liukenematon dietyl -eetterissä.
Kemialliset ominaisuudet
Natriumboori liuotetaan veteen, missä se kärsii alkuperäisestä hajoamisesta tai hydrolyysistä, joka tekee liuoksen emäksisen, mikä estää seuraavan hydrolyysin.
[BH4-- + H2O → B (OH)3 + H2↑ + OH-
Tämä selitetään, koska [bh4-- vuorovaikutuksessa H: n kanssa+ Vettä, missä H+ Ottaa hydridi -anioni- Muodostaa h2. Voidaan sanoa, että BH3 kilpailee H: n kanssa+ Hydridille H-.
Happamassa väliaineen hydrolyysissä on valmis H -ionien runsauden vuoksi+.
Nabh4 Se on vakaa kuiva ilmassa. Se ei ole haihtuva.
Natriumboori on hydridi -ionipitoisuuden vuoksi pelkistävä yhdiste. Se mahdollistaa karbonyyliryhmän C = o C-OH: n, ts. Karbonyyliyhdisteiden alkoholiin.
Nabh4 Yksinään se ei vähennä kaksoissidoksia c = c, edes konjugaatit karbonyyliryhmien kanssa -c = c -c (= o)-.
Kuitenkin kosketuksiin protonihapojen (kuten HCL) tai Lewis -happojen (kuten BCL: n kanssa3 tai Alcl3) Diborano B muodostuu2H6. Ja jos tämä reaktio suoritetaan orgaanisten yhdisteiden läsnä ollessa, joissa on kaksoissidokset c = c diborano b2H6 Suorittaa näiden hydrobacion.
Sopivien katalyyttien ja spesifisten olosuhteiden läsnä ollessa natriumboori voi vähentää erityyppisiä funktionaalisia ryhmiä.
Riskejä
Veden hydrolyysireaktion lämpö riittää siihen muodostuneen vedyn kytkemiseen. Joten on tärkeää olla varovainen manipuloidessaan sitä.
Nabh4 Se on helposti päällä ja on helposti poltettu.
Saada
Tyypillinen NABH -valmistusreaktio4 Se tapahtuu natriumhydridin NAH: n ja B: n kautta (OCH3-A3 lämpötilassa noin 250 ºC:
Se voi palvella sinua: vesielektrolyysi4 NAH + B (OCH3-A3 → Nabh4 + 3 Naoch3
Sovellukset
Vähennyksen kemiallisissa reaktioissa
Hones H: n lähde-, Nabh4 Se on pelkistävä yhdiste ja sitä käytetään muiden kemiallisten yhdisteiden valmistukseen. Tätä varten sitä käytetään apratoottisissa polaarisissa liuottimissa, ts. Ilman H -protoneja+, kuten dimetyylisulfoksidi, heksaametyylifosforinen ja dimetyyliformamidi.
Sitä käytetään pelkistävänä aineena sekä orgaanisissa että epäorgaanisissa kemian reaktioissa.
Se mahdollistaa aldehydojen vähentämisen ensisijaisiin alkoholeihin ja ketoneihin sekundaarisiin alkoholiin.
Se vähentää myös alkyylihalogenideja hiilivetyihin, kuten jododaaniin dekaaniksi.
Jos se toimii yksin, pelkistyksen tekemisessä ei vaikuta muihin funktionaalisiin ryhmiin, kuten esteriin, karboksyylihappoon, nitriiliin ja sulfoniin.
Sen ominaisuus, että se ei vähennä kaksoissidoksia c = C, edes konjugaatit karbonyyliryhmien kanssa -c = c-c (= o)-antaa sinun valmistaa tyydyttymättömät alkoholit -C = C-C-CH2-vai niin.
Aromaattisten yhdisteiden vähentäminen Nitradoksen vastaaviin aniliineihin vaatii katalyyttien, kuten kobolttikloridin tai tinan, läsnäolon. Vähennä disulfideja tioleiksi.
Sopivien olosuhteiden ja katalyyttien läsnä ollessa se mahdollistaa karboksyylihappojen, esterien, keskellä, nitriilien, imiinin, epoksidien ja jopa kaksinkertaisen ja kolminkertaisen sidoksen vähentämisen vähentämisen.
H2 Polttokennoissa
Nabh4 Se voidaan muuttaa polttokennoksi.
Nabh4 KOH: n tai NaOH: n emäksisen liuoksen läsnä ollessa se hydrolysoidaan ja tuottaa vety H2 jota voidaan käyttää polttoaineena polymeeristen elektrolyyttien polttoainakinnassa.
Sitä on tutkittu myös H -materiaalina H: n varastointia varten2 palautuvasti.
NABH -nanohiukkaset syntetisoidaan4 ja vakauttaa pinta -aktiivisen aineen kanssa. NICL -hoidon jälkeen2 Muodostuu suojakerros tai pinnoite, joka säätelee H: n vapautumista2 täysin palautuvasti.
Se voi palvella sinua: hopea -nitraatti (AGNO3): rakenne, ominaisuudet, käyttö, toksisuusTämä uusi nanometrinen materiaali mahdollistaisi H: n käytön2 Tuotettuna puhtaana ja uusiutuvaa polttoainetta.
 Ajoneuvo, joka toimii vetypolttokennolla. DR. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)]. Lähde: Wikimedia Commons.
Ajoneuvo, joka toimii vetypolttokennolla. DR. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)]. Lähde: Wikimedia Commons. Sellu- ja paperiteollisuudessa
Natriumbooria käytetään parantamaan massa- ja paperin kirkkautta ja muita fysikaalisia ominaisuuksia.
Paperin selluloosimatriisin hajoaminen tapahtuu monimutkaisten prosessien kautta, jotka sisältävät hapettumista. Hydroksyyliryhmät hapettelevat karbonyyli- ja karboksyyli.
Kun käsitellään massaa tai paperia NABH: lla4, Tämä vähentää aldehydoja ja ketoneja ryhmiin -OH vaikuttamatta happamarboksyyliryhmiin, parantaen stabiilisuutta ja kirkkautta arvoihin, jotka ovat suurempia kuin nimikirjaimet.
 Nabh4 mahdollistaa paperin kirkkauden parantamisen. Kirjoittaja: RawPixel. Lähde: Pixabay.
Nabh4 mahdollistaa paperin kirkkauden parantamisen. Kirjoittaja: RawPixel. Lähde: Pixabay. Useissa käyttötarkoituksissa
Natriumbooria käytetään jäteveden hoitamiseen, aromin virheellisenä aineena elintarvike- ja juomateollisuudessa, pinnoiteaineina ja pintojen hoidossa tupakan tuotannossa, lääke-, tekstiili- ja tekstiiliteollisuuden nahka.
Viitteet
- Kristitty, m.Lens. ja Aguey-Zinsou, K.-F. (2012). Ydin-kuoren strategia, joka johtaa NABH: n korkeaan palautuvaan vedyn varastointikapasiteettiin4. ACS Nano 2012, 6, 9, 7739-7751. Pubista toipunut.ACS.org.
- Nora de Souza, M.V. ja Alves V., T.R -. (2006). Natrium boorihydridin välittämät viimeaikaiset menetelmät eri yhdisteiden luokkien pelkistämisessä. Sovellus. Organometaalinen. Kemia. 2006; 20: 798-810. Haettu verkkokirjastosta.Viiva.com.
- Imamoto, t. (1991). Vähennys. Natriumboorihydridi. Orgaanisen synteesin ymmärtämisessä. ScienEdirect.com.
- L.C. (1986) paperin stabilointi natriumborohydridikäsittelyn kautta. Historiallisissa tekstiili- ja paperimateriaaleissa. Luku 24. Sivut 427-441. Kemian kehitys, osa 212. Pubista toipunut.ACS.org.
- Puuvilla, f. Albert ja Wilkinson, Geoffrey. (1980). Edistynyt epäorgaaninen kemia. Neljäs painos. John Wiley & Sons.
- Morrison, Robert Thornton; ja Boyd, Robert Neilson. 1992. Orgaaninen kemia. Prentice-sali. ISBN 81-203-0765-8.
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Natriumboorihydridi. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus.
- « Sosiaalisen ilmiön ominaisuudet ja esimerkit
- Kobolttikloridi (COCL2 (rakenne, nimikkeistö, ominaisuudet »

