Prosenttipitoisuus

- 1483
- 426
- Eddie Hackett
Mikä on prosentuaalinen pitoisuus?
Se prosenttipitoisuus Se on tapa ilmaista liuenneen aineen suhde sadassa osassa sekoitusta tai liuosta. On huomattava, että nämä "osat" voidaan ilmaista massa- tai tilavuusyksiköinä. Tämän konsentraation ansiosta tiedetään liuoksen koostumus, joka, toisin kuin puhtaan yhdisteen koostumus, ei ole vakio.
Sen koostumuksen lisäksi vaihtelee, vaan myös sen organoleptiset ominaisuudet. Alemman kuvan teepurkki hankkii voimakkaampia makuja (ja värillisiä), kun jääveteen liuenee enemmän mausteita. Vaikka niiden ominaisuudet muuttuvat, näiden mausteiden pitoisuus pysyy vakiona.

Jos oletamme, että 100 grammaa näistä liuotetaan veteen ja sekoitetaan sitten tarpeeksi liuoksen homogenisoimiseksi, grammat jakautuvat purkkiin. Teepitoisuus pysyy vakiona, vaikka nestepitoisuus jaetaan eri astioihin.
Tämä vaihtelee vain, jos purkkiin lisätään enemmän vettä, mikä, vaikka se ei modifioida liuenneen mausteen alkuperäistä massaa (liuenneen aineen), muuttaa sen pitoisuutta. Teenopeuden esimerkissä tämä pitoisuus voidaan ilmaista kätevästi liuenneen aineen massaan veden tilavuuden välillä.
Siten äärettömillä tapauksilla, joissa näillä pitoisuuksien laskelmilla on ratkaiseva rooli.
Mikä on ratkaisu?
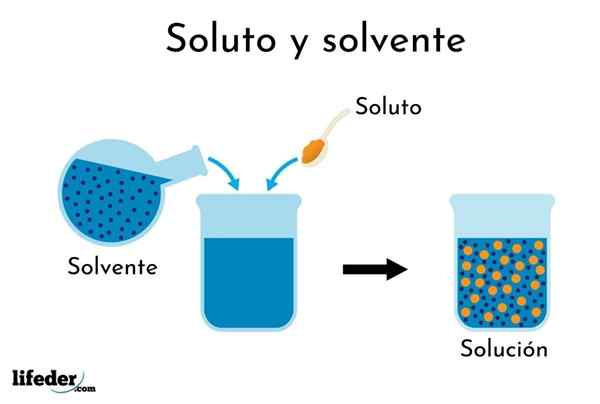 Liuenneen aineen liukeneminen liuottimeen
Liuenneen aineen liukeneminen liuottimeen Termin "ratkaisun" ymmärtäminen on välttämätöntä ennen sen pitoisuuden prosentuaalisten lausekkeiden käsittelemistä.
Liuos on homogeeninen tai tasainen seos kahdesta tai useammasta aineesta, joiden hiukkaset ovat atomia tai molekyylikokoisia.
Se voi palvella sinua: mitkä ovat negatiiviset vaikutukset veden liukoisuuteen?Tämän komponentit ovat liuennettua ja liuotinta. Liuennin aine on materiaali, joka on liuennut liuokseen, joka on vähemmän suhteessa. Liuotin on liuoksen dispersion keino ja se on suurempi osuus (kuten vettä teepurkissa).
Prosentuaalisen pitoisuuden ominaisuudet
- Prosenttipitoisuus aiheuttaa mukavuutta välttää molaarisuuslaskelmat ja muut pitoisuusyksiköt. Monissa tapauksissa riittää tietää liuenneen liuenneen aineen määrä. Kemiallisten reaktioiden osalta se kuitenkin jättää sivulle moolikonsentraation avulla.
- Helpottaa massan suojelulain todentamista.
- Se ilmaistaan osina sataa liuosta, jonka sisällä liuenneen aineen lasketaan.
- Liuenneen aineen ja liuoksen välinen suhde voidaan ilmaista massayksiköissä (grammissa) tai tilavuudessa (millilitrat).
Kuinka se lasketaan?
Tapa laskea se riippuu yksiköistä, joissa haluat ilmaista sen. Matemaattinen laskelma on kuitenkin pohjimmiltaan sama.
Molemmat painon painoa painoprosentti m/m
% (m / m) = (liuoksen liuenneen / gramman grammat) ∙ 100
Liuoksen prosenttiosuus osoittaa liuenneen gramman määrän jokaisessa 100 grammassa liuoksessa.
Esimerkiksi 10 % m/m NaOH: n liuos sisältää 10 grammaa NaOH: ta 100 grammaa liuosta kohti. Sitä voidaan tulkita myös tällä tavalla: 10 g NaOH: ta liuotetaan 90 g vettä (100-10).
Molemmat prosenttiosuus tilavuudessa % m/v
% (m / v) = (grammat liuennettua / millilitraa liuosta) ∙ 100
Voi palvella sinua: kvaternääriset yhdisteet: ominaisuudet, koulutus, esimerkitMilligrammien prosenttiosuus on pitoisuusyksikkö, jota käytetään usein kliinisissä raporteissa kuvaamaan liuenneen aineen erittäin alhaisia pitoisuuksia (esimerkiksi veren mineraalien jäljet).
Erityisenä tapauksessa on seuraava esimerkki: typen taso ihmisen veressä on 32 mg%, mikä tarkoittaa, että liuenneen typpeä on 32 mg / 100 ml veri.
Molemmat prosenttia tilavuudessa % V/V
% (tilavuus / tila
Liuoksen tilavuuden prosenttimäärä osoittaa millilitran määrän liuenneen aineen jokaisesta 100 millilitrasta liuoksesta.
Esimerkiksi 25%: n alkoholiliuos vedessä, sisältää 25 millilitraa alkoholia 100 millilitraa kohti liuosta tai mikä on sama: 75 ml vettä liukenee 25 ml alkoholia.
Esimerkkejä prosentuaalisista pitoisuuslaskelmista
Esimerkki 1
Jos heillä on 7 g Kioa3, Kuinka monta grammaa 0,5 % m/m liuosta voidaan valmistaa tällä suolalla?
0,5 % m/m -liuos on hyvin laimennettu, ja se tulkitaan seuraavasti: jokaista 100 grammaa liuosta on 0,5 grammaa KIO: ta3 liuennut. Joten tämän liuoksen grammien määrittämiseksi käytetään muuntamiskertoimia:
7 g Kio3 ∙ (100 g aurinko/ 0.5 g Kio3) = 1400 g tai 1.4 kg liuosta.
miten se on mahdollista? On selvää, että suuri määrä massaa tuli vedestä; Siten 7 grammaa Kion3 He liukensivat 1393 grammaa vettä.
Voi palvella sinua: Eräreaktori: Ominaisuudet, osat, sovelluksetEsimerkki 2
Jos haluat valmistaa 500 grammaa cuso -liuosta4 1 %, kuinka monta grammaa perussuolaa on välttämätöntä?
Muutostekijöitä käytetään CUSO: n G: n puhdistamiseen4 Haluttu:
500 g Cuso Sunia4 ∙ (1 g cusoa4/ 100 g Cuso Sunia4) = 5 g cusoa4
Eli 5 g cusoa liukenevat4 (kirkkaan sinertävän värit suola) 495 g vettä (noin 495 ml)
Esimerkki 3
Jos sekoitetaan 400 ml vettä, 37 grammaa sokeria, 18 grammaa suolaa ja 13 grammaa natriumsulfaattia (NA2Sw4), Mikä on massaprosenttipitoisuus jokaiselle seoskomponentille?
Jos oletetaan, että vesitiheys on 1 g/ ml, seoksessa on 400 g vettä. Liuoskomponenttien kokonaismassan lisääminen on: (400 + 37 + 18 + 13) = 468 g liuosta.
Tässä laskelma on suora ja yksinkertainen:
%Vesi m/ m = (400 g vettä/ 468 g aurinkoa) ∙ 100 = 85.47
%Sokeria m/ m = (37 g sokeria/ 468 g aurinkoa) ∙ 100 = 7.90
%Suolaa m/ m = (18 g suolaa/ 468 g aurinkoa) ∙ 100 = 3.84
%Na2Sw4 m/m = (13 g NA2Sw4/ 468 g aurinko) ∙ 100 = 2.77
Kaikkien yksittäisten massaprosenttien lisääminen on: (85,47 + 7,90 + 3,84 + 2,77) = 99,98 % ≈ 100 %, kokonaisseos.

