Deksyyribosa -rakenne, toiminnot ja biosynteesi
- 4452
- 171
- Dr. Travis Reichert
Se deoksihiomainen jompikumpi D-2-Desoxirribosa Se on viiden hiilen sokeri, joka koostuu deoksiribonukleiinihapon (DNA) nukleotideja. Tämä sokeri toimii perustana fosfaattiryhmän ja typpipohjan yhdistymiselle, jotka muodostavat nukleotideja.
Hiilihydraatit ovat yleensä välttämättömiä molekyylejä eläville olentoille, ne täyttävät erilaisia välttämättömiä toimintoja, ei vain molekyyleinä, joista energiaa voidaan erottaa soluille, vaan myös rakentaa DNA -ketjuja, joiden kautta geneettinen tieto välitetään.
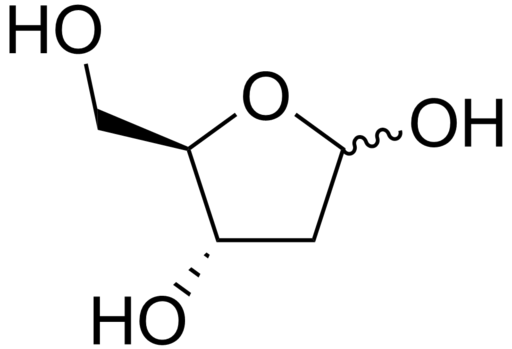 Deoksiriboosin kemiallinen rakenne (lähde: Edgar181 [julkinen alue] Wikimedia Commonsin kautta)
Deoksiriboosin kemiallinen rakenne (lähde: Edgar181 [julkinen alue] Wikimedia Commonsin kautta) Kaikilla sokereilla tai hiilihydraateilla on yleinen kaava cnH2non, deoksihiobosin tapauksessa sen kemiallinen kaava on C5H10O4.
Deoksiriboosi on sokeri, joka rakentaa DNA: ta ja eroaa vain riboosista (RNA: n koostuva sokeri), jossa siinä on vetyatomi (-h) hiilessä 3, sillä välin riboosissa on hydroksyylifunktionaalinen ryhmä (- OH) sisällä sama sijainti.
Tästä rakenteellisesta samankaltaisuudesta johtuen Riboos on tärkein aloitussubstraatti deoksiribosisokerien solun synteesille.
Keskimääräisen solun RNA: n määrä on lähes 10 kertaa suurempi kuin DNA: n, ja kierrätetyn RNA -fraktion, siirtymällä kohti deoksiriboosin muodostumista, on tärkeä vaikutus solujen eloonjäämiseen.
[TOC]
Rakenne
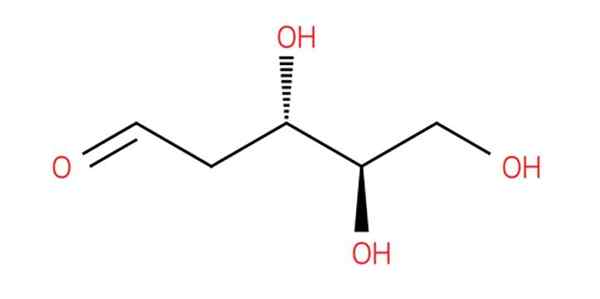
Dexyribose on monosakkaridi, joka koostuu viidestä hiiliatomista. Siinä on aldehydiryhmä, joten se luokitellaan AldoPentosa -ryhmään (Aldo, aldehydi ja Pento viidelle hiileille).
Hajottamalla deoksiribosin kemiallinen koostumus voimme sanoa, että:
Tämä koostuu viidestä hiiliatomista, aseman 1 hiilessä on aldehydiryhmä, aseman 2 hiilessä siinä on kaksi vetyatomia ja hiilessä asemassa 3 on kaksi erilaista substituenttia, nimittäin: hydroksyyliryhmä (-------------------------- Voi) ja vetyatomi.
Se voi palvella sinua: hydrokoloidiHiili asennossa 4, samoin kuin asennossa 3, on OH -ryhmä ja vetyatomi. Hydroksyyliryhmän happiatomin kautta tässä asennossa molekyyli voi hankkia syklisen konformaationsa, koska se on kytketty hiileen asennossa 1.
Viides hiiliatomi on kyllästetty kahdella vetyatomilla ja se sijaitsee molekyylin pääpäässä renkaan ulkopuolella.
Hiiliatomin 1 aldehydiryhmässä typpialustat, jotka yhdessä sokerin kanssa muodostavat nukleosidit (nukleotidit ilman fosfaattiryhmää), liitetään. Hiiliatomiin 5.
DNA -potkurissa tai juosteessa nukleotidin hiilifosfaattiryhmä 5 on se, joka liittyy toisen nukleotidiin kuuluvan hiilen OH -ryhmään 3 asemassa 3 ja niin edelleen, ja niin edelleen.
Optiset isomeerit
Niistä viidestä hiiliatomista, jotka muodostavat Deoxyriboosin tärkeimmät luuranat. Hiili asennossa 2 on epäsymmetrinen näiden suhteen, koska sitä ei liitetä mihinkään ryhmään OH.
Siksi, ja tämän hiiliatomin mukaan deoksihioboosi voidaan saavuttaa kahdessa "isoformissa" tai "optisissa isomeereissä", jotka tunnetaan nimellä L-desoksiriboosi ja D. Molemmat muodot voidaan määritellä karbonyyliryhmästä Fisherin rakenteen yläosassa.
Se on nimetty "d -desexirribosa" kaikille deoksiribosasiksi, joissa ryhmä -OH Carbon 2 on järjestetty oikealle, kun taas muodoissa "l -disoksihiobose" on ryhmä -OH vasemmalle.
Voi palvella sinua: Orgaaniset yhdisteet: Ominaisuudet, luokittelu, esimerkitSokerien "D" -muoto, mukaan lukien deoksiriboosi, on hallitseva organismien aineenvaihdunnassa.
Funktiot
Desoxyribosa on sokeri, joka toimii monien tärkeiden makromolekyylien, kuten DNA: n ja korkean energian nukleotidien, kuten ATP, ADP, AMP, GTP, rakenteellinen lohko.
Deoksiriboosin syklisen rakenteen esittämä ero ribosaan nähden tekee ensimmäisestä paljon vakaammasta molekyylistä.
Happiatomin puuttuminen hiili 2: ssa tekee deoksiriboseista vähemmän sokerialttiita pelkistykseen, etenkin Riboosiin verrattuna. Tämä on erittäin tärkeää, koska se tarjoaa vakauden molekyyleille, joihin se on osa.
Biosynteesi
Deoksiriboosi, kuten riboosi, voidaan syntetisoida eläimen kehossa reiteillä, joihin liittyy muiden hiilihydraattien (yleensä kuusosuojaus, kuten glukoosi) tai pienemmän hiilihydraattikondensaation rappeutumisen.
Ensimmäisessä tapauksessa, toisin sanoen deoksiriboosin saaminen ”ylivoimaisten” hiilihydraattiyhdisteiden hajoamisesta, tämä on mahdollista solujen metabolisen kyvyn ansiosta suorittaakseen kylkiluun 5-fosfaatin suoran muuntamisen, joka saadaan tiellä saadaan tiellä olevan tien kautta saatu Pentoosifosfaatti riboosi 5-fosfaatissa.
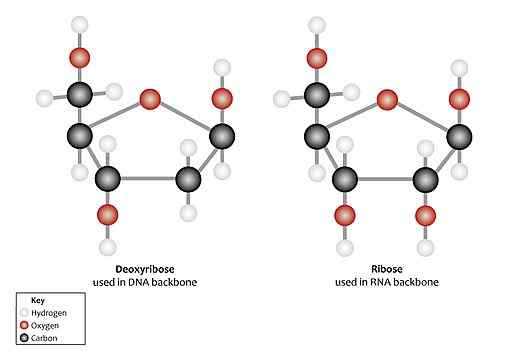 Riboosin ja deoksiriboosin välinen rakenteellinen vertailu (lähde: Genomics Education Program [CC 2: lla.0 (https: // creativecommons.Org/lisenssit/by/2.0)] Wikimedia Commonsin kautta)
Riboosin ja deoksiriboosin välinen rakenteellinen vertailu (lähde: Genomics Education Program [CC 2: lla.0 (https: // creativecommons.Org/lisenssit/by/2.0)] Wikimedia Commonsin kautta) 5-fosfaatti-riboosi voidaan myöhemmin pelkistää 5-fosfaatti-deoksiriboosiksi, jota voidaan käyttää suoraan energian nukleotidisynteesiin.
Riboosin ja deoksiriboosin saaminen pienempien sokerien kondensaatiosta on osoitettu bakteeriuutteissa, joissa deoksihioosin muodostuminen on osoitettu glyseraldehydifosfaatin ja asetaldehydin läsnä ollessa.
Voi palvella sinua: Henryn lakiSamankaltaisia todisteita on saatu tutkimuksissa, joissa käytetään eläinkudoksia, mutta inkuboidaan fruktoosi-1-6-bifosfaatti ja asetaldehydi joodetikkahapon läsnä ollessa.
Ribonukleotidien muuntaminen deksyyribonukleotideiksi
Vaikka nukleotidi -biosynteesireiteille tarkoitetut pienet hiiliatomien fraktiot on suunnattu deoksynukleotidien biosynteesiin (DNA -nukleotidit, joilla on sokeri deoksiriboosiin), suurin osa niistä on pääasiassa suuntautumassa kohti ribonukleotidien muodostumista.
Näin ollen deoksiriboosi syntetisoidaan pääasiassa sen ruoste -riboosisokerista).
Siten deksinukleotidien synteesin ensimmäinen vaihe ribonukleotideista koostuu deoksihioosin muodostumisesta riboosista, joka säveltää näitä nukleotideja.
Tätä varten riboosi vähenee, toisin sanoen OH -ryhmä poistetaan riboosin hiili 2: sta ja vaihdetaan hydridi -ionille (vetyatomi), säilyttäen saman konfiguraation.
Viitteet
- Bernstein, minä. -Lla., & Makea, D. (1958). Deoksiriboosin biosynteesi ehjässä Escherichia colissa. Biologisen kemian lehti, 233(5), 1194-1198.
- Griffiths, a. J -., Wessler, S. R -., Lewontin, R. C., Gelbart, W. M., Suzuki, D. T., & Miller, J. H. (2005). Johdatus geenianalyysiin. Macmillan.
- Mathews, c. K -k -., Van Holde, K. JA., & Ahern, k. G. (2000). Biokemia. 2000. San Francisco: Benjamincummings.
- McGeown, M. G., & Malpress, f. H. (1952). Deoksiriboosin synteesi eläinkudoksissa. Luonto, 170(4327), 575-576.
- Watson, J. D -d., & Crick, f. (1953). Rakenne deoksiriboosin nukleiinihapolle.
- « Leksikaaliset variantit tyypit ja esimerkit
- Bioelementtien luokittelu (ensisijainen ja toissijainen) »

