Diastreomerit
- 2543
- 420
- Ronald Reilly
Selitämme, mitkä ovat diastomeerit, kuinka niiden ominaisuudet, nimikkeistö ja useita esimerkkejä tunnustetaan,
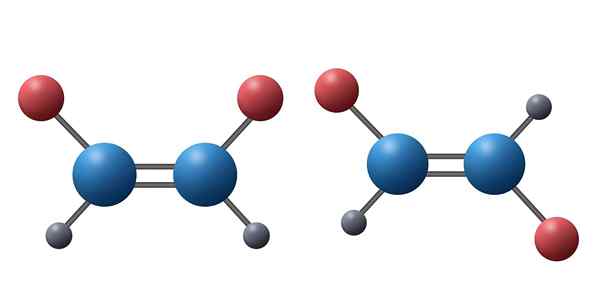
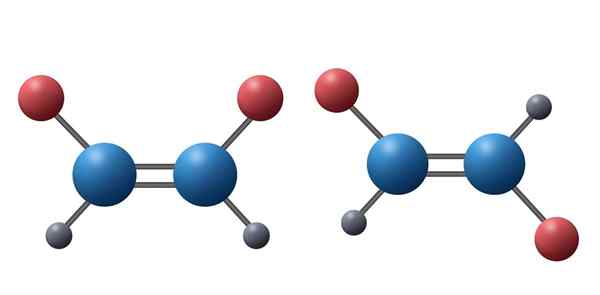 Nämä kaksi alkeenia ovat esimerkki diastereomeereistä. Tässä voidaan nähdä, että molempien molekyylien kaikki atomit yhdistyvät samassa sekvenssissä ja samantyyppisten linkkien kautta. Ensimmäisessä yhdisteessä punaiset atomit ovat kuitenkin samalla puolella, kun taas toisessa yhdisteessä ne osoittavat vastakkaisiin suuntiin. On selvää, että mikään niistä ei ole toisen peilikuva
Nämä kaksi alkeenia ovat esimerkki diastereomeereistä. Tässä voidaan nähdä, että molempien molekyylien kaikki atomit yhdistyvät samassa sekvenssissä ja samantyyppisten linkkien kautta. Ensimmäisessä yhdisteessä punaiset atomit ovat kuitenkin samalla puolella, kun taas toisessa yhdisteessä ne osoittavat vastakkaisiin suuntiin. On selvää, että mikään niistä ei ole toisen peilikuva Mitkä ovat diamaperomeerit?
Se Diastreomerit, Niitä kutsutaan myös dianedereoisomeereiksi, ne määritellään stereoisomeereiksi, jotka eivät ole peilikuvia keskenään. Ne ovat tietyntyyppisiä isomeerejä, mikä tarkoittaa, että ne ovat erilaisia yhdisteitä, joilla on sama molekyyl kaava.
Isomeerejä on erityyppisiä, joista stereoisomeerit. Nämä ovat niitä, joissa kaikki atomit yhdistyvät samassa järjestyksessä ja samantyyppisissä linkeissä, mutta niillä on erilaiset avaruudet (stereo tarkoittaa tilaa). Stereoisomeerien sisällä löydämme diamaperomeerit, joille on ominaista, että ne eivät ole peilikuvia keskenään.
Toisin sanoen, diamaperomeerit ovat Stereoisomeerit että Ne eivät ole enantiomeerejä keskenään.
Diastomeeria on erityyppisiä.
Kuinka tunnistat Diaperhereomers?
Diastomeerien tunnistamiseksi määrittelemme ensin, ovatko ne cis-trans-isomeerejä vai ovatko he E-Z-isomeerejä. Jos näin tapahtuu, he ovat diastereomerejä. Muuten seuraavia sääntöjä noudatetaan:
- Niiden on oltava stereoisomeerejä, ts. Niiden on erotettava vain atomiensa alueellisessa suunnassa.
- Heillä on oltava kaksi tai useampia kiraalikeskuksia.
- Heillä on oltava sama kokoonpano ainakin yhdessä heidän kiraalikeskuksestaan.
- Heillä on oltava päinvastainen kokoonpano ainakin yhdessä heidän kiraralikeskuksestaan.
Kaikki isomeerit, jotka täyttävät nämä ominaisuudet, ovat pari diastereomeeriä.
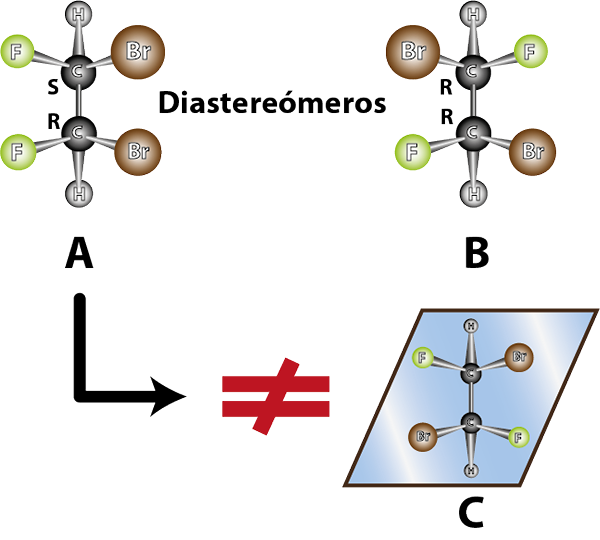 Yhdisteet A ja B ovat diasmeeria. Lisäksi A ja B eivät ole peilikuvia
Yhdisteet A ja B ovat diasmeeria. Lisäksi A ja B eivät ole peilikuvia Diastreomeerien ominaisuudet
Sen fysikaaliset ja kemialliset ominaisuudet ovat erilaisia
Toisin kuin enantiomeerit, joilla on sama kiehumispiste, fuusio jne., Diastreomeerit ovat melko erilaisia yhdisteitä, ja niillä voi olla hyvin erilaisia fysikaalisia ja kemiallisia ominaisuuksia.
Heillä on melkein aina eroja napaisuudessaan, höyrynpaineessaan, kiehumis- ja fuusiopisteissä ja jopa liukoisuudessaan eri liuottimissa.
Erot niiden fysikaalisissa ja kemiallisissa ominaisuuksissa tekevät siitä mahdollisen.
He voivat tai ehkä
Samasta yhdisteestä voi olla useita päiviä, ja jotkut niistä voivat olla kiraalisia, kun taas toiset eivät, riippuen siitä, onko molekyylillä jonkin tyyppistä symmetriaa vai ei.
Tosiasia, että kiraalikeskukset eivät varmista, että molekyyli on quiraalinen. Jotkut yhdisteet, joissa on kiraalikeskuksia. Näissä tapauksissa niitä kutsutaan Mesoyhdiste.
-
Esimerkki:
Seuraava kuva näyttää kahta hampaanhappoa. Diastreomero A ei ole kiraalinen, koska se on symmetrinen molekyyli (puolet ylhäältä on alla olevien heijastus). Kuitenkin diamaperomeeri B, jos se on kiraalista.
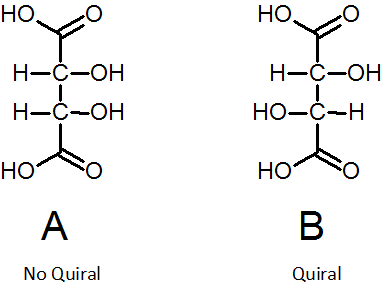
Edellisessä kuvassa isomeeri A on esimerkki mesoyhdisteestä.
Ne voivat olla cis-trans ja e-z-isomereita
CIS- ja trans-isomeerit, samoin kuin alkeenin e-z-isomeerit tai korvattu sykli, ovat stereoisomeerejä, jotka eivät ole peilikuvia keskenään, joten ne ovat myös diastereomeerejä.
Voi palvella sinua: Hekeksokinaasi: rakenteet, toiminnot, muodotOptinen toiminta
Ne diastomeerit, joissa on kiraralikeskuksia, mutta jotka eivät ole mesoyhdisteitä, ovat kiraalisia yhdisteitä, ja siksi ne ovat optisesti aktiivisia. Tämä tarkoittaa, että he kykenevät kiertämään polarisoidun valon tasoa.
Diaperhereomers -nimikkeistö
Niiden diamaperomeerien nimikkeistö, jossa on kiraalisia keskuksia (ne, jotka eivät ole cis-trans tai e-z), perustuu yhdisteen IUPAC-systemaattiseen nimeen, jota edeltää kunkin kiraalikeskuksen absoluuttinen kokoonpano ketju.
Yhden tai toisen diastereomeerin tunnistamiseksi on useita menetelmiä, mutta eniten käytettyjä on Cahn-ingold-prelog (CIP) -järjestelmä (CIP). Tämä koostuu seuraavista vaiheista:
- Hierarkiataso on osoitettu neljään ryhmään, jotka on kiinnitetty jokaiseen kiraalikeskukseen. Ryhmien prioriteetti on osoitettu atomin atomin lukumäärän mukaan, joka on suoraan kytketty Quiral Centeriin. Jos atomia on kaksi yhtä suurta, ensimmäiseen kytkettyjen atomien atominumeroita lisätään atomilukujen lisäämiseksi.
- Suunta, johon kolme prioriteettiryhmää kuljetetaan, kun alhaisimmat prioriteettipisteet takaisin määritetään.
- Jos reitin suunta on kellon käsien suuntaan, määritetään kokoonpano r, muuten S -kokoonpano on määritetty.
Esimerkki
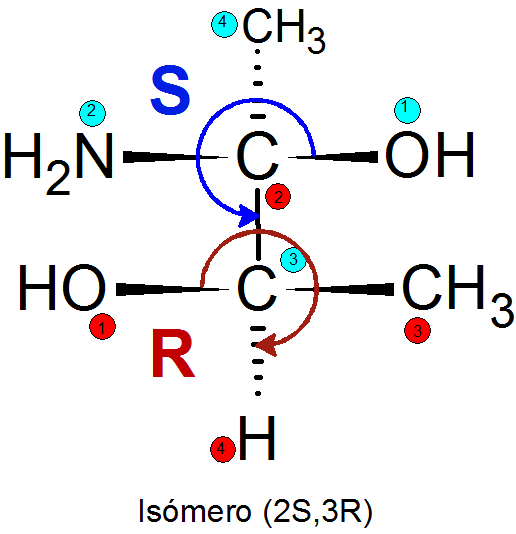
Esimerkkejä yleisistä diamaperomeereistä
Esimerkkejä hiilihydraattipäivistä
Diastreomeerit ovat luonteeltaan hyvin yleisiä, etenkin biologisen tärkeän yhdisteessä. Seuraavaksi kolmen tärkeän sokeriryhmän eri päivät esitetään esimerkinä:
-
La Ribosan diastreomerit
Ribosa on yksi luonteeltaan tärkeimmistä hiilihydraateista, koska se on osa sekä DNA: ta että RNA: ta, jotka muodostavat geneettisen materiaalin. Tässä hiilihydraatissa on kolme kiraalikeskusta, jotka aiheuttavat kahdeksan erilaista isomeeriä. Seuraavaksi esitetään tämän sokerin 4 tärkeintä diasaria:
Voi palvella sinua: ylikyllästetyt ratkaisut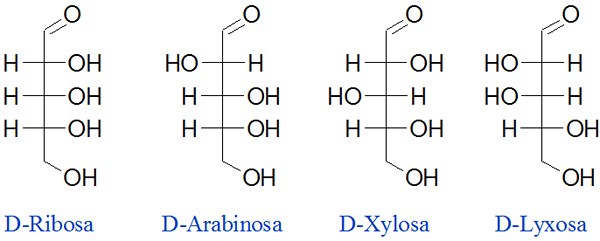
Fruktoosidiastereomerit
Kuten nimestä voi päätellä, fruktoosi on hedelmistä löydetty sokeri, ja siinä on kolme kiraalikeskusta, jotka aiheuttavat seuraavia päiviä
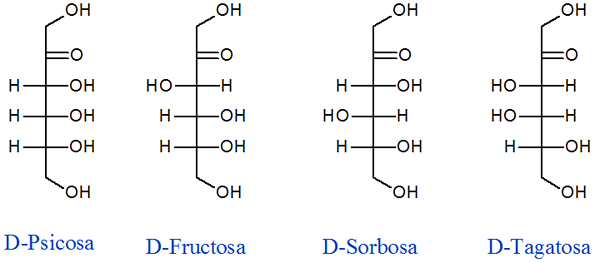
Glukoosidiastereomeerit
Glukoosi on yleisin hiilihydraatti, joka on olemassa ja on yksi yleisimmistä biologisista molekyyleistä ympäri maata. Isomeerejä on yhteensä 16, joista vain 8 on useimmissa elävissä olennoissa. Muut 8 ovat läsnä vain joissakin soluissa. Alla on 8 yleisintä diastomeeria:
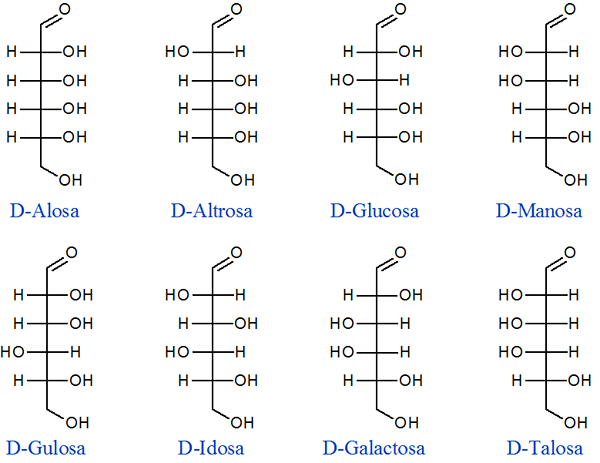
Voimme huomata, että vertaamalla mitä tahansa diastomeeria, ne eroavat ainakin yhden kiraalisen hiilen kokoonpanossa ja jakavat ainakin yhden kiraalisen hiilen kokoonpanon.
Esimerkki cis-trans-diastereomeereistä
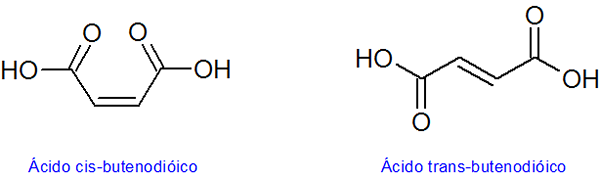
Esimerkki E-Z-diastereomeereistä
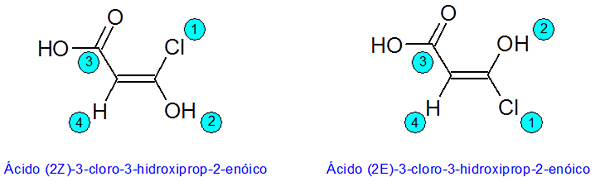
Tässä esimerkissä esitetyt numerot vastaavat CIP -järjestelmän sääntöjä noudattavien substituenttien prioriteettia.
Viitteet
- Carey f. (2008). Orgaaninen kemia. (6. ed.-A. MC Graw Hill.
- Diastereomeeri. (2021). Merriam-Webster.Com Dictionary, Merriam-Webster, Merriam-Webster.com
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. (10. ed.-A. Wiley Plus.
- Monosakkaridi. (16. helmikuuta 2021). Wikipediassa.org.
- Nelson, D. Lens., & Cox, M. M. (2017). Lehninger -biokemian periaatteet (7. ed.-A. W -.H. Freeman.

