Kemiallinen jaettavuus
- 4980
- 556
- Sheldon Kuhn
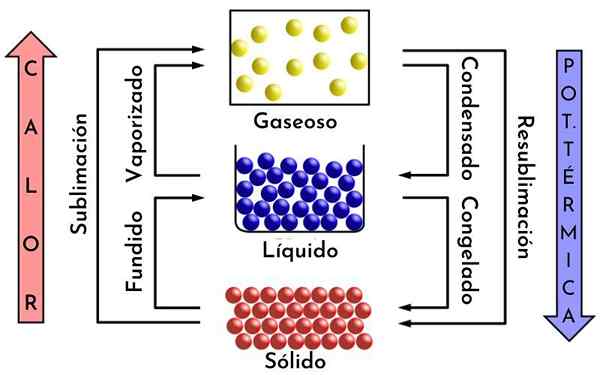
 Aineen muutos, esimerkki jaottavuudesta kemiaan. Lähde: Mikerun, CC BY-SA 4.0, Wikimedia Commons
Aineen muutos, esimerkki jaottavuudesta kemiaan. Lähde: Mikerun, CC BY-SA 4.0, Wikimedia Commons Mikä on kemiallinen jako?
Voimme määritellä Kemiallinen jaettavuus aineen ominaisuutena, jonka avulla voit erottua pienemmissä osissa. Ymmärtääksemme käsitteen voimme antaa esimerkin.
Jos jääkuutio sulaa, siitä tulee vettä, ja kun se altistetaan lämmölle, se muuttuu höyryksi. Tämä höyry voidaan jakaa puolestaan molekyyleiksi ja nämä atomeiksi.
Kemiallinen jaettavuus on silloin mahdollisuus jakaa yhä pienempiin osiin.
Alkuperä ja käsite kemiallisesta jaettavuudesta
Pitkän ajan keskusteltiin, jos asia koostui hiukkasista (mitä tunnemme tänään atomeiksi), yleinen ajatus oli, että asia oli jatkuvuus, joka voidaan jakaa.
Tämä yleinen konsepti teki pilkkaamisen loistaville tutkijoille, kuten James Clerk Maxwell (Maxwellin yhtälöistä) ja Ludwig Boltzman (Boltzmanin jakelusta) jotain, joka veti ensimmäisen hulluuteen ja toisen itsemurhaan.
5. vuosisadalla.C., Kreikkalainen filosofi Leucipo ja hänen demokruolinsa opetuslapsensa käyttivät sanan atomia nimetäkseen pienimman yksittäisen aineen ja ehdottivat, että maailma ei koostu muuta kuin atomien liikkumisesta.
Tämä varhainen atomiteoria poikkesi myöhemmistä versioista, koska se sisälsi idean ihmisen sielusta, joka koostui kehon kautta jakautuneesta atomin tyypistä.
Atomiteoria laski keskiajalla, mutta elpyi tieteellisen vallankumouksen alussa 1700 -luvulla.
Esimerkiksi Isaac Newton uskoi, että aine koostui "kiinteistä, massiivisista, kovista, läpäisemättömistä ja liikkuvista hiukkasista".
Voi palvella sinua: Molekyylinen kaava: Kuinka saada se ulos, esimerkkejä ja harjoituksiaJako voidaan antaa erilaisilla menetelmillä: Yleisin on jaettavuus fyysisillä menetelmillä, kuten omenan leikkaaminen veitsellä.
Jaottavuus voidaan kuitenkin antaa myös kemiallisilla menetelmillä, joissa aine erotettaisiin molekyyleiksi tai atomeiksi.
Kemialliset jakautumisesimerkit
1. Liuottaa suolaa
Kun suola liuentuu, esimerkiksi natriumkloridi, vedessä, tapahtuu liuottimen ilmiö, jossa suolan ioniset yhteydet rikkoutuvat:
NaCl → NA+ + Cl-
Liuottamalla vain suolajyvä veteen, se erotetaan miljardeiksi natrium- ja kloridi -ioneiksi liuoksessa.
2. Metallien hapettuminen happamassa väliaineessa
Kaikki metallit, esimerkiksi magnesium tai sinkki, reagoivat happojen, kuten laimennettujen suolahappojen, kanssa vetykuplien ja väritön metallikloridin liuoksen antamiseksi.
Mg + hcl → mg2+ +Cl- + H2
Oksida metallihapoksi erottamalla metallisidokset ionien saamiseksi liuoksessa.
3. Esterien hydrolyysi
Hydrolyysi on kemiallisen sidoksen repeämä veden avulla. Esimerkki hydrolyysistä on estereiden hydrolyysi, jossa ne on jaettu kahteen molekyyliin, alkoholiin ja karboksyylihappoon.
4. Eliminointireaktiot
Eliminaatioreaktio tekee tarkalleen mitä sanotaan: se eliminoi molekyylin atomit. Tämä tehdään hiilihiilisen kaksoissidoksen luomiseksi. Tämä voidaan tehdä emäksellä tai hapolla.
Se voi tapahtua yhdessä koordinoidussa vaiheessa (protonin abstraktio Ca: ssa, joka tapahtuu samanaikaisesti kuin C-X-linkin jako) tai kahdessa vaiheessa (C-X-linkin jako tapahtuu ensin muodostettavaksi Keskitason karbokaatio, joka sitten "sammuttaa" protonin abstraktiolla alfa-hiilissä).
Voi palvella sinua: Darmstadtio: löytö, rakenne, ominaisuudet, käyttötarkoitukset5. Aldolaasin entsymaattinen reaktio
Glykolyysin preparatiivisessa vaiheessa glukoosimolekyyli jaetaan kahteen glyseraldehydimolekyyliin 3-fosfaattiin (G3P) käyttämällä 2 ATP: tä.
Tämän viillosta vastaava entsyymi on aldolaasi, joka kääntää käänteisen kondensaation kautta 1,6-bifosfaattiruktoosimolekyylin G3P.
6. Biomolekyylien hajoaminen
Ei vain glykolyysi, vaan kaikki biomolekyylien hajoaminen katabolismin reaktioissa ovat esimerkkejä kemiallisesta jaettavuudesta.
Tämä johtuu tosiasiasta, että suuret molekyylit, kuten hiilihydraatit, rasvahapot ja proteiinit, tuottavat pienempiä molekyylejä, kuten asetyyli COA, jotka tulevat Krebs -sykliin tuottaakseen energiaa ATP: n muodossa.
7. Palamisreaktiot
Tämä on toinen esimerkki kemiallisesta jaettavuudesta, koska kompleksiset molekyylit, kuten propaanit tai butaani, reagoivat hapen kanssa tuottamaan co₂ ja vettä:
C3H8 + Viides2 → 3Co2 + 4H2JOMPIKUMPI
Biomolekyylien hajoaminen voitaisiin sanoa, että se on palamisreaktio, koska lopputuotteet ovat yhteistyötä ja vettä, niitä tapahtuu kuitenkin monissa vaiheissa eri välittäjien kanssa.
8. Veren sentrifugointi
Eri verikomponenttien erottaminen on esimerkki jaettavuudesta. Huolimatta fyysisestä prosessista, esimerkki on mielenkiintoinen, koska tiheyseron komponentit erotetaan sentrifugoimalla.
Tiheimmät komponentit, seerumi punasolujen kanssa, pysyy sentrifugiputken pohjassa, kun taas vähemmän tiheä plasma pysyy yläosassa.
Voi palvella sinua: neutraali atomi9. Bikarbonaattipuskuri
Natriumbikarbonaatti, HCO3-, Se on tärkein tapa kuljettaa CO₂: n aineenvaihdunnan hajoamisreaktioiden kehon tuotteessa.
Tämä yhdiste reagoi keskipitkän protonin kanssa hiilihapon tuottamiseksi, joka jaetaan myöhemmin co₂: een ja veteen:
HCO3- + H+ D h2Yhteistyö3 D co₂ + h₂o
Koska reaktiot ovat palautuvia, tämä on tapa, jolla keholla on hengityksen kautta fysiologisen pH: n hallitsemiseksi alkaloosi- tai asidesiprosessien välttämiseksi.
10. Ydinatomi tai fissio -osasto
Siinä tapauksessa, että massiivinen ydin (kuten uraani-235) on rikki (halkeamat) johtaa nettoenergian suorituskykyyn. Tämä johtuu siitä, että fragmenttien massojen summa on pienempi kuin uraanin ytimen massa.
Siinä tapauksessa, että fragmenttien massa on yhtä suuri tai suurempi kuin raudan linkkienergiakäyrän huipulla, ydinhiukkaset ovat läheisemmin yhteydessä kuin uraanin ytimessä ja että massan väheneminen tapahtuu energian muodossa mukaan Einsteinin yhtälöön.
Raudan kevyempiä elementtejä fuusio tuottaa energiaa. Tämä käsite johti atomipommin ja ydinenergian luomiseen.
Viitteet
- Happojen reaktiot. BBC toipunut.yhteistyö.Yhdistynyt kuningaskunta.
- Foist, l. (S.F.-A. Eliminointireaktiot orgaanisessa kemiassa. Tutkimus toipunut.com.
- Ydinsuunta (S.F.-A. Toipunut hyperfysiikasta.

