Säätiöelektroforeesi, tekniikka, mihin se on, esimerkkejä

- 5098
- 1226
- Eddie Hackett
Se Elektroforeesi Se on tekniikka, jota käytetään molekyylien erottamiseen sähkökentällä. Sen on tehtävä erityisesti, kun hiukkaset on ladattu kahden pylvään, yhden positiivisen ja toisen negatiivisen väliseen sähkövirran vaikutukseen.
Elektroforeesi on tällä hetkellä yksi rutiininomaisimmista toimenpiteistä, jotka tapahtuvat kokeen kehittämisen aikana, etenkin analyyttiseen kemiaan, biokemiaan ja biologisiin ja lääketieteellisiin tieteisiin liittyvät aloilla.
 Elektroforeesi kauha. Lähde: Melodiagar/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0)
Elektroforeesi kauha. Lähde: Melodiagar/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0) Sitä käytetään proteiinin, peptidien, DNA: n, RNA: n ja muiden erottamiseen niiden kuorman, koon, tiheyden ja puhtauden mukaan.
Eri kaupalliset talot ovat suunnitelleet erilaisia muotoja, joilla on erilaiset sovellukset ja sopivat voitot tiettyihin tarkoituksiin, mutta kaikki menettelyt vaativat samat peruselementit:
- Energialähde sähkövarauksen tuottamiseksi
- Erotteluväline
- Puskuriliuos (puskuri) Pitää pH -vakio
[TOC]
Perusta
Elektroforeesi ei ole muuta kuin hiukkasten tai ladattujen molekyylien migraatio (erotus) (luonnollisesti tai keinotekoisesti) väliaineessa tai tuki sähkökentän vaikutuksesta.
Tekniikka perustuu yhteen sähkömagneettisuuden tärkeimmistä fysikaalisista yhtälöistä, joiden mukaan voima on yhtä suuri kuin sähkökenttä, joka kerrottuna siinä vaiheessa kohdistetulla sähkökentällä (F (voima) = Q (sähkövaraus) x E (sähkökenttä -A.
Tämän yhtälön mukaan kaksi hiukkasia, joilla on sama massa, mutta erilainen kuorma, siirtyvät eri nopeuksiin samassa sähkökentässä. Lisäksi näiden hiukkasten liikkumisen nopeus riippuu niiden kuorman ja massan välisestä suhteesta.
Tutkijat ovat hyödyntäneet näitä ominaisuuksia ja lastin/massasuhteita komponenttien erottamiseksi pienimmistä osista ja erottamaan seoksen erilaisia molekyylejä muun muassa, muun muassa.
On tärkeää muistaa, että biologisilla molekyyleillä, kuten aminohapot, peptidit, proteiinit, joillakin hiilihydraateilla, nukleotideina ja nukleiinihapoissa.
Tekniikka
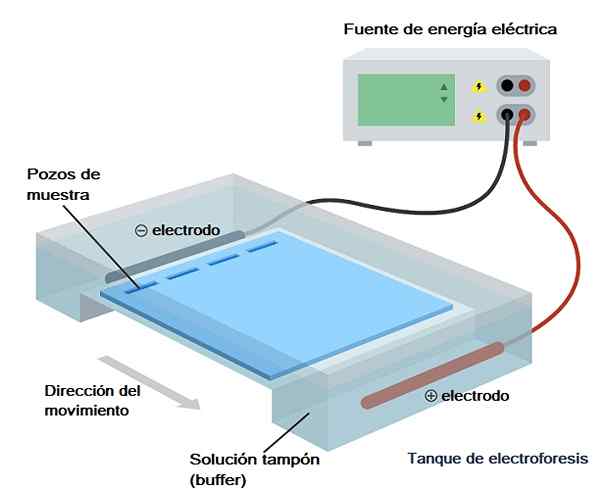
Vaikka elektroforeesityyppejä on erityyppisiä, geelielektroforeesi on eniten käytetty biokemiallisessa analyysissä, molekyylibiologiassa ja bioteknologiassa, joten se on mitä puhumme lyhyesti teknisesti.
Kuten nimestä voi päätellä, geelielektroforeesi merkitsee kiinteän muotoisen kiinteän tuen väliaineen käyttöä joko proteiinin tai nukleiinihappojen (DNA ja/tai RNA) seosten analysointiin/erottamiseen sähkökentän vaikutuksesta.
Järjestelmä tai laite, jota käytetään elektroforeettisen ”ajon” suorittamiseen.
- Esimerkki nukleiinihappoelektroforeesitekniikasta
Nukleiinihapot erotetaan yleensä käyttämällä agaroosigeelejä (galaktoosipolysakkaridia), jotka valmistetaan riittävällä puskuriliuoksella (Tris/asetaatti/EDTA tai Tris/Borato/EDTA) ja joiden pitoisuus määrittää erikokoisten fragmenttien "resoluution".
Voi palvella sinua: Maan ruokaketju: Linkit ja esimerkkinäytteen valmistus
Ensimmäinen vaihe ennen elektroforeettisen ajon suorittamista agaroosigeelissä on näytteen hankkiminen. Tämä riippuu kokeellisesta päästä ja näytteet voivat olla entsymaattisen pilkkomisen tuote polymeraasiketjureaktiosta (PCR), nukleiinihappojen puhdistamisesta jne.
 Näytteen sekoitus kuormitusharrastajan kanssa.Org/lisenssit/by/4.0) Wikimedia Commonsin kautta)
Näytteen sekoitus kuormitusharrastajan kanssa.Org/lisenssit/by/4.0) Wikimedia Commonsin kautta) Saatuaan tämä sekoitetaan värillisen liuoksen (kuormitusliuos) kanssa, joka mahdollistaa näytteen nopean laskeutumisen kaivoon, koska siinä on glyseroli ja väriaine, joka sallii ajon visuaalisesti.
Geelivalmiste
Tämä vaihe koostuu geeliytymisen substraatin (agaroosin) välttämättömän määrän sekoittamisesta puskuriliuoksen kanssa, sulattamalla se lämmöllä ja kiinteyttämällä se tuella, joka toimii "homeina".
Geelifikaation aikana jotkut "kammat" otetaan käyttöön geelissä, joka on sijoitettu "muottiin" rajaamaan "kaivot", joissa näytteet otetaan käyttöön ennen juoksua.
Kun geeli on jäähdytetty ja jähmettynyt, "kammat" poistetaan ja se johdetaan säiliöön, joka tunnetaan nimellä "ämpäri", joka on täynnä juoksevaa puskuriliuosta (Tris/asetaatti/EDTA tai Tris/Borato/Borato/EDTA).
Tämä ämpäri puolestaan sisältyy niin kutsuttuun ”elektroforeettiseen kammioon”, joka ei ole muuta kuin säiliö, jonka kautta sähkökenttä ohitetaan ja jossa on tila, jossa geeli otetaan käyttöön, ja kaksi osaa, joilla ne täytetään puskuriliuos (puskuri juosta).
Tässä kamerassa on kaksi elektrodia, yksi positiivinen ja yksi negatiivinen, joista ioniliike tuotetaan sähkökentän levityksen jälkeen (se on kytketty virtalähteeseen).
Lastausnäytteet
Kun näytteet ovat sekoittuneet vastaavan kuormitusliuoksen kanssa, ne viedään "kaivoihin", jotka on aikaisemmin valmistettu geeliin.
Koska nukleiinihapoilla on negatiivinen nettokuorma, ne siirtyvät negatiivisesta navasta positiiviseen, joten tämä on otettava huomioon, kun kamera on kytketty virtalähteeseen, varmistaen, että negatiivinen napa vastaa eniten paikan vieressä olevaa paikkaa missä näytteet ladattiin.
Corrida -aika on määritetty tiukasti riippuvuuteen kokeen vastaavasta tutkijoista. Jännite lasketaan yleensä 5 voltin suhteessa senttimetriä geelissä, joka erottaa kaksi elektrodia.
Näyttö
Kun geeli juoksee (kun näytteet ovat kulkeneet geeliä päästä toiseen), se on upotettu etidbromidin (ETBR) liuokseen, väriaineeseen, joka on väliaineen välinen väriaine ja "tuotemerkki", joten niin Ne voidaan visualisoida transilumenantissa ultraviolettivalolla.
Mikä on elektroforeesi?
Elektroforeesia on historiallisesti käytetty useisiin tarkoituksiin. Nykyään sen hyödyllisyys riippuu suurelta osin ”kysymyksestä”, jota tutkijalle kysytään ilmiön tai tiettyyn järjestelmään, samoin kuin elektroforeesityyppiin, jota hän haluaa käyttää.
Voi palvella sinua: topoisomeraasi: mitkä ovat, ominaisuudet, toiminnot, tyypitVoimme kuitenkin värvää joitain päätoimintoja, jotka tämä tekniikka on aloittaen kaikkein "harvinaisimmasta" ja päättyen suosituimmista ja enimmäkseen hyödynnetään biologisten tieteiden maailmassa. Elektroforeesi on hyödyllinen:
- Makromolekyylien monimutkaisten seosten kvantitatiivista analysointia varten ja potentiaalisen "zeta" (hiukkasen kolloidinen ominaisuus nestemäisessä väliaineessa staattisen sähkökentän vaikutuksen alaisena) laskemiseksi).
- Veriserumien analysoimiseksi diagnostisiin tarkoituksiin.
- Glukoproteiinien, lipoproteiinien ja verihemoglobiinin erottamiseksi.
- Elintarvikkeiden analysointia varten farmaseuttisia tuotteita ja ympäristöä koskevia aineita.
Elektroforeesi agaroosigeelissä
- DNA -fragmenttien erottamiseksi ruuansulatuksen jälkeen restriktioentsyymeillä.
- Nukleiinihappomolekyylien erottamiseksi ennen siirtoa kalvoihin seuraavia analyysejä varten.
- PCR.
- Molekyylien koon arvioimiseksi DNA: n tai RNA: n seoksessa.
- Puhdistettujen nukleiinihappojen määrän ja/tai laadun arviointia.
Elektroforeesi polyakryyliamidigeelissä denaturalisoinnissa tai alkuperäisissä olosuhteissa
- Proteiinin koon määrittämiseksi.
- Proteiinien tunnistamiseksi.
- Näytteen puhtauden määrittäminen useiden puhdistusvaiheiden jälkeen.
- Molekyylin disulfidilinkkien läsnäolon tunnistamiseksi.
- Proteiinien välisen vuorovaikutuksen määrittämiseksi.
- Proteiinin isoelektrisen pisteen määrittäminen.
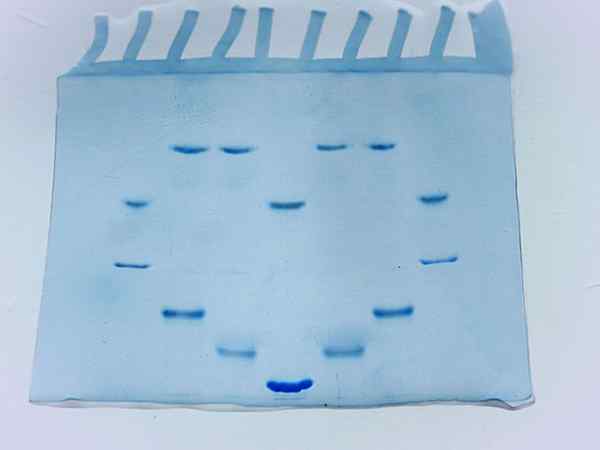 Valokuva akryyliamidigeelistä useiden proteiininäytteiden ajon jälkeen (lähde: Larionova.Marina/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0) Wikimedia Commonsin kautta)
Valokuva akryyliamidigeelistä useiden proteiininäytteiden ajon jälkeen (lähde: Larionova.Marina/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0) Wikimedia Commonsin kautta) Tekijät, jotka vaikuttavat elektroforeesiin
Hiukkasen kulkeutuminen sähkökentällä riippuu erilaisista tekijöistä, joista on:
- Sähkömaksusi
- Sen molekyylikoko
- Sen hydrofobisuus ja muoto
- Käytetyn sähkökentän suuruus
- Käytetyn puskuriliuoksen järjestelmän lämpötila ja ioninen voima
- Sen ympäristön luonne, jossa se sijaitsee
Suhteessa
Sähkökentän alaisia hiukkasiin (näyte) liittyviä parametreja tärkeimmät tekijät, jotka vaikuttavat tähän prosessiin, liittyvät niiden kuormaan, koon ja muotoon.
Mitä suurempi hiukkasen nettokuorma, sitä suurempi sen kulkeutumisnopeus ja tämä suuruus riippuu pH: sta. Suhde koon kanssa on kuitenkin käänteisesti verrannollinen, mikä tarkoittaa, että mitä "suurempi" molekyyli, sitä hitaammin siirtyy.
Se voi palvella sinua: Lia Agar (Iron Lysine): Mikä on, perusta, valmistelu, käyttöSuhteessa sähkökenttään
Toistaiseksi olemme puhuneet sähkökentän tärkeydestä hiukkasen liikkeen saavuttamiseksi elektroforeesilla, mutta emme ole määrittäneet, mikä se on: sähkövoima kuormitusyksikköä kohti tai yksinkertaisemmassa määrin tilaa, missä siellä on sähkövoima.
Siirtoon vaikuttavaa sähkökenttää koskevat parametrit ovat jännite, virta ja vastus.
Jännite vaikuttaa molekyylien ”lentoaika”, jotka on erotettu sähkökentän levittämisen jälkeen. Mitä korkeampi se on, sitä nopeammin nämä liikkuvat.
Virta (jatkuvat ja tasaiset elektronit, jotka ”työntävät” jänniterähde) suoritetaan elektroforeettisen järjestelmän elektrodien välillä puskuriliuoksessa olevien ionien ansiosta. Liittyy suoraan jännitteeseen.
Suhteessa puskuriliuokseen
Puskuriliuoksen koostumus, ioninen voima ja pH ovat tärkeimmät parametrit, jotka vaikuttavat elektroforeettiseen "ajon", koska ne vaikuttavat suoraan joihinkin näytteiden ominaisuuksiin, erityisesti sähkövaraukseen.
Koska? Puskuriliuos stabiloi tukiväliaineen pH: n, jossa elektroforeesi tapahtuu. Sen koostumus voi vaikuttaa myös kulkevien hiukkasten siirtymiseen ja myös ioniseen pitoisuuteen, koska se liittyy suoraan virtaan.
Suhteessa tukiväliaineeseen
Elektroforeesin eri tyypit ja muodot esittävät myös erilaisia väliaineita, joilla muuttoliike tapahtuu ja missä se voidaan myöhemmin "rekisteröityä".
Elektroforeesille altistuneiden molekyylien muuttoliike riippuu tukiväliaineen tyypistä, joka yleensä tulisi olla inertti.
Sen imeytymisominaisuudet, elektroendo-osmoosi ovat tärkeitä (nesteen liikkumiskapasiteetti kalvon kautta sähkökentän vaikutuksesta) ja sen molekyyliseulakapasiteetti.
Esimerkkejä elektroforeesien käytöstä
Klassisia esimerkkejä biologiassa ja biotekniikassa käytetyistä elektroforeettisista tekniikoista ovat:
- Elektroforeesi agaroosigeelissä (englanti Elektroforeesigeeli-A
- Elektroforeesi akryyliamidigeelissä denaturalisointiolosuhteissa (SDS-PAGE, englanti Natriumdodekyylisulfaatti polyakryyliamidigeelielektroforeesi-A
- Elektroforeesi akryyliamidigeelissä alkuperäisissä olosuhteissa (BN-sivu, englanti Sininen alkuperäispolyakryyliamidigeelielektroforeesi-A
- Elektroforeesi kahdessa ulottuvuudessa (2D-sivu, englannista Kaksiulotteinen polyakryyliamidigeelielektroforeesi-A
- Kapillaarielektroforeesi (englannista Elektroforeesi kapillaari-A
- Eroltrienfoque (englanti Isolektrofokus-A
- Pulssikenttäelektroforeesi (englanti Pulssikenttäelektroforeesi-A
Viitteet
- Beck, Kevin. (2020, 25. toukokuuta). Elektroforeesityypit. Tiede.com. Tiedettä haettu.com
- Esseet, Yhdistynyt kuningaskunta. (Marraskuu 2018). Elektroforeesityypit ja sovellukset. Haettu Ukessaysista.com
- Nelson, D. Lens., Lehninger, a. Lens., & Cox, M. M. (2008). Lehninger -biokemian periaatteet. Macmillan.
- Parmar, p. (Elokuu 2018). Elektroforeesi: merkitys, määritelmä ja luokittelu (kaaviolla). Biotekniikka. Bioteknologiasta haettu.com
- Perrett, D. (2010). 200 vuotta elektroforeesia. Kromato. Tänään, 4-7.
- Righetti, P. G. (2005). Elektroforeesi: Pennien marssi, Dimesin marssi. Journal of Chromatography A, 1079 (1-2), 24-40.
- Rilbe, h. (tuhatyhdeksänsataayhdeksänkymmentäviisi). Som -muistelmat elektroforeesin historiasta. Elektroforeesi, 16 (1), 1354-1359.
- Vesterberg tai. (1993). Lyhyt historia elektroforeettisista menetelmistä. Elektroforeesi, 14 (1), 1243-1249.
- Vinayagam, m. (Ei päivämäärää). Elektroforeesiin vaikuttavat tekijät. Akatemia.Edu. Haettu yliopistosta.Edu
- « Kemiallisen tasapainon selitys, tekijät, tyypit, esimerkit
- Toltec -kulttuurin alkuperää, sijainti, ominaisuudet, organisaatio »

