Elementit, yhdisteet ja seokset
- 3714
- 586
- Ronald Reilly
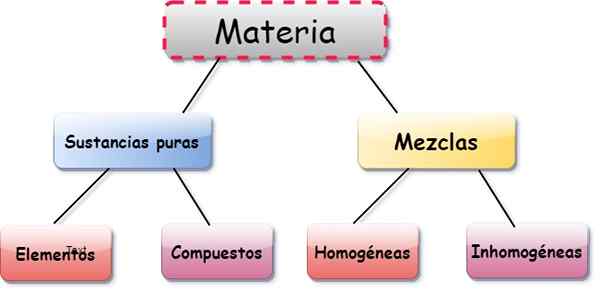
Elementit, yhdisteet ja seokset ovat kolme aineen esitysmuotoa. Se kohteet Ne ovat aineita, jotka muodostuvat yhdellä atomin luokalla, yhdisteet Ne ovat yhdistelmiä kahden tai useamman elementin välillä ja seokset Ne johtuvat useiden elementtien ja aineiden koostumuksesta.
Seosten komponentit erotetaan fysikaalisilla keinoilla. Yhdisteen elementtien erottamiseksi on suoritettava puolestaan kemialliset toimenpiteet.
Niitä ei voida erottaa pieniksi komponenteiksi tavallisilla menetelmillä, mutta on tapoja halkeaa atomeja. Itse asiassa fissio on tapa poimia niistä energiaa.
Atomit, jotka muodostavat tietyn yhdisteen, tekevät niin aina kiinteissä mittasuhteissa. Puolestaan seoksessa sen komponenttien osuudet voivat vaihdella. Siksi elementtejä ja yhdisteitä pidetään puhtaina aineina, joiden koostumus on vakio ja hyvin määritelty.
Esimerkiksi pöytäsuola tai natriumkloridi on yhdiste, johon kloori- ja natriumiatomit osallistuvat, suhteessa yksi kerrallaan. Samaan aikaan maito on sekoitus muuttuvaa koostumusta, jossa kukin komponentti ylläpitää identiteettiään.
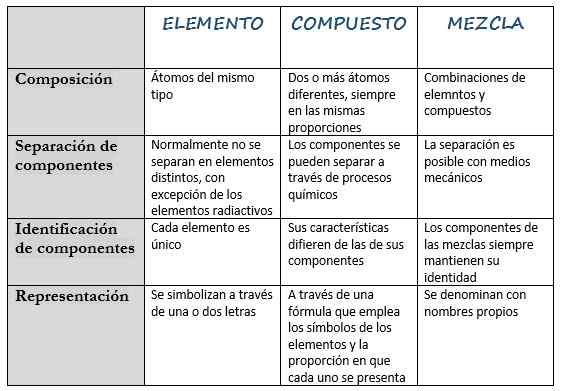
Seuraava taulukko kerää sen pääominaisuudet:
Elementti | Yhdiste | Sekoittaa | |
Määritelmä | Ainetta, jota ei voida hajottaa muissa yksinkertaisemmissa aineissa. | Aine, joka muodostuu kahdesta tai useammasta eri elementille. | Aine, joka on valmistettu sekoittaessasi muita aineita. |
Sävellys | Samantyyppiset atomit. | Kaksi tai useampaa erilaista atomia, aina samoissa mittasuhteissa. | Elementtien ja yhdisteiden yhdistelmät. |
Komponenttierottelu | Normaalisti ne eivät eroa eri elementteiksi, lukuun ottamatta radioaktiivisia elementtejä. | Komponentit voidaan erottaa kemiallisten prosessien avulla. | Erottaminen on mahdollista mekaanisilla keinoilla. |
Komponenttien tunnistaminen | Jokainen elementti on ainutlaatuinen. | Sen ominaisuudet eroavat sen komponenttien ominaisuuksista. | Seosten komponentit pitävät aina identiteettinsä. |
Esitys | Niitä symboloidaan yhdessä tai kahdessa kirjaimessa. | Kaavan kautta, joka käyttää elementtien symboleja ja osuutta, jossa kukin esitetään. | Sitä kutsutaan oikeilla nimillä. |
Esimerkit | Vety (h), pii (kyllä), helium (He), kulta (au), kalium (k). | Natriumkloridi (NaCl), ammoniakki (NH3), natriumhydridi (NAH), typpidioksidi (NO2). | Veri, maito, ilma, sementti. |
Kohteet
Määritelmä
Elementit ovat puhtaita, yksinkertaisia aineita, joiden koostumuksessa vain samantyyppiset atomit puuttuvat. Kunkin elementin kemiallinen käyttäytyminen on ominaista, eikä kahta yhtä suurta, vaikka elementtien ryhmien välillä on yhteisiä ominaisuuksia.
Voi palvella sinua: jodometria: säätiöt, reaktiot, yleinen menettely, käyttöYhtä elementtiä ei voida hajottaa yksinkertaisemmassa elementissä, paitsi erityiset menettelyt, kuten pommitus.
Hajoamisprosessi tapahtuu spontaanisti joissain aineissa, kuten radiossa, tietyissä uraanin, toriumin ja muiden elementtien lajikkeissa, joita kutsutaan radioaktiiviksi.
Sävellys
Elementit muodostuvat identtisillä atomilla. Nämä puolestaan koostuvat kolmen tyyppisistä hiukkasista: elektroneista, protoneista ja neutroneista. Elektronit ja protonit ovat vastaavasti sähkö-, negatiivinen ja positiivinen massa. Neutroneilla on massa, mutta ei kuormitus.
Atomi koostuu protonien ja neutronien muodostamasta atomi ytimestä, kun taas elektronit jakautuvat heidän ympärillään oleviin kiertorauhaan. Yksi elementti erotetaan toisesta niiden ydinprotonien lukumäärän perusteella.
Vaikka tämä pysyy vakiona, se on sama elementti, vaikka neutronien ja elektronien lukumäärä muuttuu, koska siinä tapauksessa isotoopit.
Komponenttien tunnistaminen
Erilaisia ja monimutkaisia tekniikoita käytetään esimerkiksi atomin elektronien "näkemiseen" on erityisiä mikroskooppeja, kuten tunnelimikroskooppi.
Erotustekniikka
Elementin atomia ei ole erotettu kemiallisilla menetelmillä, mutta sitä pommitetaan pienemmillä hiukkasilla, yleensä neutroneilla, ydinfissiossa kutsutussa prosessissa. Mutta vaikka teoriassa jokainen atomi on fyysisesti, se on helpompi tehdä atomien kanssa, joilla on raskaita ytimiä, kuten uraani-235.
Elementtityypit
Määräaikaisessa taulukossa on 118 elementtiä, jotka on tilattu atominumerolla. Näistä 92 löytyy luonnosta ja loput saadaan laboratoriosta.
Voi palvella sinua: amorfinen hiili: mikä on, tyypit, ominaisuudet, käyttötarkoituksetNe jaetaan kolmeen ryhmään:
- Metallit, joissa on vapaat elektronit, jotka tekevät niistä hyviä lämmön ja sähkön johtimia, melkein aina kiinteitä (paitsi elohopeaa) ja suuria tiheitä.
- Ei metalleja, puutteellisia ominaisuuksia, esitetään kiinteässä tai kaasumaisessa tilassa, paitsi bromia, ja niiden tiheys on alhaisempi.
- Metalloidit, elementit, joilla on väliominaisuudet metallien ja ei -metallien välillä.
Graafinen esitys
Jokainen jaksollisen taulukon elementti symboloidaan kirjaimilla. Esimerkiksi H, O, C ja Fe vastaavat vetyä, happea, hiiltä ja rautaa.
Esimerkkejä elementeistä
Mainittujen lisäksi on seuraavia elementtejä, joiden symboli on suluissa:
- Kloori (CL)
- Elohopea (HG)
- Fosfori (p)
- Jodi (i)
- Magnesium (mg)
Yhdisteet
Määritelmä
Yhdisteet ovat puhtaita aineita, joiden koostumus on kaksi tai useampia erilaisia atomeja, tietyissä mittasuhteissa molekyylien muodostamiseksi. Atomien väliset ammattiliitot suoritetaan linkillä, jotka ovat määräävä tekijä yhdisteiden ominaisuuksissa.
Päälinkit ovat:
- Ioninen
- Metalli
- Kovalenttinen
Sävellys
Yhdisteet koostuvat kahdesta tai useammasta atomien tyypistä, aina kiinteässä suhteessa.
Komponenttien tunnistaminen
Jokaisella yhdisteellä on ominaisuuksia, jotka tekevät siitä ainutlaatuisen, jotka eroavat sen ainesosien ominaisuuksista, koska ne menettävät identiteettinsä muodostamalla yhdiste. Esimerkiksi huoneenlämpötilassa vety ja happi ovat kaasuja, jotka yhdistettynä aiheuttavat vettä.
Erotustekniikka
Normaalisti yhdisteet erotetaan kemiallisilla reaktioilla, vaikka sähkömagneettinen säteily, mukaan lukien valo, kykenevät myös dissosioitumaan molekyyleihin.
Yhdisteiden tyypit
Yhdisteet on jaettu kahteen pääluokkaan:
- Epäorgaaninen
- Luomu
Ero on siinä, että orgaaniset yhdisteet perustuvat hiili -elementtiin, kun se muodostaa kovalenttisia -tyyppisiä yhteyksiä vetyyn. Hiili osallistuu samalla tavalla monissa epäorgaanisissa yhdisteissä muodostaen muita linkkejä.
Graafinen esitys
Se tehdään kemiallisen kaavan kautta, jossa sen ainesosat on määritelty, vastaavalla symbolillaan ja osuudellaan, johon he osallistuvat. Yhdisteillä on myös useita nimiä.
Esimerkkejä yhdisteistä
- Natriumkloridi tai pöytäsuola (NaCl)
- Natriumbikarbonaatti (Nahco₃)
- Ammoniakki (NH3-A
- Kalsiumkarbonaatti (Caco3-A
- Glukoosi (c₆h₁₂o₆)
Seokset
Määritelmä
Kahden tai useamman elementin ja/tai yhdistelmän yhdistelmä ilman määriteltyjä mittasuhteita, kukin ylläpitää identiteettiään, ts. Ilman ominaisuuksiaan muuttuvat, kun ne ovat osa seosta.
Sävellys
Se on muuttuva.
Komponenttien tunnistaminen
Se on yksinkertaisempaa suorittaa, koska komponentit säilyttävät identiteettinsä.
Erotustekniikka
Seoksen komponentit voidaan erottaa jollain fysikaalisella tai mekaanisella menetelmällä, kuten esimerkiksi suodattamalla tai sentrifugoinnilla.
Seostyypit
Seokset luokitellaan seuraavasti:
- Homogeeniset: komponenttipartikkelit ovat erottamattomia huolimatta siitä, että ne ovat eri aineita. Esimerkiksi hyvin liuennut sokeri vedessä.
- Heterogeeninen: seokset, joissa hiukkaset erottuvat, jopa paljaalla silmällä, kuten hiekka ja suola tai suola sekoitettuna metallitiedostoihin.
Graafinen esitys
Seoksista puuttuu määritelty kaava, mutta monilla on omat nimensä.
Esimerkkejä seoksista
- Sementti
- Ketsuppi
- Puu
- Ilma
- Maito
- Betoni
- Veri

