Metallilinkki
- 2774
- 583
- Shawn Stanton II
 Kuparin metallilinkki
Kuparin metallilinkki Mikä on metallinen linkki?
Hän Metallilinkki Se ylläpitää metallisten elementtien atomeja voimakkaasti yhtenäisesti. Se on läsnä metalleissa ja määrittelee kaikki fysikaaliset ominaisuutensa, jotka karakterisoivat niitä koviksi, muovautuviksi, muokattaviksi ja hyväksi lämmön ja sähkön johtimiksi.
Kaikista kemiallisista sidoksista metallisidos on ainoa, jossa elektronit eivät sijaitse yksinomaan atomien parin välillä, mutta ne demokalistetaan miljoonien välillä eräänlaisena liimana tai ”elektronien merellä”, jotka pitävät ne voimakkaasti yhtenäisesti tai yhtenäisiä tai yhtenäinen.
Oletetaan esimerkiksi kuparimetalli. Kuparissa atomit cuid valenssielektronit metallisidon muodostamiseksi. Tämä linkki on esitetty kationeina cu2+ (siniset ympyrät) ympäröivät elektronit (keltaiset ympyrät). Elektronit eivät ole vielä: ne liikkuvat koko kuparilasissa. Metalleja ei kuitenkaan puhu muodollisesti kationeista, vaan neutraaleista metalliatomeista.
Metallinen linkki tarkistetaan tutkimalla metallielementtien ominaisuuksia, samoin kuin niiden seosten ominaisuuksia. Nämä integroivat sarjan kirkkaita, hopeaa, sitkeitä, kovia materiaaleja, joilla on myös korkeat sulamis- ja kiehumispisteet.
Kuinka metallinen linkki on?
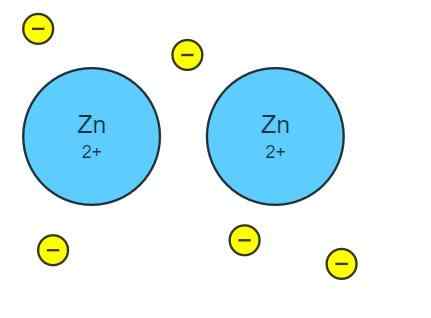
 Metallinen linkki sinkissä
Metallinen linkki sinkissä Metallinen linkki muodostuu vain metalliatomien joukon tai ryhmän välillä. Jotta elektronit siirtäisivät kaikki metallilasit, on oltava ”moottoritie”, jonka kautta he voivat matkustaa. Tämä on suunniteltu kaikkien naapuriatomien atomien kiertoratojen päällekkäisyydestä.
Tarkastellaan esimerkiksi sinkkiatomien riviä, Zn ··· Zn ··· Zn ····. Nämä atomit ovat päällekkäisiä Valencian atomisiorbitaaliensa luomiseksi molekyyliorbitaalien luomiseksi. Nämä molekyyliorbitaalit puolestaan ovat päällekkäisiä naapurimaiden Zn -atomien muiden kiertoratojen kanssa.
Jokainen sinkkiatomi osallistuu kahteen elektroniin edistämään metallisidosta. Tällä tavoin molekyyliorbitaalien päällekkäisyys tai liitto ja sinkin lahjoittamat atomit ovat lähtöisin ”moottoritiellä”, jolla elektronit siirretään koko lasin koko ikään kuin ne olisivat liimaa tai elektronien meri, peittäen tai uimalla kaikki metalliatomit.
Voi palvella sinua: enderoninen reaktioMetallilinkin ominaisuudet
Rakenteet
Metallinen linkki on peräisin kompakteista rakenteista, joissa atomit ovat tiiviisti yhtenäisiä, ilman paljon etäisyyttä, joka erottaa ne. Erityisen rakenteen tyypistä riippuen on erilaisia kiteitä, joitain tiheimpiä kuin toiset.
Metallirakenteissa molekyyleistä ei ole oikein puhetta, vaan neutraaleista atomeista (tai kationeista, muiden näkökulmien mukaan). Palattuaan kuparin esimerkkiin, tiivistetyissä kiteissä ei ole molekyylejä cu2, Cu-cu-kovalenttisen linkin kanssa.
Uudelleenjärjestely
Metallisella linkillä on uudelleenjärjestely. Tätä ei tapahdu kovalenttisten ja ionisten linkkien kanssa. Jos kovalenttinen linkki on jaettu, sitä ei muodosteta uudelleen ikään kuin mitään ei olisi tapahtunut. Myös ionisidoksen sähköiset varaukset ovat muuttumattomia, ellei kemiallinen reaktiota tapahtuva.
Harkitse esimerkiksi metalli -elohopeaa selittääksesi tämän pisteen.
Metallinen yhteys kahden vierekkäisen elohopean atomin, Hg ··· Hg: n välillä, voidaan rikkoa ja muodostaa uudelleen toisen naapurin atomin kanssa, jos lasille kohdistuu ulkoinen voima, joka muodonmuutos muodonmuutos.
Siten linkki järjestetään uudelleen, kun lasi kärsii muodonmuutosta. Tämä antaa metalleille ominaisuudet ja muokattavia materiaaleja. Muuten ne rikkoutuvat kuin lasi- tai keraamiset palat, jopa kuumat.
Lämpö- ja sähköjohto
Metallilinkin ominaisuus, jolla siirretyt elektronit saavat myös metalleille mahdollisuuden suorittaa lämpöä ja sähköä. Tämä johtuu tosiasiasta, että siirrettyjen elektronien ja liikkumisen ollessa kaikkialla atomien värähtelyt lähettävät tehokkaasti ikään kuin se olisi aalto. Nämä värähtelyt käännetään lämpöä.
Toisaalta, kun elektroneja liikuttavat, ovat tyhjiä tiloja, joiden takana muut voivat käyttää, joten sillä on elektroninen avoin työpaikka, jolla enemmän elektroneja voi "ajaa" ja siten alkuperävirta.
Voi palvella sinua: etanamidi: rakenne, ominaisuudet, käytöt, vaikutuksetPeriaatteessa käsittelemättä fyysisiä teorioita ilmiön takana, tämä on yleinen selitys metallien sähkönjohtavuudesta.
Metallinhohde
Landalisoitu ja liikkuvat elektronit voivat myös olla vuorovaikutuksessa näkyvien valofotonien kanssa ja hylätä ne. Tiheydestä ja metallipinnasta riippuen voit osoittaa erilaisia harmaita tai hopea sävyjä tai jopa irisoivia välähdyksiä. Poikkeuksellisimmat tapaukset ovat kuparia, elohopeaa ja kultaa, jotka absorboivat tiettyjen taajuuksien fotoneja.
Elektronien defoatio
Metallisen linkin ymmärtämiseksi on tarpeen ymmärtää, mitä elektronien siirtäminen ymmärretään. On mahdotonta määrittää, missä elektronit ovat. Se voidaan kuitenkin arvioida, millä avaruusalueella se todennäköisesti löytää ne. Kovalenttisessa sidoksessa A-B elektronipari on jakautunut avaruuteen, joka erottaa atomit A ja B; Sitten sanotaan, että ne sijaitsevat A: n ja B: n välillä.
AB-metallisessa linkissä ei kuitenkaan voida sanoa, että elektronit käyttäytyvät samalla tavalla kuin kovalenttisessa sidoksessa A-B. Ne eivät sijaitse kahden a: n ja b: n spesifisen atomin välissä, mutta ne ovat hämärtyneet tai suunnattu muihin kiinteiden osiin, joissa on myös tiivistettyjä atomeja, toisin sanoen A ja B.
Kun näin on, sanotaan, että metallisen sidoksen elektronit siirretään: ne kulkevat mihin tahansa suuntaan, missä A- ja B -atomeja on, kuten ensimmäisessä kuvassa kupariatomien ja niiden elektronien kanssa on esitetty.
Siksi metallisessa sidoksessa puhutaan näiden elektronien siirtämisestä, ja tämä ominaisuus on vastuussa monista metallien ominaisuuksista. Siinä tukee myös elektronien meren teoriaa.
Esimerkkejä metallilinkeistä
Jotkut metallilinkit yleiseen käyttöön päivittäisessä elämässä ovat seuraavat:
- Metallielementit
Sinkki
 Metallinen linkki sinkissä
Metallinen linkki sinkissä Sinkissä, siirtymämetallissa, sen atomeja yhdistää metallinen sidos.
Se voi palvella sinua: magnesiumnitraatti (mg (NO3) 2): rakenne, ominaisuudet, käyttötarkoituksetKulta (au)
Puhdasta kultaa, kuten tämän materiaalin seoksia kuparilla ja hopealla, käytetään tällä hetkellä erittäin hienoilla koruilla.
Kupari (Cu)
Tätä metallia käytetään laajasti sähkösovelluksissa erinomaisten sähkön ajoominaisuuksien ansiosta.
Hopea (AG)
Ominaisuuksiensa vuoksi tätä metallia käytetään laajasti sekä hienoissa koruohjelmissa että teollisuuskentällä.
Nikkeli (Ni)
Puhtaimmassa tilassa sitä käytetään yleensä kolikoiden, paristojen, valun tai monipuolisten metallikappaleiden valmistukseen.
Kadmium (CD)
Se on erittäin myrkyllinen materiaali ja sitä käytetään paristojen kehittämisessä.
Platinum (PT)
Sitä käytetään hienoissa koruissa (seokset kullalla) ja laboratoriomittauslaitteiden ja hammasimplanttien kehittämisessä.
Titanium (TI)
Tätä metallia käytetään yleisesti tekniikan haarassa sekä osteosynteettisten implanttien, teollisuussovellusten ja korujen valmistuksessa.
Lyijy (PB)
Tätä materiaalia käytetään sähköjohtimien kehittämisessä, tarkemmin sanottuna puhelin- ja televiestintäkaapeleiden ulkokannen valmistuksessa.
- Metalliyhdisteet
Yleinen teräs
Rautareaktio hiilen kanssa tuottaa yleistä terästä, materiaali, joka on paljon vastustuskykyisempi mekaanisille ponnisteluille verrattuna rautaan.
Ruostumaton teräs
Edellisen materiaalin muunnelma on mahdollista löytää yhdistämällä tavallinen teräs siirtymämetallien, kuten kromin ja nikkelin kanssa.
Pronssi
Se tapahtuu yhdistäessäsi kuparia tinalla, vastaavasti 88%: n ja 12%: n osuudessa. Sitä käytetään julkisten valuuttojen, työkalujen ja koristeiden kehittämisessä.
Elohopeaseokset
Erilaiset elohopeaseokset, joissa on muita siirtymämetalleja, kuten hopea, kupari ja sinkki, tuottavat hammaslääketieteessä käytetyt amalgaamit.
Kromi- ja platina -seos
Tämän tyyppistä seosta käytetään laajasti parranajojen valmistukseen.
Nahka
Tätä tina -seosta, antimonia, ja vismuttia käytetään yleisesti kotitalousvälineiden laatimiseen.
Messinki
Se syntyy yhdistämällä kupari sinkin kanssa, vastaavasti 67% ja 33%. Sitä käytetään laitteistoartikkeleiden valmistuksessa.

