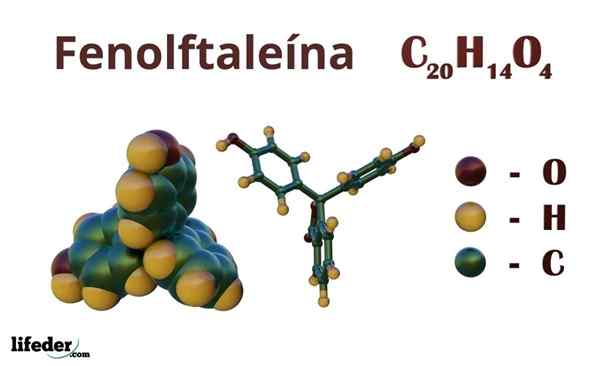
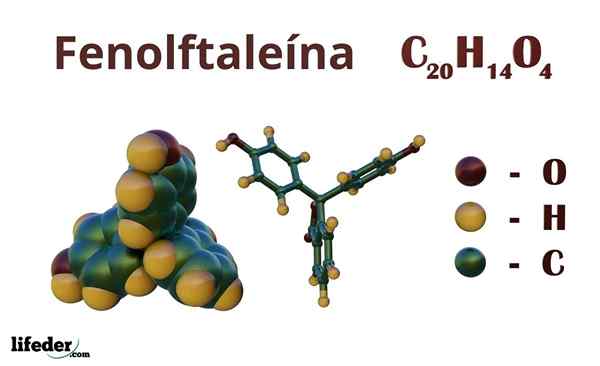
Fenolphthalein (C20H14O4)
- 4978
- 535
- Mr. Clifford Kshlerin
Mikä on fenoliftaleiini?
Se fenolftaleiini Se on orgaaninen väriaine, joka puolestaan on heikko diproottihappo, jota käytetään monissa tilavuusmäärityksissä happo-emäsindikaattorina. Eli jos se on diproottinen happo, liuoksessa voit menettää kaksi H -ionia+, Ja ollakseni indikaattori, sinulla on oltava ominaisuus olla värikäs PH -alueella, jota arvostetaan.
Perusväliaineessa (pH> 8) fenolftaleiini on vaaleanpunainen, jota voidaan vahvistaa violetiksi punaiseksi. Voit käyttää happo-emäsindikaattorina, sinun ei pitäisi reagoida nopeammin OH: n kanssa- ympäristöstä, joka analysoi määrittää.
Lisäksi, koska se on erittäin heikko happo, ryhmien läsnäolo -COOH on suljettu pois ja siksi happoprotonien lähde on kaksi OH -ryhmää, jotka on kytketty kahteen aromaattiseen renkaaseen,.
Kaava
Fenolftaleiini on orgaaninen yhdiste, jonka tiivistetty kemiallinen kaava on CkaksikymmentäH14JOMPIKUMPI4. Vaikka ehkä ei tarpeeksi selvittää, mitkä orgaaniset ryhmät omistavat, kaavasta voit laskea tyydyttymättömyyden, luurankon selvittämiseksi aloittamiseksi.
Kemiallinen rakenne
 Fenoliftaleiinin rakenne
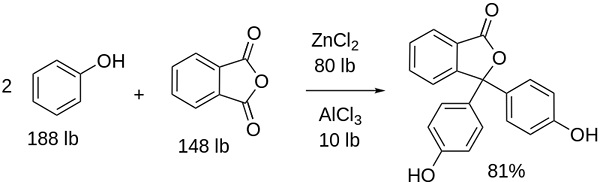
Fenoliftaleiinin rakenne Fenolftaleiinin rakenne on dynaaminen, mikä tarkoittaa, että se tapahtuu muutoksissa sen ympäristön pH: n mukaan. Ylemmässä kuvassa havainnollistetaan fenoliftaleiinin rakennetta 0 Pentagonaalinen rengas kärsii suurimmista muutoksista. Esimerkiksi perusväliaineessa, kun yksi OH-fenolirenkaiden ryhmistä, niiden negatiivinen kuormitus (-o-) houkutellaan aromaattiseen renkaaseen, "avataan" viisikulmainen rengas sen linkkien uudessa järjestelyssä. Tässä uusi negatiivinen kuorma sijaitsee ryhmässä -coo-, joka "tuli pois" Pentagonal Ringistä. Sitten, kun väliaineen emäksisyyttä on kasvatettu, fenolirenkaiden toinen OH -ryhmä ja tuloksena oleva kuorma on tuhoisa koko molekyylirakenteessa. Alempi kuva on yhteenveto kahden ei -deprotonoinnin tuloksesta perusväliaineessa. Tämä rakenne on vastuussa fenoliftaleiinin tutusta vaaleanpunaisesta väristä. Elektronit, jotka "kulkevat" konjugoidun π -järjestelmän läpi (esitetään kaksoisresonanssisidoksilla), absorboivat näkyvässä spektrissä, erityisesti keltaisen värin aallonpituuteen, heijastavat vaaleanpunaista väriä, joka saavuttaa odotettavan silmän. Fenolphthaleinilla on yhteensä neljä rakennetta. Kaksi edellistä ovat tärkeimmät käytännöllisesti ja esitetään lyhennettynä seuraavasti: H2Sisään ja sisään2-. Fenolftaleiinia käytetään kemiallisessa analyysissä visuaalisena indikaattorina määritettäessä ekvivalenssipisteen neutralointireaktioissa tai happo-emäsasteissa. Näiden happo-emäsarviointien reagenssi valmistetaan 1 %: n liuenneen 90 %: n alkoholiin. Fenolphthalein esittelee 4 osavaltiota: Tämä käyttäytyminen on mahdollistanut fenoliftaleiinin käytön osoituksena betonin hiilihapotuksesta, joka vaihtelee pH: n arvoksi välillä 8,5 - 9. Myös värien muutos on hyvin äkillinen; eli anionissa2- vaaleanpunainen tuotetaan suurella nopeudella. Tämän seurauksena tämä antaa sinun olla ehdokas indikaattorina monissa tilavuusmäärityksissä; Esimerkiksi heikko happo (etikkahappo) tai vahva (suolahappo). Fenolphthaleinia käytettiin laksatiivisena aineena. On kuitenkin olemassa ohjeellinen tieteellinen kirjallisuus, että joillakin laksatiiveilla, jotka sisältävät fenoliftaleiinia aktiivisena periaatteena - joka estää veden ja elektrolyyttien imeytymistä suuren suolen edistävissä evakuoinneissa - voi olla kielteisiä vaikutuksia. Näiden fenoliftaleiinia sisältävien lääkkeiden pitkäaikainen käyttö liittyy useiden suoliston toiminnan, haimatulehduksen ja jopa syövän häiriöiden tuotantoon, joka on tuotettu pääasiassa naisilla ja tämän kemiallisen yhdisteen farmakologisessa tutkimuksessa käytetyissä eläinmalleissa. Kemiallisesti modifioitua fenoliftaleiinia, ja muuttavat sen sitten vähentyneeksi tilaksi, reagenssina oikeuslääketieteellisissä testeissä, jotka sallivat hemoglobiinin läsnäolon määrittämisen näytteessä (Kastle-Meyer-testi), mikä ei ole vakuuttavaa väärien positiivisten läsnäolon takia. Se muodostuu ftaalihappoanhydridin kondensaatiolla fenolin kanssa, konsentroituneen rikkihapon läsnä ollessa ja alumiinin ja sinkkikloridien seosta reaktion katalyytteinä: Aromaattinen elektrofiilinen substituutio on mekanismi, joka hallitsee tätä reaktiota. Mistä se koostuu? Fenolirengas (vasemmanpuoleisen molekyyli) on negatiivisesti ladattu elektronien happiatomin ansiosta, mikä pystyy tekemään mistä tahansa vapaasta parista, joka kulkee renkaan "elektronisen piiri". Toisaalta ftaali -anhydridin ryhmän C = O hiili. Fenolirengas, runsaasti elektroneja, hyökkää tätä huonoa hiiltä elektroneissa, sisällyttäen ensimmäisen renkaan rakenteeseen. Tämä hyökkäys tapahtuu ensisijaisesti OH -ryhmään kytketyn hiilen vastakkaisessa päässä; Tämä on sijainti -puolesta. Sama koskee toista rengasta: se hyökkää samaan hiileen ja tästä muodostettu vesimolekyyli vapautuu happaman väliaineen ansiosta. Tällä tavoin fenoliftaleiini ei ole muuta kuin ftaalihappoanhydridimolekyyli, joka on sisällyttänyt kaksi fenolirengasta yhteen sen hiiliöryhmään (c = o). Sen fyysinen ulkonäkö on valkoinen kiinteä aine, jossa on trikliinikiteitä, usein agglomeroituja tai rombisten neulojen muodossa. Se on wc, tiheämpi kuin nestemäinen vesi (1 277 g/ml 32 ºC: lla) ja hyvin vähän haihtuvaa (arvioitu höyrynpaine: 6,7 x 10-13 MMHG). Se on hyvin vähän liukeneva veteen (400 mg/l), mutta erittäin liukenee alkoholiin ja eetteriin. Tästä syystä on suositeltavaa laimentaa se etanolissa ennen sitä. Se on liukenematon aromaattisissa liuottimissa, kuten bentseenissä ja tolueenissa, tai alifaattisissa hiilivedyissä, kuten n-heksaanissa. Löydetty 262,5 ºC ja nesteen kiehumispiste on 557,8 ± 50,0 ºC ilmakehän paineeseen. Nämä arvot viittaavat voimakkaisiin molekyylien välisiin vuorovaikutuksiin. Tämä johtuu vety sillasta, samoin kuin renkaiden välisistä etuvuorovaikutuksista. Sen PKA on 9,7 - 25 ºC. Tämä tarkoittaa erittäin matalaa trendiä dissosioitua vesipitoisessa väliaineessa: H2In (ac) + 2h2Tai (l) sisään2-(AC) + 2H3JOMPIKUMPI+ Tämä on vesipitoinen tasapaino. OH -ionien lisääntyminen kuitenkin- Liuoksessa nykyinen H: n määrä vähenee3JOMPIKUMPI+. Tämän seurauksena tasapaino liikkuu oikealle, tuottaa enemmän h3JOMPIKUMPI+. Tällä tavoin sen alkuperäinen menetys palkitaan. Kun lisää pohjaa lisätään, tasapaino siirtyy edelleen oikealle ja niin edelleen, kunnes lajista H ei ole mitään2Sisään. Tässä vaiheessa lajit2- Rosado väri liuoksen. Lopuksi fenoliftaleiini hajoaa kuumentuessa, säteilemällä hehtaaria ja ärsyttävää savua.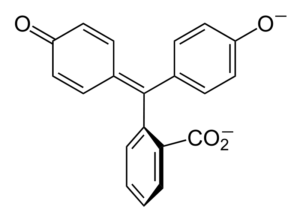
Käyttää/sovelluksia fenoliftaleiinin
 Alkalisen liuoksen lisääminen neutraaliin liuokseen fenoliftaleiinin indikaattorilla
Alkalisen liuoksen lisääminen neutraaliin liuokseen fenoliftaleiinin indikaattorilla Indikaattoritoiminto
Käyttö lääketieteessä
Fenolftaleiinisynteesi
Fenolphthalein -ominaisuudet
Viitteet