Kaliumpermanganaatti (KMNO4)

- 1871
- 539
- Louis Moen
 Kaliumpermanganaattikiteitä
Kaliumpermanganaattikiteitä Mikä on kaliumpermanganaatti?
Hän kaliumpermanganaattia (Kmno4) Se on epäorgaaninen yhdiste, joka on muodostunut ryhmän 7 (viib) -, happea ja kaliumin mangaanin siirtymämetallia. Se on tumman violetti lasimainen kiinteä. Hänen vesipitoiset ratkaisut ovat myös tumman violetteja; Nämä liuokset muuttuvat vähemmän violetiksi, koska ne laimennetaan suurina vesimäärissä.
Kaupallisesti saavutetaan tablettien, kiteiden ja pölyn esityksissä. Se tunnetaan Condy- tai Mineral Camaleón -nimillä. Termi "kameleontti" viittaa mineraalin kykyyn: Jos se muuttaa väriä kosketuksessa kaustisen soodan ja orgaanisen aineen kanssa, sokeri tapahtuu.
Kmno4 Se alkaa kärsiä pelkistyksiä (Gain Elektronit) seuraavan järjestyksen värien peräkkäin: Purple> Blue> Vihreä> Keltainen> Väritöntä (ruskean ruskean MNO: n kanssa2-A. Tämä reaktio osoittaa kaliumpermanganaatin tärkeän ominaisuuden: se on erittäin vahva hapettava aine.
Kaava
Sen kemiallinen kaava on KMNO4; eli jokaiselle kationille K+ On anion -MNO4- vuorovaikutuksessa tämän kanssa
Kaliumpermanganaatin kemiallinen rakenne
 KMNO4: n kiteinen rakenne
KMNO4: n kiteinen rakenne Yläkuvassa KMNO: n kiteinen rakenne on esitetty4, joka on ortorrominen tyyppi. Violetti pallot vastaavat Kations+, kun taas tetraedri on muodostunut neljästä punaisesta pallasta ja sinertävä pallo vastaa anionin MNO: ta4-.
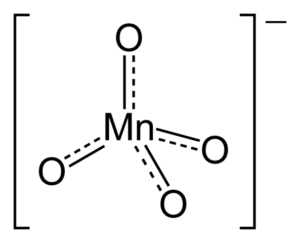
Miksi anionilla on tetraedrinen geometria? Sen Lewis -rakenne vastaa tähän kysymykseen. Katkoviivat tarkoittavat, että kaksoislinkit resonoivat Mn: n ja O: n välillä. Tämän rakenteen omaksumiseksi metallikeskuksessa on oltava hybridisaatio SP3.

Koska mangaanista puuttuu epätavallisia elektronipareja, MN-O-sidoksia ei työnnetä kohti samaa tasoa. Samoin negatiivinen kuorma jakautuu neljään happiatomiin, mikä vastaa Kationien suuntautumisesta+ Kiteisiin järjestelyihin.
Voi palvella sinua: ionisaatiovakioKMNO käyttää4
Lääketieteen ja eläinlääketieteen
Bakterisidisen vaikutuksensa vuoksi sitä käytetään lukuisissa sairauksissa ja olosuhteissa, jotka aiheuttavat ihovaurioita, kuten: jalat infektiot sienillä, impetigo, pinnalliset haavat, ihottuma ja trooppiset haavaumat.
Haitallisen vaikutuksensa vuoksi kaliumpermanganaattia on käytettävä alhaisissa pitoisuuksissa (1: 10000), mikä rajoittaa sen toiminnan tehokkuutta.
Sitä käytetään myös kalaparasitoosin hoidossa akvaarioissa, jotka tuottavat ihon suolista ja haavaumia koskevia infektioita.
Vedenkäsittely
Se on kemiallinen uudistaminen, jota käytetään raudan, magnesiumin ja rikkivetyjen poistamiseen vedestä (epämiellyttävän hajun), kykenevä käyttämään jäteveden puhdistamiseen.
Rauta- ja magnesium saostuvat liukenemattomien vesioksidien muodossa. Lisäksi se auttaa poistamaan putkissa läsnä olevan ruosteen.
Hedelmien säilyttäminen
Kaliumpermanganaatti poistaa banaaneissa tuotetun eteenin aikana, jolloin se voi pysyä yli 4 viikkoa kypsymättä, myös huoneenlämpötilassa.
Afrikassa he käyttävät sitä vihannesten liottamiseen, neutraloida ja eliminoida kaikki nykyiset bakteeriaineet.
Palotoiminta
Kaliumpermanganaattia käytetään tulen jatkamisen rajoittamiseen. Perustuen permanganaatin kykyyn aloittaa tulipalo, sitä käytetään vastavirtojen luomiseen metsäpaloissa.
Redox -otsikko
Analyyttisessä kemiassa sen standardisoidut vesiliuokset käytetään hapettimena redox -määrityksissä.
Orgaaninen reagenssi
Sen tarkoituksena on muuntaa alkeenit dioleiksi; eli kaksi OH -ryhmää lisätään kaksoissidokseen c = c. Seuraava kemiallinen yhtälö:

Myös rikkihappoliuos kromihapolla (H2Kro4) Sitä käytetään primaaristen alkoholien (R-OH) hapettumiseen karboksyylihapoihin (R-COOH tai RCO2H).
Voi palvella sinua: ei -polaarinen kovalenttinen sidosSen hapettumisteho on riittävän vahva hapettamaan aromaattisten yhdisteiden primaariset tai sekundaariset alkyyliryhmät "karboksikoivat ne"; toisin sanoen sivuketjun R muuntaminen (esimerkiksi CHO3) COOH -ryhmässä.
Historialliset käytöt
Se oli osa jauheita, joita käytettiin salamana valokuvauksessa tai termiittireaktion käynnistämiseen.
Sitä käytettiin toisessa maailmansodassa valkoisten hevosten naamiointiin päivän aikana. Tätä varten he käyttivät mangaanidioksidia (MNO2), joka on ruskea; Tällä tavalla he jäivät huomaamatta.
KMNO -synteesi4
Pyrolusiitti mineraali sisältää mangaanidioksidia (MNO2) ja kaliumkarbonaatti (Caco3-A.
Vuonna 1659 kemisti Johann R. Glauber sulasi mineraalin ja liukasti sen veteen tarkkailemalla vihreän värin esiintymistä liuoksessa, joka myöhemmin muuttui violettivärinä ja lopulta punaiseksi. Tämä viimeinen väri vastasi kaliumpermanganaatin sukupolvea.
19. vuosisadan puolivälissä Henry Condy haki antiseptistä tuotetta ja käsitteli alun perin pyrolusiittia NaOH: lla ja myöhemmin KOH: lla, tuottaen niin kutsutut kondyylikiteitä; eli kaliumpermanganaatti.
Kaliumpermanganaatti tuotetaan teollisesti mangaanidioksidista, joka on läsnä pyrolusiitti -mineraalissa. MNO2 Läsnä mineraalissa reagoi kaliumhydroksidin kanssa ja lämmitetään myöhemmin hapen läsnä ollessa.
2 mno2 + 4 Koh +tai2 => 2 k2Mne4 + 2 h2JOMPIKUMPI
Kalium -manganaatti (k2Mne4) muunnetaan kaliumpermanganaattiin elektrolyyttisellä hapettumisella alkaliseen väliaineeseen.
2 K2Mne4 + 2 h2O => 2 kmno4 + 2 KOH +H2
Toisessa reaktiossa kaliumpermanganaatin tuottamiseksi kalium -manganaatti reagoi2, suhteellisen prosessin kiihdyttäminen:
3 K2Mne4 + 2 co2 => 2 kmno4 + Mne2 + K -k -2Yhteistyö3
Voi palvella sinua: Molecular Orbital TheoryMNO: n sukupolven vuoksi2 (mangaanidioksidi) Prosessi on epäsuotuisa, KOH on luotava K: stä2Yhteistyö3.
KMNO: n ominaisuudet4
Se on violetti kiteinen.
Se ei ole kovin liukoinen veteen (6,4 g/100 ml 20 ºC: lla), mikä osoittaa, että vesimolekyylit eivät ratkaise suurelta osin MNO -ioneja4-, Koska ehkä heidän tetraedriset geometriat vaativat paljon vettä niiden liukenemiseen. Samoin se voi myös liukenemista metyylialkoholiin, asetoniin, etikkahapeen ja pyridiiniin.
Hajoaminen
Se hajoaa 240 ºC: n nopeudella vapauttaen happea:
2 kmno4 => K2Mne4 + Mne2 + JOMPIKUMPI2
Voit kokea hajoamisen alkoholin ja muiden orgaanisten liuottimien vaikutuksesta, samoin kuin vahvojen happojen ja vähentävien aineiden vaikutuksesta.
Hapetusvoima
Tässä suolassa mangaani osoittaa suurimman hapettumistilansa (+7) tai mikä on sama, enimmäismäärään elektroneja, jotka se voi menettää ionisella tavalla. Sähköinen mangaanin kokoonpano puolestaan on 3d -d54s2; Siksi mangaaniatomin koko Valencia -kerros on "tyhjä" kaliumissa.
Sitten mangaaniatomi esittelee luonnollisen taipumuksen saada elektroneja; toisin sanoen alkamaan muihin hapettumistiloihin alkalisessa tai happamassa väliaineessa. Tämä on selitys miksi KMNO4 Se on voimakas hapettava aine.
Viitteet
- F.Albert Cotton ja Geoffrey Wilkinson, FRS. (1980). Edistynyt epäorgaaninen kemia. Toimitus Limusa, Meksiko, 2. painos, sivu 437-452.
- Robin Wasserman. Lääketieteelliset käytöt kaliumpermanganaatille. Livestrong toipunut.com
- Clark d. Kolme Ultimate käyttää kaliumpermanganaattia. Toipunut tekniikasta.org
- J -.M. Cedardea, c. Arnáiz ja E. Díaz. Kaliumpermanganaatti: voimakas ja monipuolinen hapettiminen. Osasto. Kemikaali- ja ympäristötekniikka. Sevillan yliopiston korkeakoulu.

