Tiivistetty kaava Mikä on ja esimerkkejä (metaani, etaani, glukoosi ...)
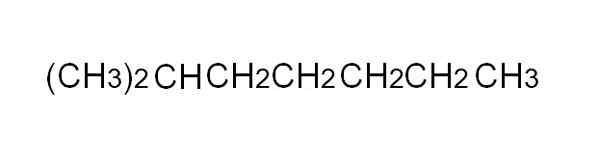
- 2487
- 326
- Joshua Emmerich
Se tiivistetty kaava Se on puhtaasti tekstin esitys molekyylistä, jossa linkit jätetään pois. Sen tarkoituksena on tietää, mikä on atomien tilaaminen. Yleensä lineaariset tai haarautuneet molekyylit ovat tiivistettyjä kaavoja, paitsi syklisiä tai niitä, jotka ovat erittäin haarautuneita.
Orgaanisessa kemiassa on yleensä sekaannusta siitä, mikä on ero tämän kaavan ja molekyylin välillä. Itse asiassa on yleistä löytää ne synonyymeiksi. Samaan aikaan epäorgaanisessa kemiassa käytetään enemmän molekyylimuotoja, koska useimmissa tapauksissa kovalenttiset yhdisteet kuvaavat perustellusti; Kuten vesi, h2JOMPIKUMPI.
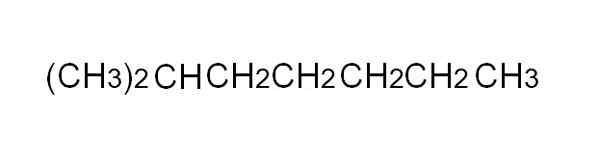 2-metyylipeptanon tiivistynyt kaava. Lähde: Gabriel Bolívar.
2-metyylipeptanon tiivistynyt kaava. Lähde: Gabriel Bolívar. [TOC]
Mikä on tiivistetty kaava?
Sen määrittelemiseksi helpommin tiivistetty kaava on yksinkertaistettu esitys puoliksi kehitetystä. Yksinkertaisia linkkejä ei tarvitse kirjoittaa, eikä sen pitäisi peittää useampaa kuin yhtä riviä tekstissä. Esimerkiksi 2-metyylipeptano, haarautunut alkaani, voidaan edustaa samalla rivillä kuin ylemmässä kuvassa.
Kondensoituneet kaavat ovat hyödyllisiä edustaa joitain molekyylejä tarvitsematta piirtää niitä. Tämä on erinomaista, kun kemialliset yhtälöt on kirjoitettu, kun sykliset tai hyvin haarautuneet molekyylit eivät osallistu. Nähdään, että nämä kaavat turvautuvat suluihin molekyylin esityksen yksinkertaistamiseksi edelleen.
Esimerkit
Metaani
Metaani on ainoa kemiallinen yhdiste, jolla on yksi kaava: ch4. Tämä vastaa empiiristä, molekyyliä, tiivistettyjä ja puoliksi kehitettyjä samanaikaisesti. Siksi monta kertaa, säästämään sekaannus kaikkien näiden käsitteiden välillä, ihmiset mieluummin viittaavat yksinkertaiseen ja epätarkkaun yhdisteen "kemialliseen kaavaan".
Etano
Estanolla on molekyylinen kaava C2H6. Tiivistynyt kaava on sen sijaan CHO3CH3. Huomaa, että C-C-linkki ja C-H-linkit jätetään pois. Ajatuksena on pystyä kirjoittamaan kaava ikään kuin se olisi "sana" ilman, että sinun tarvitsee piirtää raitoja tai piirtää rakenteita.
Voi palvella sinua: PycnometriMääritelmän mukaan molekyylinen kaava on c2H6 eikä ch3CH3; Yksinkertaisten molekyylien kohdalla molemmat kaavat ovat kuitenkin tapana vaihtaa, vaikka se on edelleen väärä. Tämä on ristiriitaisten välillä useiden lähteiden välillä, joissa tässä suhteessa on ilmeisesti erityisiä sääntöjä.
Glukoosi ja fruktoosi
Tässä on esimerkki, jossa virhe havaitaan heti, kun haluat vaihtaa molekyylikaavan kondensaattiin.
Makealla, glukoosilla ja fruktoosimomentilla on sama molekyyl kaava: C6H12JOMPIKUMPI6, Ja siksi tämä ei auta niiden erottamista. Sitä vastoin rakenteelliset ja puoliksi kehittyneet kaavat muodostavat näkymät erilaisia molekyylejä.
Glukoosilla tai fruktoosilla on kuitenkin tiivistetty kaava. Tämä johtuu siitä, että niiden esityksestä tai projektiosta riippumatta niiden rakenteita ei voida kirjoittaa samaan linjaan; tai ainakin miellyttävällä ja yksinkertaisella tavalla lukijan silmissä.
Butaani
Butanolla on molekyylinen kaava C4H10. Siinä on kaksi isomeeriä: lineaarinen, n-Butano ja haarautunut, 2-metyylipropaani. Molempia voidaan edustaa niiden tiivistettyjen kaavojen avulla. Hän n-Butano on ch3CH2CH2CH3 tai ch3(CH2-A2CH3, Ja 2-metyylipropaani on CHO3Ch (ch3-A2 tai (ch3-A3CH.
2-metyylipropanissa meillä on ryhmä CH, jota ympäröi kolme CHO: ta3. Sen kaksi kaavaa ovat kelvollisia, ja suluja käytetään seurausten korostamiseen, tilaus on indikaattori siitä, kuinka monta ryhmää muodostavat tämän haaran.
Etanoli
Etanolilla on tiivistetty kaava ch3CH2vai niin. Huomaa, kuinka paljon se muistuttaa puoliksi kehitettyä kaavaa: ch3-CH2-vai niin. Samalla tavalla se tehdään propanolilla, CHO3CH2CH2Voi, n-Butanoli, ch3CH2CH2CH2Voi, ja kaikkien muiden alkoholien kanssa.
Voi palvella sinua: Natriumfosfaatti: rakenne, ominaisuudet, synteesi, käyttääJos heillä on haara, se osoitetaan atomin oikealla puolella, johon se on linkitetty. Esimerkiksi 2-metyylibutanoli voitaisiin kirjoittaa seuraavasti: ch3CH2Ch (ch3) Ch2vai niin. Huomaa, että monille molekyyleille se alkaa olla helpompaa turvautua rakenteelliseen tai osittain kehitettyyn kaavaan.
Pentaneo
Pentanin lineaarinen isomeri, n-Pentano, sen tiivistettyä kaavaa on helppo edustaa: Cho3CH2CH2CH2CH3. Tätä kaavaa voidaan myös yksinkertaistaa suluilla: ch3(CH2-A3CH3, osoittaen, että kahden CH: n välillä3 CH on kolme2.
Pentanin kaksi muuta isomeeriä ovat kuitenkin hieman monimutkaisempia: ch3CH2Ch (ch3-A2, 2-metyylibutaanille ja C (C3-A4 2,2-dimetyylipropaanille tai neopantumille. Huomaa, että sulujen vasemmalla puolella oleva hiiliatomi on se, joka muodostaa yhteydet substituenteihin tai seurauksiin.
Oktaani
Oktaanin lineaarinen isomeeri, n-Oktaani, sen pituuden vuoksi on nyt aiheellista edustaa sen tiivistettyä kaavaa kuin Cho3(CH2-A6CH3. Juuri tässä vaiheessa on oltava jonkin verran tiivistettyjä kaavoja: he pyrkivät säästämään aikaa edustaessaan molekyylejä tai yhdisteitä kirjoittamatta niin paljon paperille.
Sykloheksa
Sykloheksanin tapaus on samanlainen kuin glukoosin ja fruktoosin tapaus: muodollisesti puuttuu tiivistetty kaava syklisen yhdisteen vuoksi. Tapa yrittää edustaa sitä olisi: (ch2-A6, mikä tarkoittaa, että kuusi ryhmää Cho2 Ne on linkitettävä, koska ne ovat mahdollisia vain, jos ne sulkeutuvat kuusikulmaiseen renkaaseen. On kuitenkin parempi piirtää rengas.
Asetoni
Asetoni esittelee karbonyyliryhmän hallussapidon erityispiirteet, c = o. Siksi tiivistetyn kaavan kirjoittamiseksi meillä on kolme vaihtoehtoa: (ch3-A2Co, ch3C (o) ch3 tai ch3(C = o) ch3.
Voi palvella sinua: Kahvihappo: rakenne, ominaisuudet, biosynteesi, käyttääItse asiassa suuremmissa molekyyleissä karbonyyliryhmä esitetään yleensä nimellä (O) ottaen huomioon.
Etikkahappo
Etikkahapon tiivistynyt kaava on CHO3Cooh o ch3Yhteistyö2H. Tässä on tärkeä kohta: samaan riviin kirjoitetut funktionaaliset ryhmät ovat tiivistetyn kaavan osia. Näin oli etanolin ja asetonin tapaus, ja sitä koskee myös tioles (-sh), aldehydos (-cho) esterit (-co2R o -coor) ja amiinit (-nh2-A.
Yleinen kommentti
Molekyyli- ja kondensoituneiden kaavojen välillä on paljon sekaannusta. Ehkä se johtuu siitä, että pelkästään nämä esitykset tarjoavat jo likimääräisen kuvan molekyylistä, joten mielestämme se on molekyyl kaava.
Myös kaavat, kuten c6H12JOMPIKUMPI6 Niitä pidetään myös kondensaattina, koska niitä yksinkertaistetaan, "kondensoi" atomien ja alaindeksien molekyyliä. Siksi on yleistä nähdä, kuinka kaksi kaavaa mainitaan ikään kuin ne olisivat synonyymejä.
Monissa lähteissä, mukaan lukien Wikipedia -artikkelit, termejä 'kemiallinen kaava' käytetään viittaamaan molekyyliin (tyyppi C6H12JOMPIKUMPI6 ja muut), ja 'kaava' viitata kondensaattiin.
Viitteet
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Helmestine, Anne Marie, PH.D -d. (18. marraskuuta 2019). Tiivistetty kaavan määritelmä kemiassa. Toipunut: Admingco.com
- James Ashenhurst. (11. joulukuuta 2019). Tiivistetyt kaavat: Selkärangan purkaminen tarkoittavat. Orgaaninen kemia. Toipunut: MasterorganicChemistry.com
- Copolingenieria. (2. toukokuuta 2016). Empiirinen, rakenteellinen ja kondensaatti kaava. Haettu osoitteesta: ChemioTeCablog.WordPress.com
- Johdanto kemiaan: yleinen, orgaaninen ja biologinen. (S.F.-A. Tiivistetyt rakenne- ja viivakulmakaavat. Palautettu: 2012 -kirjoista.Lardbucket.org
- « 250 parasta vastaamattomia kysymyksiä
- Heptano (C7H16) rakenne, ominaisuudet ja käyttötarkoitukset »

