Bakteerien levitys mikä on, ominaisuudet ja valmisteet
- 4273
- 282
- Ronald Reilly
Hän Bakteeri- Se on jatkoa bakteerimikro -organismien suspension ohutkalvoa, joka on valmistettu läpinäkyvälle lasilevylle tai liukumäelle, havainnointia varten optisen mikroskoopin alla.
Elokuvan muodossa oleva laajennus suoritetaan mikro -organismien erottamiseksi mahdollisimman paljon, koska jos havainto on ryhmitelty.
Bakteerikasvien tutkimuksessa käytetään niiden analysointia, kiinnitys- ja värivalmistustekniikoita. Mikro -organismien pienen koon takia tarkkailuun tarvitaan optisen mikroskoopin käyttöä.
Optiset mikroskoopit ovat välttämättömiä instrumentteja levityksen havaitsemiseksi. Nämä käyttävät optisia linssejä ja valoa, mikä mahdollistaa näytteiden visualisoinnin, joiden koko on suuri.
Yleensä elävissä soluissa ei ole pääosin värillisiä rakenteita, näkymät optiseen mikroskoopiin ovat värittömiä, läpinäkyviä näytteitä ja osoittavat hyvin vähän sisäistä kontrastia ja niiden ympäristöä.
Havainto selkeän kentän yksinkertaisella optisella mikroskoopilla ilman apuvärjäystekniikoiden käyttöä on hyvin rajallinen ja sitä käytetään vain joissain tapauksissa, kuten mikro -organismiliikkeen havainnoinnissa.
Mikro -organismien havaitsemiseksi optimaalisesti on välttämätöntä saavuttaa tasapaino kontrastin ja resoluution välillä. Solujen yksityiskohtia ei voida havaita mikroskoopissa, jopa korkealla resoluutiolla; Väriaineen käyttöä värjäystekniikoiden avulla tarvitaan, mikä lisää havaintojen kontrastia.
Laadukkaan bakteerien levitysominaisuudet
Erinomainen kontrasti
Erinomaisen kontrastin saavuttamiseksi on hienostuneita mikroskooppeja vaihekontrastimikroskooppi, differentiaaliset häiriöt ja tumman kentän mikroskooppi. Tämän tyyppistä mikroskooppia käytetään bakteerirakenteiden, kuten palkojen ja filamenttien, tarkkailuun.
Värjäys on yksinkertainen tekniikka lisäämään kontrastia, joka saavutetaan selkeällä kenttämikroskoopilla. Tässä tekniikassa voidaan käyttää erilaisia väriaineita, jotka parantavat merkittävästi mikroskoopin havaintoa.
Värjäys tehdään suoraan diojen mikro -organismien suspensioiden levyihin tai pidennyksiin, aiemmin kuivattuihin ja kiinteisiin.
Hyvä kiinteä
Kiinnitys on tekniikka, jota käytetään solurakenteiden säilyttämiseen; aiheuttaa mikro -organismien inaktivoinnin ja liukumäen lasiin tarttumisen. Käsittelyjä on erilaisia: lämmön kiinnitys ja kemiallinen kiinnitys.
Voi palvella sinua: palmitholiisiinihappo: rakenne, toiminnot, missä se onLämmön kiinnitys
Tämä on eniten käytetty menetelmä bakteerien levityksen havainnoinnissa. Tekniikka koostuu levitysbakteerisuspension läpäisemisestä vaaleamman liekin avulla. Tämä tekniikka pystyy säilyttämään bakteerien ulkoisen morfologian, mutta tuhoaa sen sisäiset rakenteet.
Kemiallinen kiinnitys
Kemiallinen kiinnitys käyttää säilyttämisessä kemiallisia aineita, kuten formaldehydi tai formaliini, etanoli ja etikkahappo, muun muassa. Kemiallisten aineiden kiinnittämisen etuna on, että mikro -organismien sisäisten solurakenteiden säilyttäminen saavutetaan.
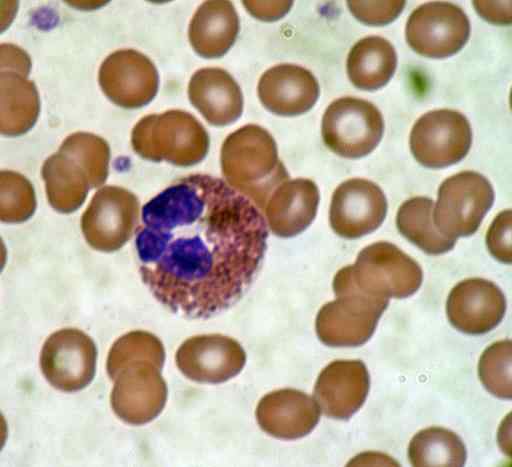
 Verenpoikki. Lähde: Bobjgalindo [GFDL (http: // www.GNU.Org/copyleft/fdl.html) tai cc by-sa 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)], Wikimedia Commons
Verenpoikki. Lähde: Bobjgalindo [GFDL (http: // www.GNU.Org/copyleft/fdl.html) tai cc by-sa 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)], Wikimedia Commons Hyvä värjäys
Yleisimmät menettelytavat aiemmin kuivumisen ja kiinteän levyn värjäytymisen suorittamiseksi ovat positiivinen tai yksinkertainen värjäys, differentiaalivärjäys ja negatiivinen värjäys. Tietyissä solurakenteissa on myös erityisiä tekniikoita (kapseli, itiöt, flagella).
Positiivinen värjäys tai yksinkertainen värjäys
Positiivinen tai yksinkertainen värjäys on eniten käytetty levitystekniikka. Käytä väriaineita, joilla on kyky liittyä tiettyihin mikrobirakenteisiin, jolloin ne voivat tarkkailla niitä mikroskoopissa.
Näissä väriaineissa on kromofoorisia ryhmiä (värillinen osa) kemiallisessa rakenteessaan vaihtoehtoisilla kaksoissidoksilla ja yksinkertaisilla sidoksilla (konjugaatio). Nämä linkit voivat puolestaan luoda ionisia tai kovalenttisia sidoksia joidenkin solurakenteiden kanssa.
Positiivisessa tai yksinkertaisessa värjäyksessä käytetyt väriaineet ovat enimmäkseen kemiallisia johdannaisia aniliini (Värilliset orgaaniset suolat).
Toisaalta väriaineiden joukosta löydämme joitain emäksisellä pH: lla ja toiset happamassa pH: lla.
Perusvärit
Perusväriaineilla kromoforiryhmällä on positiivinen sähkövaraus. Suurimmalla osalla prokaryoottisia mikro -organismeja on sisäinen neutraali pH, ja niiden solun pinnalla on negatiivinen kuorma. Tämän sähköstaattisen vuorovaikutuksen kautta kromofori sitoutuu soluun ja väriaineen.
Esimerkkejä perusväriaineista ovat muun muassa metyleenin sininen, violetti lasi, malakkiittivihreä, perussulake, safraniini.
Happovärit
Happamissa väriaineissa kromoforiryhmällä on negatiivinen sähkövaraus. Näitä käytetään proteiinien värjäytymiseen positiivisilla varausryhmillä. Esimerkkejä happoväriaineista ovat happamoke, bengali ruusu, Kongo Red ja Eosin.
Se voi palvella sinua: Profage: Mikä on, tyypit ja niiden ominaisuudetDifferentiaalinen värjäys
Erotteluvälitystekniikka on käyttää kahta eri väriä tai voimakkuutta väriainetta mikroskoopin mikroskoopin erottamiseksi. Gram-värjäys ja happo-alkoholiresistenssivärjäys ovat eniten käytettyjä erilaisia värjäytyksiä bakteriologiassa.
Gramin värjäystä käytetään alustavana testinä muodon, koon, soluryhmän tuntemiseksi soluseinämän tyypin lisäksi. Gram -värjäyskokeella soluseinämän bakteerit luokitellaan GRAM -positiivisiksi bakteereiksi ja gram -negatiivisiksi bakteereiksi.
Negatiivinen värjäys
Tässä tekniikassa käytetään kemiallisia väriaineita, jotka eivät tunkeudu solujen sisätiloihin, vaan tekevät väliaineesta, jossa mikro -organismit ovat mustana taustana.
Negatiivisessa värjäystekniikassa levitys valmistetaan tipalla kiinalaisia tai nigrosiinimustejousitusta, joka huoneenlämpötilassa kuivumisen sallimisen jälkeen muodostaa läpinäkymättömän kalvon valon kulkemiseen. Tällä tavoin mikro -organismeja havaitaan kirkkaina muodoina tummalla taustalla.
Valmistautuminen
-Lla. Levittää
1.- Pese erittäin hyvin dioja, kuivaa absorboivalla paperilla ja merkitse ne. Etiketin on ilmoitettava sen käsitellien valmistelun, päivämäärän ja nimen sisältö.
2.- Sytytä kevyempi ja steriloi liekin inokulaatiokahva punaiseksi elossa.
3.- Antaa käsitys.
4.- Ota bakteerien satoputki, poista korkki ja siirrä putken suun nopeasti kevyemmän liekin lähellä (liekki).
5.- Syötä inokulaatiokahva putkeen, joka sisältää bakteeriviljelmän ja ota näyte.
6.- Jos sato on nesteessä, aseta kahva otettu näyte liukun keskelle ja laajenna sitä varovasti halkaisijaltaan noin 2 cm: n ympyrään.
7.- Steriloi inokulaatiokahva.
8.- Anna saastumisen kuivuminen ilmassa.
9.- Toista vaiheet 3: sta 8: een kolme kertaa.
10.- Jos sato on kiinteä, tippa tislattua vettä on aikaisemmin asetettava liukumäelle. Tämä tehdään pienen näytteen sekoittamiseksi inokulaatiokahvalla otetusta sadosta vaiheiden 2 - 5 (ASEPSIS -olosuhteiden) indikaatioiden mukaan (ASEPSIS).
Se voi palvella sinua: Kehitysbiologia: historia, mitä tutkimuksia, sovelluksiayksitoista.- Laajenna näytte, joka on laimennettu veden pudotuksella liukussa ja toista kolme kertaa.
B -. Kiinnitys
1.- Lisää kuivaprosentin opettajat nestemäisessä keskipitkässä -kaksi tippaa metanolia tai absoluuttista etanolia.
2.- Anna ilmakuivata pois kevyemmältä.
3.- Jos levitys tulee kiinteästä viljelmästä, kuivahaju on valmistettu lämmöllä, ohittaen sen 2-3 kertaa nopeasti.
4.- Kosketa levityksen pohjaa vasemman käden selkäosan kanssa (oikealla kädessäsi; muuten käytä oikeaa kättä) ja varmista, että se on kylmä.
C. Yksinkertainen värjäys
1.- Lisää valittua väriaineen sadetta 2 tippaa ja anna toimia kunkin väriaineen erityisissä protokollissa tarvittava aika (yleensä välillä 1–5 minuuttia).
2.- Jotkut väriaineet vaativat lämmönkäyttöä aktivoitumiseen, jolloin sinun on oltava erittäin varovainen, kun lämmitetään matkatavaroita kevyemmän liekissä (manipuloimalla sitä pinsetteillä ja välttämällä kiehua). Smulaarin ylikuumeneminen voi tuhota halutut solut.
3.- Poista ylimääräinen väriaine tislatulla vedellä kuvasta. Poista veden pesu, lyömällä varovasti sen kappaleen liukua, joka on kalteva työpöydälle.
4.- Salli ilmankuivaus.
5.- Havaintotyypistä riippuen kannetta käytetään tai ei tässä vaiheessa. Peite ja säilyttää levitys. Jos tässä vaiheessa suoritetaan öljyn sukellusvaikutus, levitystä ei käytetä, mutta sadetta ei voida säilyttää.
D -d. Lopullinen säilytys
1.- Upota levitys peräkkäin jokaisessa jäljempänä ilmoitetussa ratkaisussa, vähintään 5 minuutin ajan. Näiden "kylpyhuoneiden" tarkoituksena on jättää levitys täysin kuivuneeksi. Jokainen reagenssi on tyhjennettävä hyvin, ennen kuin se saapuu seuraavaan kylpyhuoneeseen.
Dehydratointien järjestys on seuraava:
- 70 % etanolia
- 95 % etanoli
- Puhdas asetoni
- Asetoniseos -xiloli 1: 1
- Ksiloli
Anna sitten ilmankuivaus.
2.- Asenna kannet, mieluiten 22 × 22 mm, käyttämällä Kanadan balsamia tai muita kokoonpanoon.
Viitteet
- Cappucino, j.G. ja Welch, c.T. (2017). Mikrobiologia: manuaalinen laboratorio. Pearson.
- Holt, J.G. Toimittaja. (1977). Lyhyempi Bergeyn määräävän bakteriologian käsikirja. 8th Baltimore: Williams ja Wilkins Co.
- « Mikä on disulfurinen mikä on, rakenne, ominaisuudet, käyttää
- Mikä on Sigmund Freudin psyykkinen laite? »

