Karbonyyliryhmän ominaisuudet, ominaisuudet, nimikkeistö, reaktiivisuus
- 4197
- 8
- Gustavo Runte DVM
Hän Karbonyyliryhmä Se on orgaaninen ja hapetettu funktionaalinen ryhmä, joka muistuttaa hiilimonoksidimolekyyliä. Sitä esitetään C = O: ksi, ja vaikka sitä pidetään orgaanisena, sitä löytyy myös epäorgaanisista yhdisteistä; Kuten hiilihappo, H2Yhteistyö3, tai organometallisissa yhdisteissä, joiden CO on sitoutunut.
Tämä ryhmä erottuu kuitenkin hiilikemiassa, elämässä, biokemiassa ja muissa analogisissa tieteellisissä haaroissa. Jos se ei olisi hänelle, monet molekyylit eivät voineet olla vuorovaikutuksessa veden kanssa; Proteiineja, sokereita, aminohapoja, rasvoja, nukleiinihappoja ja muita biomolekyylejä ei olisi olemassa, jos se ei olisi sen puolesta.
 Karbonyyliryhmä. Lähde: Jü [julkinen verkkotunnus]
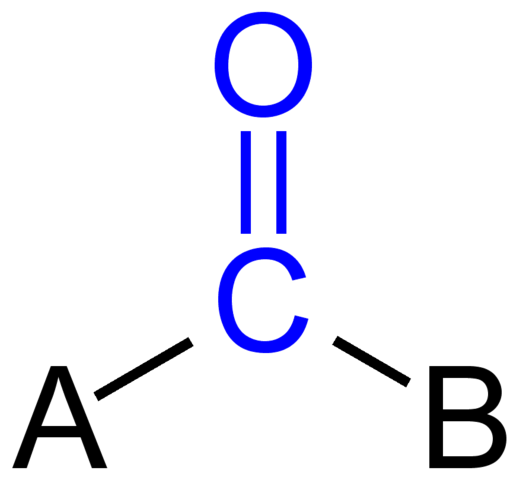
Karbonyyliryhmä. Lähde: Jü [julkinen verkkotunnus] Yläkuva osoittaa, kuinka tämä ryhmä näyttää yhdisteen yleisessä luurankoissa. Huomaa, että sininen väri korostaa sitä, ja jos poistamme korvaukset a ja b (r tai r ', yhtä pätevä), hiilimonoksidin molekyyliä olisi. Näiden substituenttien läsnäolo määrittelee suuren määrän orgaanisia molekyylejä.
Jos A ja B ovat hiiliatomeja, kuten metalleja tai ei -metallisia elementtejä, voidaan tehdä organometallisia tai epäorgaanisia yhdisteitä. Orgaanisen kemian tapauksessa substituentit a ja b ovat aina tai vetyatomeja, hiilihapotettuja linjoja, seurauksilla tai ilman seurauksia, syklisiä tai aromaattisia renkaita.
Siksi se alkaa ymmärtää, miksi karbonyyliryhmä on melko yleinen niille, jotka tutkivat luonnollisia tai terveystieteitä; Se on kaikkialla, ja ilman sitä soluissamme tapahtuvia molekyylimekanismeja ei tapahdu.
Jos sen merkitys voitaisiin tiivistää, sanotaan, että se tarjoaa polaarisuuden, happamuuden ja reaktiivisuuden molekyyliin. Jos on karbonyyliryhmä, on enemmän kuin todennäköistä, että juuri siinä vaiheessa molekyyli voi kärsiä muutoksesta. Siksi se on strateginen paikka kehittää orgaanista synteesiä hapetusten tai nukleofiilisten hyökkäysten avulla.
[TOC]
Karbonyyliryhmän ominaisuudet ja ominaisuudet
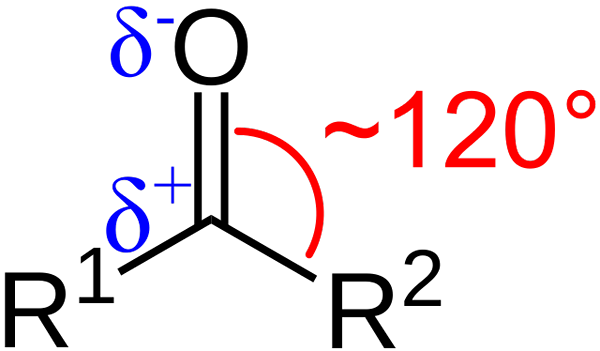 Karbonyyliryhmän rakenteelliset ominaisuudet. Lähde: Atsaliini Gomberg [julkinen alue].
Karbonyyliryhmän rakenteelliset ominaisuudet. Lähde: Atsaliini Gomberg [julkinen alue]. Mitkä ovat karbonyyliryhmän rakenteelliset ja elektroniset ominaisuudet? Ylöspäin1 ja r2 A: n ja B: n sijasta, joka on substituenttien ja happiatomin välillä kulma 120 ° C; Toisin sanoen geometria tämän ryhmän ympärillä on trigonaalinen tasainen.
Mikä on sellainen geometria2; Siten hiilellä on kolme SP -kiertorataa2 Yksinkertaisten kovalenttisten linkkien muodostaminen R: n kanssa1 ja r2, ja kiertorata p Puhdas kaksoissidoksen muodostamiseksi hapen kanssa.
Tällä tavoin selitetään, kuinka voi olla kaksoissidos c = o.
Jos kuvaa havaitaan, nähdään myös, että happea on suurempi elektroninen tiheys, Δ-, kuin hiili, δ+. Tämä johtuu siitä, että happi on enemmän elektronegatiivista kuin hiiltä, ja siksi "varastaa" elektronisen tiheyden; Ja ei vain hänelle, vaan myös substituenteille r1 ja r2.
Tämän seurauksena syntyy pysyvä dipolimomentti, joka voi olla suurempi tai pienempi kuin molekyylirakenteesta riippuen. Missä on karbonyyliryhmä, on dipolimomentteja.
Resonanssirakenteet
 Tämän orgaanisen ryhmän kaksi resonanssirakennetta. Lähde: Mfomich [CC0]
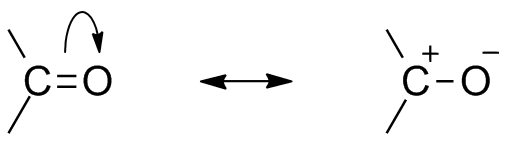
Tämän orgaanisen ryhmän kaksi resonanssirakennetta. Lähde: Mfomich [CC0] Toinen seuraus hapen elektronegatiivisuudesta on, että karbonyyliryhmässä on resonanssirakenteita, jotka määrittelevät hybridi (ylemmän kuvan kahden rakenteen yhdistelmä). Huomaa, että elektronipari voi siirtyä kiertoradalle p happea, joka jättää hiiliatomin positiivisella osittaisella kuormalla; Carbocation.
Voi palvella sinua: sykloalcanos: ominaisuudet, reaktiot, käytöt, esimerkitMolemmat rakenteet tapahtuvat jatkuvasti, joten hiili ylläpitää elektronien jatkuvaa puutetta; Eli kationille, jotka ovat hyvin lähellä sitä. Mutta jos se on anioni tai laji, joka pystyy luovuttamaan elektroneja, se tuntee voimakkaan vetovoiman tähän hiileen.
Sitten niin kutsutaan nukleofiiliseksi hyökkäykseksi, joka selitetään seuraavassa osassa.
Nimikkeistö
Kun yhdisteessä on ryhmä C = O, sanotaan, että se on karbonyyli. Siten karbonyyliyhdisteen luonteesta riippuen sillä on omat nimikkeistösäännöt.
Vaikka jokaisella on yhteinen sääntö riippumatta siitä, mikä on, hiilihiiliatomien listautumishetkellä C = O on etusijalla.
Tämä tarkoittaa, että jos on olemassa seurauksia, halogeeniatomeja, typpejä funktionaalisia ryhmiä, kaksois- tai kolminkertaisia linkkejä, yksikään niistä ei voi kantaa pienempää määrää kuin C = O; Siksi pisin ketju alkaa luetella mahdollisimman lähellä karbonyyliryhmää.
Jos päinvastoin on useita c = tai ketjussa, ja yksi niistä on osa suuremman hierarkian funktionaalista ryhmää, niin karbonyyliryhmä kantaa suuremman paikan ja mainitaan okso -substituentina.
Ja mitä sanotaan hierarkia? Seuraava, korkeimmasta alaikäiseen:
-Karboksyylihapot, RCOOH
-Ester, rcoor '
-Amida, Rconh2
-Aldehydi, RCOH (tai RCHO)
-Cetona, RCOR
Korvaamalla r ja r 'molekyylisegmenteillä, loputtomien karbonyyliyhdisteiden edustajat yllä olevat perheet: karboksyylihappot, esterit, amidas jne. Jokainen on yhdistänyt sen perinteisen nimikkeistön tai IUPAC: n.
Reaktiivisuus
Nukleofiilinen hyökkäys
 Nukleofiilinen hyökkäys karbonyyliryhmään. Lähde: Benjah-BMM27 [julkinen alue]
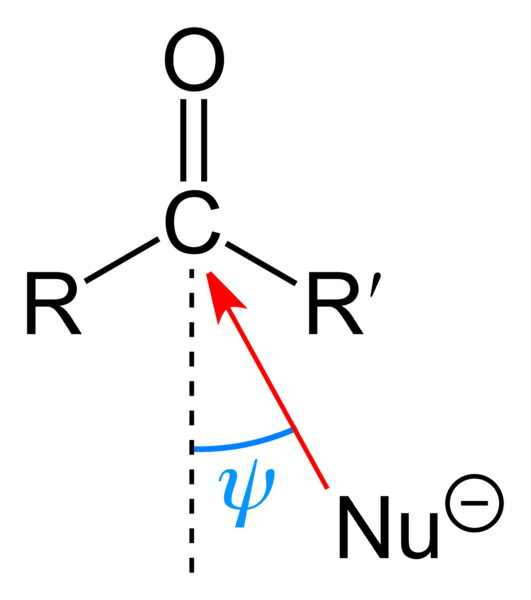
Nukleofiilinen hyökkäys karbonyyliryhmään. Lähde: Benjah-BMM27 [julkinen alue] Yläkuva näyttää karbonyyliryhmän kärsimän nukleofiilisen hyökkäyksen. Nukleofiili, nu-, Se voi olla anioni tai neutraali laji, jolla on käytettävissä olevat elektronit; Kuten ammoniakki, NH3, Esimerkiksi. Tämä näyttää yksinomaan hiileltä, koska resonanssirakenteiden mukaan se on positiivinen osittainen kuorma.
Positiivinen kuorma houkuttelee NU: ta-, joka pyrkii lähestymään ”kyljyä” siten, että substituentit r ja r "on pienin steerinen este,. Riippuen siitä, kuinka tilaa vieviä ne ovat, tai saman NU: n kokoa-, Hyökkäys tapahtuu eri kulmiin ψ; Se voi olla hyvin avoin tai suljettu.
Kun hyökkäys tapahtuu, muodostuu välittäjäyhdiste, nu-cr'-o-; Eli happi pysyy muutaman elektronin kanssa, jotta Nu voi lisätä- karbonyyliryhmään.
Tämä negatiivisesti ladattu happi voi puuttua reaktion muihin vaiheisiin; Protoni hydroksyyliryhmänä, OH, tai vapauta kuin vesimolekyyli.
Voi palvella sinua: Osiokerroin: Jakelu, jakelu, sovelluksetMekanismit, samoin kuin tällä hyökkäyksellä saatujen reaktion tuotteet, ovat hyvin monipuolisia.
Johdannaiset
Nublyic -agentti Nu- Se voi olla monia lajeja. Jokaiselle spesifiselle reagoivaksi karbonyyliryhmän kanssa eri johdannaiset.
Esimerkiksi, kun mainittu nukleofiilinen aine on amiini, NH2A, iminas on kotoisin, r2C = nr; Jos se on hydroksyyliamiinia, NH2Voi, johtaa oksimasiin, rr'c = noh; Jos se on syanidianioni, CN-, Cianohydrinas, RR'C (OH) CN, ja siten muiden lajien kanssa.
Vähennys
Aluksi sanottiin, että tämä ryhmä on happea, ja siksi Rusty. Tämä tarkoittaa, että olosuhteiden vuoksi linkkejä voidaan vähentää tai menettää happiatomia, joka korvaa sen vetyillä. Esimerkiksi:
C = o => ch2
Tämä muutos osoittaa, että karbonyyliryhmä pelkistettiin metyleeniryhmään; Happehäviöstä johtui vetyvahvistusta. Sopivimmissa kemiallisissa termeissä: karbonyyliyhdiste pelkistetään alkaaniksi.
Jos se on cetona, rcor ', hydraracina, h2N-NH2, ja voimakkaasti perusympäristö voidaan vähentää vastaavaan alkaaniinsa; Tämä reaktio tunnetaan nimellä Wolff-Kishner-pelkistys:
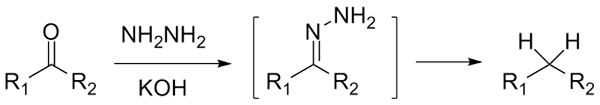 Wolff-Kishnerin vähentäminen. Lähde: Jü [CC0]
Wolff-Kishnerin vähentäminen. Lähde: Jü [CC0] Jos toisaalta reaktioseos koostuu amalgamaatin sinkistä ja suolahaposta, reaktio tunnetaan nimellä Clemmensen -pelkistys:
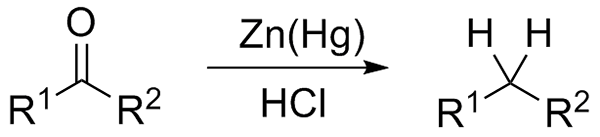 Clemmensenin pelkistys. Lähde: Wikimedia Commons.
Clemmensenin pelkistys. Lähde: Wikimedia Commons.
Asetaali- ja lakkauskoulutus
Karbonyyliryhmä ei voi vain lisätä nukleofiilisiä aineita Nu-, Mutta happoolosuhteissa se voi myös reagoida alkoholien kanssa samanlaisten mekanismien kautta.
Kun aldehydi tai Cetona reagoi osittain alkoholin kanssa, hemiaketaalit tai hemisetaalit ovat peräisin vastaavasti. Jos reaktio suoritetaan kokonaan, tuotteet ovat asetaaleja ja ketaleja. Seuraavat kemialliset yhtälöt tekevät yhteenvedon ja selventävät vasta mainittua:
Rcho + r3Voi g rchoh (tai3) (Hemiaceetaalinen) + R4Voi g rch (tai3) (Tai4) (Asetaali)
RCOR2 + R -3Voi g rcor2(Voi) (tai3) (Hemical) + R4Voi g rcor2(Tai3) (Tai4) (Ketal)
Ensimmäinen reaktio vastaa hemiasetaalien ja asetaalien muodostumista aldehydistä, ja toinen hemisetalleista ja ketonista ketonista.
Nämä yhtälöt eivät ole riittävän yksinkertaisia selittämään näiden yhdisteiden muodostumista; Ensimmäiseen lähestymistapaan aiheeseen riittää kuitenkin ymmärtää, että alkoholit lisätään ja että heidän sivuketjut R (R (R3 ja r4) Ne on kytketty karbonyylihiileen. Siksi tai tai tai tai3 ja tai4 Alkuperäiseen molekyyliin.
Tärkein ero asetaalin ja Ketalin välillä on hiileen kytketty vetyatomin läsnäolo. Huomaa, että ketonista puuttuu tämä vety.
Kaverit
Hyvin samanlainen kuin karbonyyliryhmän nimikkeistöosassa selitetään, sen tyypit perustuvat siihen, mitkä ovat substituentit a ja b tai r ja r '. Siksi on rakenteellisia ominaisuuksia, joilla on sarja karbonyyliyhdisteitä vain järjestyksen tai linkkityypin ulkopuolella.
Esimerkiksi, mainittiin analogian periaate tämän ryhmän ja hiilimonoksidin välillä, C lähelläo. Jos molekyylillä ei ole vetyatomeja ja jos on myös kaksi c = O -naveja, se on sitten hiilioksidi, cnJOMPIKUMPI2. N: lle, joka on yhtä suuri kuin 3, sinulla on:
Voi palvella sinua: IsóbarosO = c = c = c = o
Mikä on kuin hiilellä kaksi C päin -molekyyliä olisi kytketty ja erotettu.
Karbonyyliyhdisteet eivät voi vain johtua CO -kaasusta, vaan myös hiilihapposta, H2Yhteistyö3 tai OH- (c = o) -OH. Täällä kaksi OH edustavat r ja r ', ja korvataan jommankumman niistä tai niiden vetyjä, hibonihappojohdannaiset saadaan.
Ja sitten on karboksyylihappojen johdannaisia, RCOOH, saatu muuttamalla R -identiteettejä tai korvaamalla H toisella atomilla tai ketjulla R '(joka aiheuttaisi esteriä, rcoor')).
Kuinka tunnistaa se aldehydoissa ja ketoneissa
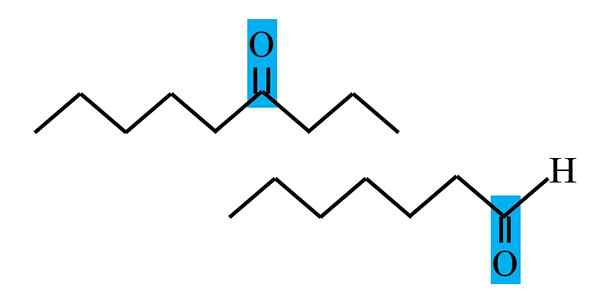 Ketonin ja aldehydin erottelu rakenteellisesta kaavasta. Lähde: Gabriel Bolívar.
Ketonin ja aldehydin erottelu rakenteellisesta kaavasta. Lähde: Gabriel Bolívar. Sekä aldehydoilla että ketoneilla on yhteinen karbonyyliryhmän läsnäolo. Sen kemialliset ja fysikaaliset ominaisuudet johtuvat siitä. Niiden molekyyliympäristöt eivät kuitenkaan ole yhtä suuret molemmissa yhdisteissä; Entisessä hän on terminaaliasennossa ja sekunneissa, missä tahansa ketjussa.
Esimerkiksi ylemmässä kuvassa karbonyyliryhmä on sinertävän laatikon sisällä. Ketoneissa tämän laatikon vieressä on oltava toinen hiili- tai ketjusegmentti (ylösalaisin); Aldehydeissä voi olla vain vetyatomia (alla).
Jos C = O on ketjun toisessa päässä, se on aldehydi; Se on suorin tapa erottaa se Cetonasta.
Henkilöllisyystodistus
Mutta miten tietää kokeellisesti, jos tuntematon yhdiste on aldehydi tai ketoni? Spektroskooppisia (infrapunasäteilyn absorptio, IR) tai orgaaniset laadulliset testit ovat lukuisia menetelmiä.
Laadullisten esseiden osalta nämä perustuvat reaktioihin, että positiivisen annettaessa analyytikko tarkkailee fyysistä vastetta; Värimuutos, lämmön vapautus, kuplan muodostuminen jne.
Esimerkiksi näytteen lisääminen k: n happoliuos2Cr2JOMPIKUMPI7 Aldehydi muuttuu karboksyylihapoksi, mikä tekee liuoksen väristä vaihtamaan oranssista vihreäksi (positiivinen testi). Samaan aikaan ketonit eivät reagoi, ja siksi analyytikko ei havaitse mitään värimuutosta (negatiivinen testi).
Toinen tutkimus on käyttää Tollens -reagenssia [AG (NH3-A2-+, niin, että aldehydi vähentää kationien AG: tä+ metallihopeaksi. Ja tulos: Hopeapeilin muodostuminen koeputken alaosaan, johon näyte asetettiin.
Tärkeimmät esimerkit
Lopuksi luetellaan sarja karbonyyliyhdisteistä:
-CH3COOH, etikkahappo
-HCOOH, muurahaishappo
-CH3Kokki3, Propanona
-CH3Kokki2CH3, 2-butanoni
-C6H5Kokki3, asefenoni
-CH3Cho, etanal
-CH3CH2CH2CH2Pentanal
-C6H5Cho, bentsaldehydi
-CH3Conh2, asetamidi
-CH3CH2CH2Keittää3, Propyyliasetaatti
Nyt, jos mainitaan esimerkkejä yhdisteistä, joilla yksinkertaisesti hallussaan on tämä ryhmä, luettelo olisi melkein loputon.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5. painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. Amiini. (10. painos.-A. Wiley Plus.
- Reid Danielle. (2019). Karbonyyliryhmä: Ominaisuudet ja yleiskatsaus. Opiskelu. Toipunut: Opiskelu.com
- Sharleen Agvateesiri. (5. kesäkuuta 2019). Karbonyyliryhmä. Kemian librettexts. Palautettu: Chem.Librettexts.org
- Wiki Kids Ltd. (2018). Karbonyyliyhdisteet. Palautettu: yksinkertaisesti.Tiede
- Toppr. (S.F.-A. Karbonyyliryhmän nimikkeistö ja rakenne. Toipunut: Toppr.com
- Clark j. (2015). Aldehydien ja ketonien hapettuminen. Talteenotettu: Chemguide.yhteistyö.Yhdistynyt kuningaskunta

