Guanina -ominaisuudet, rakenne, koulutus ja toiminnot
- 4991
- 948
- Arthur Terry II
Se Guanina Se on typpipohja, joka palvelee 5'-monofosfaatin guanilaatin biosynteesiä. Molemmat aineet ovat vastaavasti osa RNA: ta ja DNA: ta, jotka tallentavat solujen geneettiset tiedot.
Ribonukleiinihappo (RNA) ja deoksiribonukleiinihappo (DNA) muodostuu nukleotideilla, jotka muodostuvat sokeriin ja fosfaattiryhmään kiinnittyneellä typpipohjalla ja fosfaattiryhmällä.
 Lähde: Neurotoger [julkinen alue]
Lähde: Neurotoger [julkinen alue] Guaniini, joka on osa nukleiinihappoja, osallistuu monofosfaatissa, difosfaatissa ja kolmifaasin nukleosideissa (GMP, BKT ja GTP), kuten energian aineenvaihdunta, solunsisäisen signaalin translaatio, valoreseptoreiden fysiologia ja vesiklerien fuusio.
[TOC]
Kemiallinen rakenne
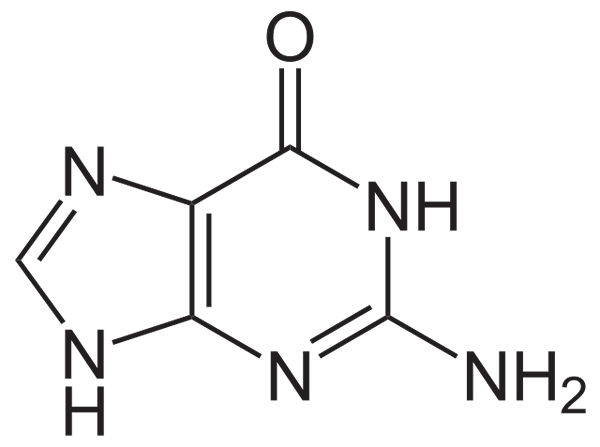
Guaniinin kemiallinen rakenne (2-amino-6-hydroksipuriini) on heterosyklinen puriinirengas, joka koostuu kaksirenkaasta United: Yksi rengas on pyrimidiini ja toinen rengas on imidatsoli.
Guaniinin heterosyklinen rengas on litteä ja joillakin kaksoiskonjugaattiyhteyksillä. Lisäksi sillä on kaksi tautomeeristä muotoa, keto ja enolmuoto, ryhmien C-1 ja N-6 välillä.
Ominaisuudet
Guaniinin ominaisuudet ovat seuraavat:
- Guaniini on apolaarinen aine. Se on liukenematon veteen, mutta se liukenee happojen tiivistettyihin liuoksiin tai vahvoihin emäksiin.
- Se voidaan eristää valkoisena kiinteänä aineena, empiirisellä kaavalla C5H5N5Tai ja molekyylipaino 151,3 g/mol.
- Valon absorboiva ominaisuus 260 nm DNA: sta johtuu osittain guaniinin kemiallisesta rakenteesta.
- DNA: ssa guaniini muodostaa kolme vety sidosta. Karbonyyli C-6-ryhmä on vetyyhteyshenkilö, N-1-ryhmä ja C-2 Amino -ryhmä ovat vety sidosluovuttajia.
Tästä syystä tarvitaan enemmän energiaa yhteyden katkaisemiseksi guaniinin ja sytosiinin välillä kuin adeniinin, jolla on Timin, koska jälkimmäinen vääntömomentti yhdistää vain kaksi vety sillaa.
Voi palvella sinua: elektroforeesi: perusta, tekniikka, mihin se on, esimerkkejä- Solussa se on aina osa nukleiinihappoja tai GMP: tä, BKT: tä ja GTP: tä, ei koskaan vapaassa muodossaan.
Biosynteesi
Guaniinimolekyyli, kuten muutkin puriinit, syntetisoidaan Novo 5-fosoribosyyli-1-pyrofosfaatin (PRPP) alkaen entsyymi katalysoiduilla reaktioilla.
Ensimmäinen askel koostuu aminoryhmän lisäämisestä glutamiinista PRPP: hen ja muodostaa 5-fosforibosyyliamiinin (PRA).
Myöhemmin järjestyksessä glysiinin, aspartaatin, glutamiinin, muodostumisen ja hiilidioksidin lisääminen PRA: han lisää. Tällä tavoin muodostetaan inosina 5'-monofosfaatti (IMP), nimeltään inosina 5'-monofosfaatti.
Tämän prosessin aikana käytetään ATP-hydrolyysin vapaata energiaa (adenosiini 5'-triffosfaattia), joka tuottaa ADP: tä (adenosiini 5'-Diaphypho) ja PI (epäorgaaninen fosfaatti).
Imponden hapettuminen nad: lle+ (Nikotiinamidi ja adeniinin dinukleotidi), tuottaa xantine 5'-monofosfaattia (XMP). Myöhemmin aminoryhmän lisääminen XMP: hen tuottaa guanilaato -molekyylin.
Guanilaato -biosynteesin säätely suoritetaan alussa, kun PRA muodostuu, ja lopulta, kun IMPE: n hapettuminen tapahtuu. Säätely tapahtuu negatiivisen palautteen kautta: GMP -nukleotidi estää entsyymejä molemmissa vaiheissa.
Nukleotidien metabolisen hajoamisen aikana typpipohjat kierrätetään. GMP muodostuu hypoksantiini-keepeeniinentsyymifosforibosyylitransferaasilla siirtämällä fosribosyyliryhmää PRPP: stä guaniiniin.
Funktio
Koska guaniinia ei löydy vapaasta muodossaan, sen toiminnot liittyvät GMP: hen, BKT: hen ja GTP: hen. Jotkut heistä mainitaan alla:
- 5'-triffosfaatti (GTP) guanosiini toimii vapaana energiasäiliönä. GTP-fosfaattiryhmä voidaan siirtää adenosiini 5'-trifosfaattiin (ADP), ATP: n muodostamiseksi. Tämä reaktio on palautuva, ja sitä katalysoi nukleosididifosfaattikinaasi.
Voi palvella sinua: Beeta -galaktosidaasi: Ominaisuudet, rakenne, toiminnot- GMP on guaninaan sisältävän nukleotidin vakain muoto. Hydrolyysin kautta GMP -muodossa GMP -syklinen (GMPC), joka on toinen lähettiläs solunsisäisten opasteiden aikana, käännösteillä. Esimerkiksi fooreseptori- ja kemioreseptorisoluissa.
- GMPC osallistuu sileän lihaksen verisuonten rentoutumiseen typpioksidin biosynteesin aikana endoteelisoluissa.
- GTP -gammafosfaatti -hydrolyysi toimii vapaana energialähteenä proteiinien biosynteesille ribosomeissa.
- Helikaasientsyymit tarvitsevat GTP -hydrolyysin vapaan energian kaksinkertaisen DNA -potkurin erottamiseksi DNA: n replikaation ja transkription aikana.
- Hippokampuksen hermosoluissa jännitteen riippuvaisten natriumkanavien vaikutusta säätelee GTP -hydrolyysi BKT: hen.
Liittyvät sairaudet
Korkeat veritasot ja virtsahappo- ja virtsa on liitetty kolmeen erilaiseen aineenvaihduntavaurioon, jotka näemme alla.
Lesch-Nyehan-oireyhtymä
Sille on ominaista HPRT-puute (hypoksantiini-guaddibosyylitransferaasi), tärkeä entsyymi hypoksaniinin ja guaniinin kierrättämiseksi. Tässä tapauksessa se lisää PRPP -tasoja eikä muodosta IMP: tä ja GMP: tä, alkuperäisen purinisynteesivaiheen kaksi tärkeää säätelijää. Kaikki tämä suosii biosynteesiä Novo Puriineista.
PRPP -aktiivisuus lisäsi syntaasia
Tämä tuottaa PRPP -tasoja. Tämä metaboliitti toimii gutamiini-prpp-amidotranferaasin aktivaattorina, joka vastaa 5-fosforibosyllamiinin synteesistä, lisäämällä biosynteesiä Novo puriinit.
Voi palvella sinua: Sphingomyeline: Mikä on, rakenne, toiminnot, synteesiVon Gierken oireyhtymä
Se on tauti, joka liittyy tyypin I glykogeenin varastointiin. Tästä oireyhtymästä kärsivillä potilailla on viallinen 6-fosfataasi-glukoosi. Tämä tuottaa 6-fosfaattien glukoositasojen nousun, joka palvelee 5-fosfaattiriboosin synteesiä pentoosifosfaatin kautta.
5-fosfaatti-riboosi on aloitusmetaboliitti PRPP-biosynteesille. Samoin kuin kaksi edellistä tapausta, tämä johtaa biosynteesin lisääntymiseen Novo Puriineista.
Verenhapon lisääntyminen veressä ja virtsassa aiheuttaa oireita, jotka tunnetaan yleisesti kihti. Lesch Nyhanin oireyhtymän tapauksessa potilailla puuttuu täysin HPRP -entsyymin aktiivisuus, mikä johtaa muiden oireiden ilmenemiseen, jotka sisältävät halvaantumisen ja henkisen vajauksen.
HPRP -geeni löytyy X -kromosomista. Siksi tämän geenin mutaatiot vaikuttavat miehiin. Neurologisten ongelmien hoitamiseksi ei ole hoitoa. Virtsahapon lisääntymiseen liittyvät oireet hoidetaan allopurinolilla.
Viitteet
- Dawson, R. et al. 1986. Tiedot biokemiallisesta tutkimuksesta. Clarendon Press, Oxford.
- Horton, R; Moran, L; Scrimgeour, G; Perry, m. Ja rawn, d. 2008. Biokemian periaatteet. 4. painos. Pearson -koulutus.
- Mathews, Van Holde, Ahern. 2001. Biokemia. 3. painos.
- Murray, R; Granner, D; Mayes, P. Ja Rodwell, V. 2003. Harperin kuvitettu biokemia. 26. painos. McGraw-Hill -yritykset.
- Nelson, DL ja Cox, M. 1994. Lehninger. Biokemian periaatteet. 4. painos. Ed Omega.
- Sigma-Aldrich. 2019. Guaniinikemiallinen arkki. Word Wide Web -osoite: Sigmaaldrich.com.

