Hafnium

- 4153
- 865
- Gustavo Runte DVM
 Metallinen hafnio -näyte. Lähde: Hi-Res-kuvat kemiallisista elementeistä [CC by (https: // creativecommons.Org/lisenssit/by/3.0)]
Metallinen hafnio -näyte. Lähde: Hi-Res-kuvat kemiallisista elementeistä [CC by (https: // creativecommons.Org/lisenssit/by/3.0)] Mikä on hafnio?
Hän hafnium Se on siirtymämetalli, jonka kemikaali on HF ja jonka atomismäärä on 72. Se on jaksollisen taulukon ryhmän 4 kolmas elementti, joka on kongeeni titaanissa ja ruumiissa. Jälkimmäisen kanssa sillä on monia kemiallisia ominaisuuksia, jotka sijaitsevat yhdessä maapallon kuoren mineraaleissa.
Hafnio -etsiminen etsii missä zirkoniumia, koska se on sen uuttotuote. Tämän metallin nimi tulee latinalaisesta sanasta 'hafnia', jonka merkitys on Kööpenhaminan nimi, kaupunki, josta se löydettiin zirkonin mineraaleista ja kiista päättyi sen todelliseen kemialliseen luonteeseen.
Tämä metalli tekee eron siitä, että se on viimeinen stabiilimmista elementeistä, jotka on löydetty täällä maan päällä; Eli muut löytöt ovat muodostaneet sarjan ultrapesadoja, radioaktiivisia ja/tai keinotekoisia isotooppeja.
Hafnio -yhdisteet ovat analogisia titaani- ja sironiumin kanssa, pääosin +4 hapettumisluku, kuten HFCL4, HFO2, HFI4 ja hfbr4. Jotkut heistä johtavat luettelon kaikkien aikojen luotuista tulenkestävistä materiaaleista sekä suuren lämpövastuksen seoksista ja toimii myös erinomaisina neutronien absorbentteina.
Tästä syystä Hafniolla on paljon osallistumista ydinkemiaan, etenkin painevesireaktoreihin.
Löytö
Siirtymämetalli tai harvinaiset maametallit
Hafnion löytöä ympäröivät kiistat, vaikka sen olemassaolon ennustettiin jo vuodesta 1869 lähtien Mendeleevin jaksollisen taulukon ansiosta.
Ongelmana oli, että se sijoitettiin zirkoniumin alle, mutta se tapahtui samanaikaisesti harvinaisten maametallien elementtien samana ajanjaksona: Lantanoides. Tuolloin kemistit eivät tienneet, oliko se siirtymämetallia vai metallia harvinaisista maametallista.
 99,9% Hafnium Bar. Lähde- Alchemist-HP (www.Pse-Mendelejew.), cc by-Sa 2.0, Wikimedia Commons
99,9% Hafnium Bar. Lähde- Alchemist-HP (www.Pse-Mendelejew.), cc by-Sa 2.0, Wikimedia Commons Ranskalainen kemisti Georges Urbain, Luthacion löytäjä, Hafnion naapurimaiden metalli, kertoi vuonna 1911 löytäneensä elementin 72, jonka Celtio kutsui ja julisti, että se oli harvinaisten maametallien metalli. Mutta kolme vuotta myöhemmin pääteltiin, että sen tulokset olivat vääriä ja että se oli vain eristänyt sekoituksen Lantanoides.
Vasta kun elementit tilattiin niiden atomilukujen perusteella, Henry Moseleyn työn ansiosta vuonna 1914, Luthaten ja elementin 72 välinen naapurusto oli todiste sama ryhmä kuin titaani- ja kiertometallit ja ympäröivä metallit.
Voi palvella sinua: Flokkulaatio: Reaktio, tyypit, sovellukset, esimerkitKööpenhaminan havaitseminen
Vuonna 1921 Niels Bohrin atomirakenteen ja sen ennusteen X -raynemissiospektrin tutkimuksen jälkeen elementti 72: lle tämä metalli pysäytettiin harvinaisten maametallien mineraaleissa; Ja sen sijaan hänen haku Circonium Minerals -yrityksistä, koska molempien elementtien piti jakaa useita kemiallisia ominaisuuksia.
Tanskalainen kemisti Dirk Coster ja unkarilainen kemisti Georg Von Hevesy vuonna 1923 tunnustivat lopulta Niels Bohrin ennustetun spektrin Norjan ja Grönlannin zirkoninäytteissä. Saatuaan löytön Kööpenhaminassa, he kutsuivat elementtiä 72 tämän kaupungin latinalaisen nimen mukaan: Hafnia, joka myöhemmin johdettiin 'Hafnio'.
Eristys ja tuotanto
Se ei kuitenkaan ollut helppo tehtävä. Vaikka vuonna 1924 menetelmä suunniteltiin murto -uudelleenkiteyttämisellä Hafnio -tetrakloridin saamiseksi, HFCL4, Se oli Alankomaiden kemikaalien Anton Eduard Van Arkel ja Jan Hendrik de Boer, jotka vähensivät hänet metalliselle hafniumille.
Tätä varten HFCL4 Se tehtiin pelkistys metallimagnesiumin avulla (Kroll Process):
Hfcl4 + 2 mg (1100 ° C) → 2 mgcl2 + HF
Toisaalta aloittaen Hafnio Tetrayoduro, HFI4, Tämä höyrystettiin kärsimään lämpöhajoamisesta hehkulamppulla volframihahlan, jolle metallinen hafnium kerrostettiin aiheuttamaan monikiteisen ulkonäköpalkin (kiteinen palkkiprosessi tai arkel-boer-prosessi):
HFI4 (1700 ° C) → HF + 2 I2
Hafnio -rakenne
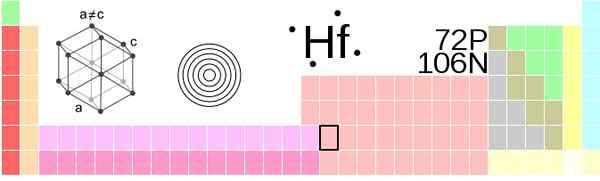 Hafnio -sijainti jaksollisessa taulukossa. Suihkulähde: !Alkuperäinen: AhoTeseierVector: Sushant Savla, CC BY-SA 3.0, Wikimedia Commons
Hafnio -sijainti jaksollisessa taulukossa. Suihkulähde: !Alkuperäinen: AhoTeseierVector: Sushant Savla, CC BY-SA 3.0, Wikimedia Commons Hafnio, HF -atomit, on ryhmitelty ympäristön paineeseen kompaktiin kuusikulmainen rakenteen kide, HCP, aivan kuten titaani- ja zirkoniummetallit tekevät. Tästä Hafnio HCP -kiteestä tulee sen a -faasi, joka pysyy vakiona vuoteen 2030 K: n lämpötilaan, kun se kärsii siirtymisestä β -faasiin, kuutiorakenteen keskittymisellä kehossa, BCC, BCC.
Tämä ymmärretään, jos lämpö "rentoutuu" lasia otetaan huomioon, ja siksi HF -atomit pyrkivät sijoittamaan itsensä siten, että heidän tiivistymisensä vähenee. Nämä kaksi vaihetta ovat riittävät ottamaan huomioon hafniumin polymorfismi.
Siinä on myös polymorfismi, joka riippuu korkeista paineista. Α- ja β -faasit esiintyvät 1 atm: n paineessa; Vaikka ω, kuusikulmainen, mutta vieläkin tiivistynyt vaihe kuin tavallinen HCP, ilmestyy, kun paineet ylittävät 40 GPA: ta. Mielenkiintoista on, että kun paineet kasvavat edelleen, β -faasi ilmestyy uudelleen, vähiten tiheä.
Voi palvella sinua: SeleenHydric Acid (H2SE): Mikä on, rakenne, ominaisuudet, käyttötarkoituksetHafnio -ominaisuudet
Fyysinen ulkonäkö
Hopeavalkoinen kiinteä aine, joka näyttää tummat sävyt, jos siinä on kerros oksidia ja nitridiä.
Moolimassa
178,49 g/mol
Sulamispiste
2233 ºC
Kiehumispiste
4603 ºC
Tiheys
Huoneenlämpötilassa: 13,31 g/cm3, on kahdesti tiheämpi kuin ympyrä
Aivan sulamispisteessä: 12 g/cm3
Sulamislämpö
27,2 kJ/mol
Höyrystyslämpö
648 kJ/mol
Elektronegatiivisuus
1.3 Pauling -asteikolla
Ionisaatioenergiat
Ensimmäinen: 658,5 kJ/mol (HF+ kaasumainen)
Toinen: 1440 kJ/mol (HF2+ kaasumainen)
Kolmas: 2250 kJ/mol (HF3+ kaasumainen)
Lämmönjohtokyky
23,0 W/(M · K)
Sähkövastus
331 nω · m
Mohsin kovuus
5.5
Reaktiivisuus
Ellei metalli ole pulaa ja palovammoja, ampumalla kipinöitä lämpötilassa 2000 ºC, sillä ei ole alttiutta hapettaa tai ajaa, koska sen oksidin ohut kerros suojaa sitä. Tässä mielessä se on yksi vakaimmista metalleista. Itse asiassa hapot tai vahvat emäkset voivat liuottaa sen; Lukuun ottamatta fluoriarhorihappoa ja halogeenit, jotka kykenevät hapettamaan sen.
Elektroninen kokoonpano
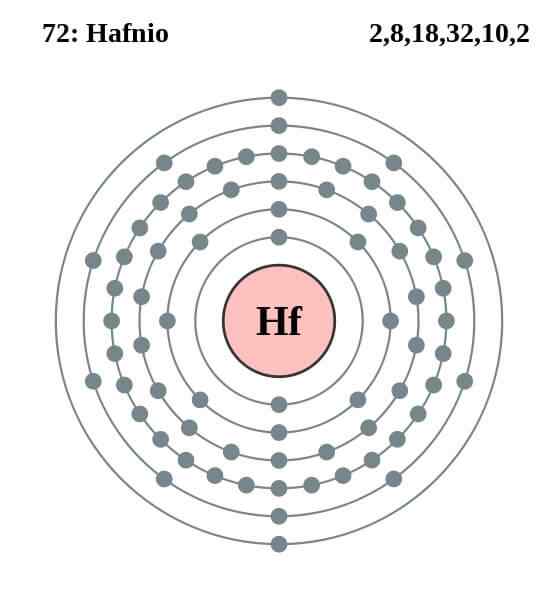 Hafnio -elektroninen kokoonpano
Hafnio -elektroninen kokoonpano Hafnion atomilla on seuraava elektroninen kokoonpano:
[Xe] 4f14 5 D2 6s2
Tämä on samaan aikaan tosiasian, joka kuuluu jaksollisen taulukon ryhmään 4, yhdessä titaanin ja sironiumin kanssa, koska siinä on neljä Valencia -elektronia 5D- ja 6S -kiertoradalla. Huomaa, että Hafnio ei voinut olla lantanoidi, koska sillä on täysin täydet 4F -kiertoradat.
Hapetusluvut
Sama elektroninen kokoonpano paljastaa kuinka monta elektronia pystyy menettämään hafnio -atomin, kun se on osa yhdistettä. Olettaen, että hän menettää neljä Valencia -elektronia, hän olisi tetravalenttinen kationi HF4+ (Analogisesti sinulle4+ ja Zr4+), Ja siksi olisi hapettumismäärä +4.
Tämä on itse asiassa vakain ja yleisin sen hapetuslukuista. Muita vähemmän merkityksellisiä ovat: -2 (HF2-), +1 (HF+), +2 (HF2+) ja +3 (HF3+-A.
Isotoopit
Hafnio esitetään maapallolla viidellä vakaalla isotooppina ja radioaktiivisena, jolla on erittäin suuri elämänaika:
-174HF (0,16%, puoli -elämä 2,10viisitoista vuosia, joten sitä pidetään käytännössä vakaana)
-176HF (5,26%)
-177HF (18,60%)
Voi palvella sinua: Heikot perusteet-178HF (27,28%)
-179HF (13,62%)
-180HF (35,08%)
Huomaa, että sellaista isotooppia ei ole sellainen, joka erottuu runsaasti, ja tämä heijastuu Hafnion keskimääräisessä atomimassassa, 178.49 Uma.
Kaikista Hafnion radioaktiivisista isotoopeista, jotka yhdessä alkuperäiskansojen kanssa yhteensä 34, 178m2HF on kiistanalaisin, koska radioaktiivisessa rappeutumisessa vapauttaa gammasäteilyä, joten näitä atomeja voitaisiin käyttää sodan aseena.
Käyttää/sovelluksia
 Hafnio peitetty ohuella oksidikerroksella. Lähde: Alchemist-HP (Talk) (www.Pse-Mendelejew.De), Fal, Wikimedia Commons
Hafnio peitetty ohuella oksidikerroksella. Lähde: Alchemist-HP (Talk) (www.Pse-Mendelejew.De), Fal, Wikimedia Commons Ydinreaktiot
Hafnio on kosteuden resistentti metalli ja korkeat lämpötilat sen lisäksi, että se on erinomainen neutronien absorboiva. Tästä syystä sitä käytetään painevesireaktoreissa, samoin kuin ydinreaktorien hallitsevien palkkien valmistuksessa, joiden pinnoitteissa ne on valmistettu Ultrapuro Circuista.
Seokset
Hafnio -atomit voivat integroida muut metallikiteitä erilaisten seosten aiheuttamiseksi. Niille on ominaista olla sitkeitä ja lämpökestävää, joten ne on tarkoitettu alueellisiin sovelluksiin, kuten rakettien moottorin suuttimien rakentamisessa.
Toisaalta joillakin seoksilla ja kiinteillä Hafnio -yhdisteillä on erityisiä ominaisuuksia; kuten heidän Carbides ja Nitturos, HFC ja HFN, jotka ovat erittäin tulenkestävää materiaalia. Tantalo ja Hafnio Carbide, TA4HFC5, Fuusiopiste on 4215 ºC, se on yksi kaikkien aikojen tunnetuimmista materiaaleista.
Katalyysi
Hafnion metalloseenejä käytetään orgaanisina katalyytteinä polymeleenisynteesille, kuten polyeteeni ja polystyreeni.
Riskejä
Tähän mennessä ei ole tietoa, mitä vaikutuksia HF -ioneilla voi olla kehomme4+. Toisaalta, koska niitä löytyy luonnosta zirkonium -mineraaleissa, ei uskota, että he saavat muuttaa ekosysteemiä suolojensa vapauttamiseksi ympäristöön.
Nyt on suositeltavaa manipuloida HAFNIO -yhdisteitä huolellisesti, ikään kuin ne olisivat myrkyllisiä, vaikka ei olisi lääketieteellisiä tutkimuksia, jotka todistaisivat, että ne ovat haitallisia terveydelle.
Hafnion todellinen vaara sijaitsee sen hienoksi jauhon kiinteiden hiukkasten hiukkasissa, jotka voivat polttaa juuri silloin, kun ne joutuvat kosketuksiin ilman hapen kanssa.
Tämä selittää miksi, kun se on kiillotettu, toiminta, joka raaputtaa pinnan ja antaa puhtaita metallihiukkasia, palavat kipinät vapautuvat lämpötilan ollessa 2000 ºC; toisin sanoen Hafnio esittelee pyroporisisuutta, ainoa omaisuus, joka aiheuttaa tulipalon tai vakavia palovammoja.

