Molaarinen massa miten se lasketaan, esimerkit ja harjoitukset ratkaistu
- 980
- 81
- Arthur Terry II
Se Moolimassa Se on intensiivinen aineen ominaisuus, joka liittyy MOL: n käsitteen massamittauksiin. Koska se on tiiviimpi, se on massa, joka vastaa aineen moolia; eli se, mikä "painaa" Avogadro -numero (6.022 · 1023) tiettyjen hiukkasten.
Yksi mooli minkä tahansa aineesta sisältää saman määrän hiukkasia (ionit, molekyylit, atomit jne.) Sen massa kuitenkin vaihtelee, koska sen molekyylin mitat määritetään sen rakenteen muodostavien atomien ja isotooppien lukumäärän perusteella. Mitä enemmän massaa atomi tai molekyyli, sitä suurin sen molaarinen massa.
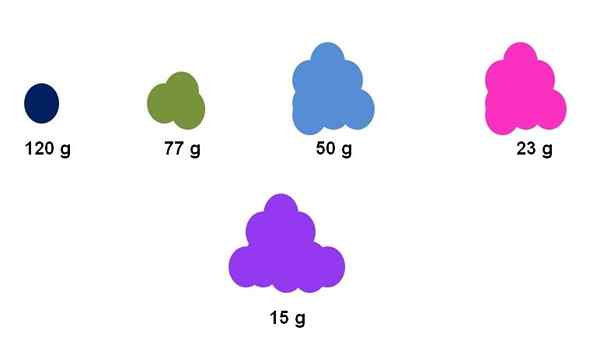
 Eri aineiden molaarimassojen välinen ero voidaan pinnallisesti huomata niiden näytteen ilmeinen määrä. Lähde: Gabriel Bolívar.
Eri aineiden molaarimassojen välinen ero voidaan pinnallisesti huomata niiden näytteen ilmeinen määrä. Lähde: Gabriel Bolívar. Oletetaan esimerkiksi, että tarkalleen yksi mol tapaa viisi erilaista yhdistettä (ylivoimainen kuva). Tasapainoa käyttämällä taikina on mitattu jokaiselle klusterille, joka on ilmaistu alla. Tämä massa vastaa molaarista taikinaa. Kaikista niistä violetti yhdiste on kevyempien hiukkasten kanssa, kun taas tummansininen yhdiste, raskaimmat hiukkaset.
Huomaa, että esitetään yleinen ja liioiteltu taipumus: mitä suurempi molaarimassa, sitä pienempi näytteen määrä on sijoitettava tasapainoon. Tämä ainetilavuus riippuu kuitenkin myös suuresti kunkin yhdisteen aggregaatiotilasta ja sen tiheydestä.
[TOC]
Kuinka molaarinen taikina lasketaan?

Määritelmä
Molaarimassa voidaan laskea sen määritelmästä: Massan määrä ainetta kohden:
M = aineen grammat /mol
Itse asiassa g/mol on yksikkö, jossa molaarimassa yleensä ilmenee, kg/mol vieressä. Siten, jos tiedämme kuinka monta moolia meillä on yhdisteestä tai elementistä, ja punnitsemme sen, saavutamme sen molaarimassan, joka käyttää yksinkertaista jakoa.
Voi palvella sinua: Justus von LiebigKohteet
Molaarimassa ei koske vain yhdisteitä, vaan myös elementtejä. Moolien käsite ei syrjitä ollenkaan. Siksi asetamme jaksollisen taulukon avulla suhteelliset atomimassat kiinnostavalle elementille ja kerrotaan sen arvo 1 g/mol; Tämä on Avogadron vakio, MTAI.
Esimerkiksi strontiumin suhteellinen atomimassa on 87,62. Jos haluamme sen atomimassan, se olisi 87,62 UMA: ta; Mutta jos etsimme sen molaarimassaa, niin se on 87,62 g/mol (87,62 · 1 g/mol). Ja niin, kaikkien muiden elementtien molaarimassa saadaan samalla tavalla edes tekemättä tällaista kertolaskua.
Yhdisteet
Yhdisteen molaarimassa ei ole muuta kuin sen atomien suhteellisten atomimassojen summa kerrottuna MTAI.
Esimerkiksi vesimolekyyli, H2Tai siinä on kolme atomia: kaksi vetyä ja yksi happea. H: n ja O: n suhteelliset atomimassat ovat vastaavasti 1 008 ja 15 999. Siten lisäämme sen massat kertomalla yhdisteen molekyylissä esiintyvällä atominumerolla:
2 H · (1,008) = 2 016
1 O · (15 999) = 15 999
M(H2O) = (2 016 + 15 999) · 1 g/mol = 18 015 g/mol
On melko yleinen käytäntö jättää pois MTAI lopussa:
M(H2O) = (2 016 + 15 999) = 18 015 g/mol
Ymmärretään, että molaarisella taikinalla on yksiköitä g/mol.
Esimerkit
Yksi tunnetuimmista molaarimassista on juuri mainittu: vesi, 18 g/mol. Ne, jotka tuntevat nämä laskelmat, saavuttavat pisteen, jossa he kykenevät muistamaan joitain molaarimassoja etsimättä niitä tai laskemalla niitä, kuten tehtiin. Jotkut näistä molaarimassoista, jotka toimivat esimerkkeinä, ovat seuraavat:
Se voi palvella sinua: terveyskemian edut ja haitat-JOMPIKUMPI2: 32 g/mol
-N2: 28 g/mol
-Nh3: 17 g/mol
-CH4: 16 g/mol
-Yhteistyö2: 44 g/mol
-HCL: 36,5 g/mol
-H2Sw4: 98 g/mol
-CH3COOH: 60 g/mol
-Usko: 56 g/mol
Huomaa, että annetut arvot ovat pyöristettyjä. Tarkempia tarkoituksia varten molaarimassat, joilla on enemmän desimaalia.
Ratkaisut
Harjoitus 1
Analyyttisten menetelmien avulla arvioitiin, että näytesäyttö sisältää analyytin 0,0267 moolia. On myös tiedossa, että sen massa vastaa 14% näytteestä, jonka kokonaismassa on 76 grammaa. Laske väitetyn analyytin d moolimassa.
Meidän on määritettävä liuokseen liuenneen D -massa. Jatkamme:
Massa (d) = 76 g · 0,14 = 10,64 g d
Toisin sanoen laskemme 14% näytteen 76 grammasta, jotka vastaavat analyytin d grammia. Sitten, ja lopuksi, käytämme molaarimassan määritelmää, koska meillä on riittävästi tietoja sen laskemiseksi:
M(D) = 10,64 g d/ 0,0267 moolia d
= 398,50 g/mol
Mikä kääntää: Yksi mol (6.022 · 1023) Ja on massa, joka on yhtä suuri kuin 398,50 grammaa. Tämän arvon ansiosta voimme tietää, kuinka paljon ja haluamme punnita tasapainon, jos haluamme esimerkiksi valmistaa liuos molaaripitoisuudesta 5,10-3 M; toisin sanoen liuottaa 0,1993 grammaa ja litraa liuotinta:
5 · 10-3 (mol/l) · (398,50 g/mol) = 0,1993 g ja
Harjoitus 2
Laske sitruunahapon molaarimassa tietäen, että sen molekyylinen kaava on c6H8JOMPIKUMPI7.
Sama kaava C6H8JOMPIKUMPI7 Se helpottaa laskelman ymmärrystä, koska se kertoo meille kerran C: n, h: n ja tai tai että sitrushappossa on atomien lukumäärä. Siksi toistamme saman veden tehdyn vaiheen:
Voi palvella sinua: Dodecil -natriumsulfaatti (SDS): rakenne, ominaisuudet, käyttötarkoitukset6 C · (12 0107) = 72 0642
8 H · (1,008) = 8 064
7 o · (15 999) = 111 993
M(sitruunahappo) = 72 0642 + 8,064 + 111 993
= 192 1212 g/mol
Harjoitus 3
Laske pentahydraattien kuparisulfaatin, cuo, molaarinen taikina4· 5H2JOMPIKUMPI.
Tiedämme ennen kuin vesimassa on 18 015 g/mol. Tämän tarkoituksena on yksinkertaistaa laskelmia, koska jätämme sen pois tällä hetkellä ja keskitymme CuO: n vedettömään suolaan4.
Meillä on, että kuparin ja rikin suhteelliset atomimassat ovat vastaavasti 63 546 ja 32 065. Näiden tietojen avulla jatkamme samalla tavalla kuin harjoituksella 2:
1 cu · (63 546) = 63 546
1 S · (32 065) = 32 065
4 O · (15 999) = 63 996
M(Cuso4) = 63 546 + 32 065 + 63 996
= 159 607 g/mol
Mutta olemme kiinnostuneita pentahydraattisuolan molaarisesta taikinasta, ei vedonlyönnistä. Tätä varten meidän on lisättävä tulos vastaava veden massa:
5 h2O = 5 · (18 015) = 90,075
M(Cuso4· 5H2O) = 159 607 + 90,075
= 249 682 g/mol
Viitteet
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Wikipedia. (2020). Moolimassa. Haettu: vuonna.Wikipedia.org
- Nissa Garcia. (2020). Mikä on molaarinen massa? Määritelmä, kaava ja tentit. Opiskelu. Toipunut: Opiskelu.com
- DR. Kristy M. Bailey. (S.F.-A. Stoikiometria -opetusohjelma
Molaarimassan löytäminen. Haettu: OCC.Edu - Helmestine, Anne Marie, PH.D -d. (2. joulukuuta 2019). Molaarimassan esimerkki ongelma. Toipunut: Admingco.com
- « Darmstadtio -löytö, rakenne, ominaisuudet, käytöt
- Vesi- tai hydrologiset syklivaiheet ja merkitys »

