Metilamiinirakenne, ominaisuudet, tuotanto, käyttö
- 2080
- 508
- Joshua Emmerich
Se Metilamiini Se on orgaaninen yhdiste, jonka tiivistetty kaava on CHO3Nh2. Erityisesti se on kaikkien yksinkertaisin ensisijainen alkyamiini, koska se sisältää vain alquilic-substituentin, joka on sama kuin sanoen, että on vain yksi C-N-kovalenttinen linkki.
Normaaliolosuhteissa se on ammoniakkikaasu, joka haisee kalalta, mutta se on suhteellisen helppoa tiivistää ja kuljettaa hermeettisiä säiliöitä. Samoin se voidaan liuottaa huomattavasti veteen, aiheuttaen kellertäviä ratkaisuja. Toisaalta se voidaan kuljettaa myös kiinteänä hydrokloridisuolan muodossa, ch3Nh2· HCL.
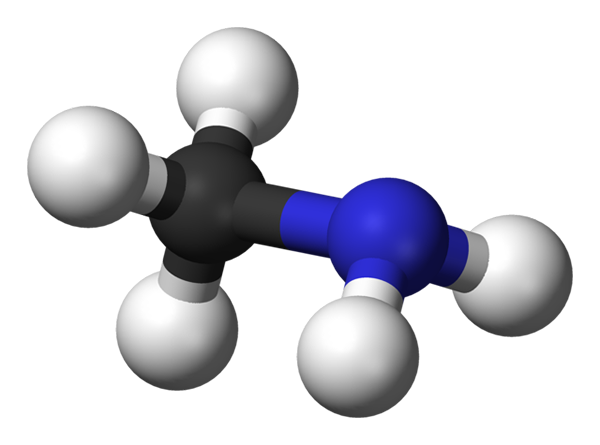
 Metilamiinimolekyyli. Lähde: Benjah-BMM27 Wikipedian kautta.
Metilamiinimolekyyli. Lähde: Benjah-BMM27 Wikipedian kautta. Metilamiini tapahtuu teollisesti ammoniakista ja metanolista, vaikka laboratorio -asteikolla on monia muita tuotantomenetelmiä. Sen kaasu on erittäin räjähtävä, joten jokaisella lähellä olevaan lämmönlähteeseen on potentiaali aiheuttaa suurta tulipaloa.
Se on yhdiste, jolla on korkea kaupallinen kysyntä, mutta samalla se aiheuttaa vahvoja oikeudellisia rajoituksia, koska se toimii huumeiden ja psykotrooppisten aineiden raaka -aineena.
[TOC]
Rakenne
Yllä oleva kuva näyttää metyyliamiinin molekyylirakenteen, jota edustaa pallo- ja tankojen malli. Musta pallo vastaa hiiliatomia, sinistä typpiatomiin ja valkoinen vetyatomeihin. Siksi se on pieni molekyyli, jossa metaani, cho4, Menettää H NH -ryhmään2, Antaa CH3Nh2.
Metilamiini on erittäin polaarinen molekyyli, koska typpiatomi houkuttelee elektronista hiilitiheyttä ja vetyatomeja. Sillä on kyky myös muodostaa vety sillat molekyylien välisten voimien kokoelman välillä. Jokainen CH -molekyyli3Nh2 Voit lahjoittaa tai hyväksyä peräkkäisen vetysillan (CH3HNH-NH2CH3-A.
Voi palvella sinua: Mikä on bänditeoria?Sen molekyylimassa on kuitenkin huomattavasti alhainen porttien lisäksi3 Ne estävät sellaisia vety sillat. Tuloksena on, että metyyliamiini on kaasu normaaleissa olosuhteissa, mutta se voidaan tiivistää lämpötilassa -6 ºC. Kitettäessä se tekee niin ortorromisen rakenteen seurauksena.
Ominaisuudet
Fyysinen ulkonäkö
Värikäs kaasu tai neste, mutta joiden vesipitoiset liuokset voivat esiintyä kellertäviä sävyjä.
Haju
Epämiellyttävä, samanlainen kuin kalan ja ammoniakin seoksen.
Moolimassa
31 058 g/mol
Sulamispiste
-93.10 ºC
Kiehumispiste
Noin -6 ºC: n noin. Siksi se on kaasu, joka voi tiivistää ei liian kylmässä lämpötilassa.
Tiheys
656,2 kg/m3 25 ºC: lla. Sen höyryt ovat 1,1 kertaa tiheitä kuin ilma, kun taas sen neste tai kondensaatti on noin 0,89 kertaa vähemmän tiheä kuin vesi.
Höyrynpaine
Huoneen lämpötilassa höyrynpaine vaihtelee 3,5 atm.
Dipolaarinen hetki
1,31 d
Vesiliukoisuus
1.080 g/l 20 ºC: n lämpötilassa. Se on kaasu, joka liukenee erittäin hyvin veteen, koska molemmat molekyylit ovat polaarisia ja liittyvät toisiinsa, kun vedosiltoja muodostetaan (CH3HNH-OH2-A.
Perusteetti
Metilamiinilla on emäksisyysvakio (PKb -) 3,36. Tämä arvo osoittaa, että se on huomattavasti emäksinen aine, jopa enemmän kuin sama ammoniakki, joten se liukenee veteen tietyn määrän OH -ioneja- Kun hydrolysoitiin:
CH3Nh2 + H2Tai ⇌ ch3Nh3+ + vai niin-
Metilamiini on emäksisempi kuin ammoniakki, koska sen typpiatomilla on suurempi elektroninen tiheys. Tämä johtuu siitä, että Cho3 Tehty enemmän typpielektroneja kuin NH -molekyylin kolme vetyatomia3. Silti metyilamiinia pidetään heikkona pohjana muiden alkyamiinien tai amiinien edessä.
Voi palvella sinua: CO2 -linkkityyppiLeimahduspiste
-10 ºC suljettuun kuppiin, mikä tarkoittaa, että se on erittäin syttyvä ja vaarallinen kaasu.
Itsensuuntainen lämpötila
430 ºC
Pintajännitys
19,15 mn/m 25 ºC
Hajoaminen
Kun poltetaan, se hajoaa termisesti hiili- ja typpioksidit, jotka muodostavat myrkyllisen savua.
Tuotanto
Metilamiini voidaan tuottaa tai syntetisoida joko kaupallisella tai teollisella menetelmällä tai laboratoriomenetelmillä alemmilla asteikoilla.
Teollisuus-
Metilamiini tapahtuu teollisesti ammoniakin ja metanolin välillä tapahtuvan reaktion kautta katalyyttisellä sympaattisella geelituella. Tämän reaktion kemiallinen yhtälö on seuraava:
CH3Voi + NH3 → ch3Nh2 + H2JOMPIKUMPI
Prosessissa voidaan luoda muita alkamiineja; Metyilamiini on kuitenkin tuote, joka näyttää aineettisesti suositummalta.
Laboratorio-
Laboratoriotasolla on useita menetelmiä, jotka mahdollistavat pienen asteikon metyyliamiinin syntetisoinnin. Yksi niistä on reaktio vahvassa emäksisessä väliaineessa, KOH: sta, asetamidin ja bromin välillä, jonka aikana metyylisosianaatti syntyy, CH3NCO, joka puolestaan on hydrolysoitu metylaatioksi.
Metilamiinia voidaan varastoida kiinteäksi, jos neutraloitua suolahapolla, niin että muodostuu hydrokloridisuolaa:
CH3Nh2 + HCL → CH3Nh2· HCL
Sitten metyyliamiinihydrokloridi, edustaa myös [ch3Nh3] Cl, voi perustua turvalliseen paikkaan vesiliuoksen hankkimiseksi liuenneella kaasulla:
[CH3Nh3] Cl + naoh → ch3Nh2 + NaCl + H2JOMPIKUMPI
Toisaalta metyyliamiini voidaan syntetisoida myös heksamiinista (CH2-A6N4, joka on suoraan hydrolysoitu suolahapolla:
Voi palvella sinua: kiteytyminen(CH2-A6N4 + Hcl + 6 h2O → 4 NH4Cl + 6 ch2JOMPIKUMPI
Peräkkäin ammoniumkloridi reagoi kuuman formaldehydin kanssa aiheuttamaan metyilamiinia ja muurahaishappohöyryt, HCOOH.
Myös metyyliamiini voidaan saada vähentämällä nitrometaania, CH3EI2 Metallisella sinkillä ja suolahapolla.
Sovellukset
 Efedriini on lääkitys, joka tarvitsee metyilamiinia kaupalliseen tuotantoon. Lähde: Turkephant.
Efedriini on lääkitys, joka tarvitsee metyilamiinia kaupalliseen tuotantoon. Lähde: Turkephant. Metilamiini on yhdiste, jonka käyttötarkoitukset yleensä aiheuttavat kiistoja, koska se on ainetta, jota käytetään huumausaineiden synteesissä, kuten metamfetamiini. Itse asiassa sen suosio johtuu halusta, että Breaking Bad Television -sarjan päähenkilöiden piti saada se hinnalla millä hyvänsä.
Tätä yhdistettä käytetään myös raaka -aineena hyönteismyrkkyjen, lääkkeiden, pinta -aktiivisten aineiden, räjähteiden, väriaineiden, sienitautien, lisäaineiden jne., Joten sillä on vahva maailman kysyntä useiden laillisten rajoitusten lisäksi sen hankkimiseksi.
Sen valtava kemiallinen monipuolisuus johtuu sen CHO -molekyylistä3Nh2 Se on hyvä nukleofiilinen aine, joka on kytketty tai koordinoitu suuremman molekyylimassan substraateihin useissa orgaanisissa reaktioissa. Esimerkiksi, tämä perustuu efedriinin synteesiin, missä Cho3Nh2 Se liittyy molekyyliin, jonka seurauksena A H: n menetys.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5. painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. (10. painos.-A. Wiley Plus.
- Wikipedia. (2020). Metyyliamiini. Haettu: vuonna.Wikipedia.org
- Kansallinen bioteknologiatietojen keskus. (2020). Metyyliamiini. Pubchem -tietokanta., CID = 6329. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- Dylan Matthews. (15. elokuuta 2013). Tässä on se, mitä 'murtaminen huono' saa oikein ja väärin met -liiketoiminnasta. Toipunut: WashingtonPost.com
- Prepchem. (2020). Metyyliamiinihydrokloridin valmistus. Palautettu: prepchem.com

