Natriumnitraatin (nano3) rakenne, ominaisuudet, käytöt, riskit

- 1872
- 119
- Kelly Kilback
Hän natriumnitraatti Se on kiteinen epäorgaaninen kiinteä aine, joka on muodostettu natrium -ionilla+ ja nitraatti -ioni ei3-. Sen kemiallinen kaava on nano3. Luonnossa sitä löytyy nitratiinina tai nitratiittimineraalina, jota on runsaasti Atacaman autiomaassa Chilessä, joten tätä mineraalia kutsutaan myös Salitre de Chileksi tai Calicheksi.
Natriumnitraatti on epäyhtenäinen kiinteä kiinteä, mutta voi nopeuttaa syttyvien materiaalien hapettumista tai polttamista. Tästä syystä sillä on laaja käyttö ilotulitusvälineissä, räjähteissä, otteluissa, hiilen tiilissä ja tietyissä torjunta -aineissa, jyrsijöiden ja muiden pienten nisäkkäiden poistamiseksi.
 Nitratin or nitratita, nano sodium nitrate mineral3. John Sobolewski (JSS) [CC 3: lla.0 (https: // creativecommons.Org/lisenssit/by/3.0)]. Lähde: Wikimedia Commons.
Nitratin or nitratita, nano sodium nitrate mineral3. John Sobolewski (JSS) [CC 3: lla.0 (https: // creativecommons.Org/lisenssit/by/3.0)]. Lähde: Wikimedia Commons. Kyky suosia muiden materiaalien palamista tai sytytystä tarkoittaa, että sitä on manipuloitava erittäin varovaisesti. Jos se altistuu liekkeille tai tulipaloille, se voi hyödyntää. Tästä huolimatta nano3 Sitä käytetään elintarviketeollisuudessa, koska sillä on säilöntäaineita, etenkin lihaa ja tietyntyyppisiä juustoja.
Heidän liiallinen nauttiminen voi kuitenkin aiheuttaa terveysongelmia, etenkin raskaana olevilla naisilla, vauvoilla ja lapsilla. Ruoansulatusjärjestelmän nitriiteiksi muuttuessa voi aiheuttaa tiettyjä sairauksia.
[TOC]
Kemiallinen rakenne
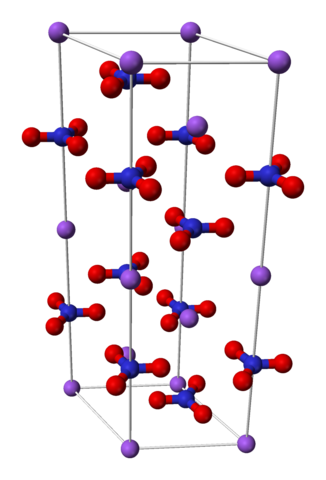 Nano3 Romboédrica Unikarinen solu. Lähde: Benjah-BMM27 [julkinen alue]
Nano3 Romboédrica Unikarinen solu. Lähde: Benjah-BMM27 [julkinen alue] Natriumnitraatti koostuu natriumkationista+ ja nitraatti -anionin ei3-.
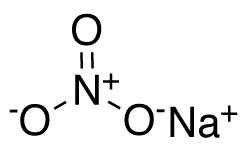 Nano -natriumnitraatti3. Ccroberts [julkinen alue]. Lähde: Wikimedia Commons.
Nano -natriumnitraatti3. Ccroberts [julkinen alue]. Lähde: Wikimedia Commons. Nitraatti -anionissa3- Typen N: n valenssi on +5 ja happi A -2: n valenssi. Tästä syystä nitraatti -anionilla on negatiivinen kuorma.
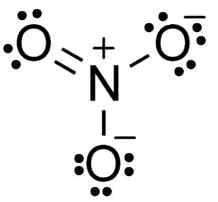 Nitraatti -ion Lewis -rakenne. TEM5psu [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)]. Lähde: Wikimedia Commons.
Nitraatti -ion Lewis -rakenne. TEM5psu [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)]. Lähde: Wikimedia Commons. Anionin ei3- Sillä on tasainen ja symmetrinen rakenne, jossa kolme happea jakavat negatiivisen tai tasaisen tavan.
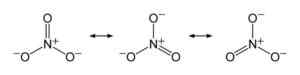 Nitraatti -ionissa negatiivinen kuorma jakautuu tasaisesti kolmen happiatomin kesken. Benjah-BMM27 [julkinen alue]. Lähde: Wikimedia Commons.
Nitraatti -ionissa negatiivinen kuorma jakautuu tasaisesti kolmen happiatomin kesken. Benjah-BMM27 [julkinen alue]. Lähde: Wikimedia Commons. Nimikkeistö
-Natriumnitraatti
-Natriumnitraatti
-Natriumsaltipetteri (englanti Natriumsuola-A
-Nitro -sooda (englanti Sooda -nitre-A
-Salitre de Chile
-Chileläinen nitraatti
-Nitratiini
-Nitratita
-Kaliche
Ominaisuudet
 Natriumnitraatin romboédical -kiteet, jotka on saatu sen ylikyllästeestä liuoksesta. Lähde: Vadim Sedov [CC 4: llä.0 (https: // creativecommons.Org/lisenssit/by/4.0)]
Natriumnitraatin romboédical -kiteet, jotka on saatu sen ylikyllästeestä liuoksesta. Lähde: Vadim Sedov [CC 4: llä.0 (https: // creativecommons.Org/lisenssit/by/4.0)] Fyysinen tila
Väritön väritön valkoinen, trigonaalinen tai rhomboedical kiteitä.
Molekyylipaino
84 995 g/mol
Sulamispiste
308 ºC
Kiehumispiste
380 ºC (hajoaa).
Tiheys
2 257 g/cm3 20 ºC.
Liukoisuus
Vesiliukoinen: 91,2 g/100 g vettä 25 ºC: lla tai 1 g 1,1 ml vettä. Liukenee hieman etanoliin ja metanoliin.
PHE
Natriumnitraattiliuokset ovat neutraaleja, toisin sanoen, ei happo tai emäksinen, siksi sen pH on 7.
Muut ominaisuudet
Se on hygroskooppinen kiinteä aine, ts. Se imee vettä ympäristöstä.
 Nano -natriumnitraatti3 kiinteä. Ondřej Mangl [julkinen alue]. Lähde: Wikimedia Commons.
Nano -natriumnitraatti3 kiinteä. Ondřej Mangl [julkinen alue]. Lähde: Wikimedia Commons. Sen veden liukeneminen aiheuttaa liuoksen jäähtymisen, joten sanotaan, että tämä liukenemisprosessi on endoterminen, toisin sanoen, kun liukenee se, se imee lämpöä ympäristöstä ja siksi liuos jäähtyy.
Voi palvella sinua: Ensisijainen hiili: Ominaisuudet, tyypit ja esimerkitHyvin alhaisissa lämpötiloissa natriumnitraatti liukenee nestemäiseen NH -ammoniakkiin3, Nanon muodostaminen3· 4NH3 Alle -42 ºC.
Nano3 Se ei ole polttoainetta, mutta sen läsnäolo kiihdyttää materiaalien tai yhdisteiden palamista. Tämä johtuu siitä, että kun sitä lämmitetään, happi tai2, muun muassa.
Saada
Se saadaan pääasiassa Salitre de Chilen (Caliche tai Nitratita) mineraaliesiintymien tai kaivoksien uuttamalla. Tätä varten käytetään suolavettä ja sitten kiteytyminen ja uudelleenkiteytys suoritetaan nanokiteiden saamiseksi3 puhtain.
Nämä kaivokset ovat pääasiassa Etelä -Amerikassa Pohjois -Chilessä Atacaman autiomaassa. Kaliumnitraatti -kno liittyy3 ja hajottaa orgaanista ainetta.
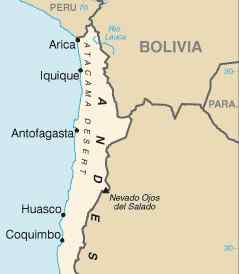 Atacaman autiomaassa sijaitseva sijainti Pohjois -Chilessä, missä on tärkeitä natriumnitraattia varten. CIA [julkinen alue]. Lähde: Wikimedia Commons.
Atacaman autiomaassa sijaitseva sijainti Pohjois -Chilessä, missä on tärkeitä natriumnitraattia varten. CIA [julkinen alue]. Lähde: Wikimedia Commons. Se voidaan saada myös reagoimalla typpihappo natriumkarbonaatin kanssa NA: lla2Yhteistyö3 tai NaOH -natriumhydroksidilla:
2 hno3 + Naa2Yhteistyö3 → 2 nano3 + Yhteistyö2↑ + H2JOMPIKUMPI
Läsnäolo ihmisen organismissa
Natriumnitraatti voi tulla ihmisen organismiin ruoan ja juomaveden kautta, joka sisältää sitä.
60-80% nautitusta nitraatista tulee hedelmistä ja vihanneksista. Toinen lähde on parannettu liha. Lihateollisuus käyttää sitä mikrobien kasvun estämiseen ja värien säilyttämiseen.
Suuri osa ihmiskehossa läsnä olevasta nitraatista tulee kuitenkin sen endogeenisestä synteesistä tai organismin prosesseista johtuen.
Sovellukset
Elintarviketeollisuudessa
Sitä käytetään elintarvikkeiden säilöntäaineena, suolakurkkua varten ja lihan värinpidätysmiehenä. Ruokaa, joka voi sisältää sitä.
 Parannetut lihat, jotka todennäköisesti sisältävät natriumnitraattia. Kirjoittaja: Falco. Lähde: Pixabay.
Parannetut lihat, jotka todennäköisesti sisältävät natriumnitraattia. Kirjoittaja: Falco. Lähde: Pixabay. Lannoitteissa
Natriumnitraattia käytetään lannoiteseoksissa tupakan, puuvillan ja vihanneskasvien hedelmöittämiseksi.
 Traktori viljelee istutusta. Kirjoittaja: Franck Barske. Lähde: Pixabay.
Traktori viljelee istutusta. Kirjoittaja: Franck Barske. Lähde: Pixabay. Palamisen tai räjähdyksen promoottorina tai imartelevana
Nano3 Sitä käytetään hapettimena monissa sovelluksissa. Se on vankka happirikas, joka helpottaa sytytysprosessia tuottamalla tai2.
Nanon läsnäolo3 Tekee materiaalit eivät vaadi happea ulkoisista lähteistä sytyttämiseen, koska tämä toimittaa riittävästi tai2 Mitä tulee itsensä vakaviin eksotermisiin reaktioihin (lämpögeneraattorit), jotka tapahtuvat tulehduksen tai räjähdyksen aikana.
Sitä on käytetty jo pitkään pyroteknisten materiaalien (ilotulitusten) päähapettina, räjähteiden ja räjähdyksen tai purskeiden hapettisen komponenttina ja ponneaineena aineena.
Voi palvella sinua: kemiallinen yhdiste Ilotulitus. Koostumuksessaan on nano -natriumnitraatti3. Kirjailija: pukeutuminen. Lähde: Pixabay.
Ilotulitus. Koostumuksessaan on nano -natriumnitraatti3. Kirjailija: pukeutuminen. Lähde: Pixabay. Sitä käytetään myös kivihiilen tiilien (briquetas) palamisen parantamiseen, otteluiden sytytyksen suosimiseksi ja jopa tupakan palavien ominaisuuksien parantamiseksi.
Jyrsijöiden ja muiden nisäkkäiden poistamiseksi
Sitä käytetään erityiseen torjunta -ainetyyppiin. Sitä sisältävät koostumukset ovat pyroteknisiä fumigantteja, jotka on sijoitettu ja poltettu hauihin, jotka vapauttavat tappavia myrkyllisiä kaasuja.
Tästä syystä sitä käytetään useiden jyrsijöiden, marmoottien, kojoottien ja skunksien hallintaan avoimilla pelloilla, nurmeilla, ei -viljelemättömillä alueilla, céspedes- ja golfkenttillä.
Muiden yhdisteiden valmistuksessa
Sitä käytetään typpihapon valmistuksessa HNO3, Nano -natriumnitriitti2, ja toimii myös katalysaattorina rikkihapon H valmistuksessa2Sw4.
Sitä käytetään typpioksidin valmistuksessa n2O ja hapettumisaineena farmaseuttisten yhdisteiden valmistuksessa.
Elektronisten jätteiden metallien uuttamisessa
Tietyt tutkijat havaitsivat, että nano3 Helpottaa elektronisiin laitteisiin sisältyvien metallien (matkapuhelimia, tabletteja, tietokoneita jne.-A.
Hyödylliset metallit, jotka voidaan uuteta näiden elektronisten laitteiden komponenteista, ovat Nickel Ni, Cobalt Co, Manganese MN, sinkki Zn, Copper Cu ja alumiini.
Uuttaminen tehdään käyttämällä vain yhtä nano -ratkaisua3 ja polymeeri. Ja 60%: n sato saavutetaan.
Tällä tavoin elektroninen jäte voidaan kierrättää, mikä edistää jätteiden minimointia ja resurssien vakaa talteenotto.
Terveys- ja liikuntatutkimuksessa
Joidenkin tutkimusten mukaan nano -lisäravinteiden nauttiminen3 tai sitä sisältävillä elintarvikkeilla on luonnollisesti positiivisia vaikutuksia terveyteen. Jotkut nitraateista runsaista elintarvikkeista ovat juurikkaiden, pinaatti ja arugula.
Vaikutusten joukossa on parantaa sydän- ja verisuonijärjestelmää, vähentää verenpainetta, parantaa verenvirtausta ja nostaa hapen määrää fyysisesti harjoitetuissa kudoksissa.
Tämä osoittaa, että nanon käyttöä voidaan harkita3 alhaisina kustannuslääkkeinä verenpaineongelmia sairastavien potilaiden ehkäisyssä ja hoidossa.
Lisäksi se voi toimia tehokkaana ja luonnollisena apuna lisäämään urheilijoiden lihasvoimaa.
Useissa käyttötarkoituksissa
 2000 -luvun mainosjuliste, joka yllyttää maksamaan maahan Chilen nitraatin kanssa. David Perez [julkinen alue]. Lähde: Wikimedia Commons.
2000 -luvun mainosjuliste, joka yllyttää maksamaan maahan Chilen nitraatin kanssa. David Perez [julkinen alue]. Lähde: Wikimedia Commons. Sitä käytetään hapettimena ja perustaja -aineena lasien ja emalien valmistuksessa keramiikkaan. Sitä käytetään myös erityisissä sementteissä.
Se toimii kemiallisena aineena tinan talteenotossa roskarejasta, lateksikoroinnissa, ydinteollisuudessa ja korroosion torjunnassa vesipitoisissa järjestelmissä.
Se voi palvella sinua: Disposio: rakenne, ominaisuudet, hankkiminen, käyttöRiskejä
Sen manipuloinnin vaarat
Sillä on ominaisuus kiihdyttää palavien materiaalien palamista. Jos olet mukana tulipalossa, räjähdys voi tapahtua.
Lämmölle tai tulipalolle altistettaessa voidaan hyödyntää, tuottaen myrkyllisiä typpioksideja.
Ruokaan tai veteen nauttimiseen liittyvät ongelmat
Nitraatti nautittuna voi tulla nitriitti sekä suussa että vatsassa että suolistossa.
Nitriitti, kun reagoivat joidenkin ruokien läsnä olevien amiinien kanssa, voi tulla nitrosamiini happamassa väliaineessa kuten vatsassa. Nitrosamiini ovat syöpää aiheuttavia.
Tätä ei kuitenkaan tapahdu, kun nitraatteja sisältävät hedelmät ja vihannekset ovat luonnollisesti.
Joidenkin tutkimusten mukaan korkeiden nitraattitasojen läsnäolo voi tuottaa verihäiriön, joka aiheuttaa hapen vapautumisen tehokkaasti kudoksissa.
Tätä voi tapahtua vauvoilla, joiden meijerikorja valmistetaan nitraatteja sisältävällä vesivedellä.
On myös havaittu, että korkea nitraattitaso voi aiheuttaa ongelmia vauvojen raskaudessa, aiheuttaen spontaaneja abortteja, ennenaikaisia syntymiä tai vikoja sikiöiden hermoputkessa.
Viime aikoina on havaittu, että natriumnitraatti voi tarkoittaa riskiä tuki- ja liikuntaelinten järjestelmän kehittymiselle, ja hermo-monish-lihasviestintä vaikuttaa ihmisissä.
Natriumnitraatti ruoassa
 Natriumnitraattia löytyy lisäaineena pekonissa ja muissa lihatuotteissa. Lähde: Cookbookman17 Flickr: n kautta (https: // www.Flickr.com/valokuvat/[Sähköposti suojaukset]/6175755733)
Natriumnitraattia löytyy lisäaineena pekonissa ja muissa lihatuotteissa. Lähde: Cookbookman17 Flickr: n kautta (https: // www.Flickr.com/valokuvat/[Sähköposti suojaukset]/6175755733) Natriumnitraatti on synonyymi lihalle, koska ne lisätään niihin yhdessä nitriitin kanssa niiden säilyttämiseksi ja heidän ulkonäkönsä ja makujen parantamiseksi. Sen vuoksi lihan liiallinen kulutus (perrocalientes, pekoni, kinkut, savustetut kalat jne.) on ollut mukana syöpien häiritsevässä linkissä koko ruuansulatuksessa.
Vaikka nitraattiset nitriittisuoloilla ja syövällä hoidetun lihan välinen suhde ei ole ehdoton, on suositeltavaa maltittaa sen saantia.
Toisaalta vihannekset (porkkanat, punajuuret, retiisi, salaatti, pinaatti jne.) Heillä on runsaasti nanoa3 Koska he ovat absorboineet sen viljelymaailmasta lannoitteen toiminnan vuoksi. Näiden vihannesten saanti, toisin kuin lihatuotteiden sato, ei liitetä mainittuihin sairauksiin.
Tämä johtuu kahdesta syystä: ero tällaisten elintarvikkeiden proteiinitasoissa ja tapa, jolla he kokkivat. Lihat paistamalla tai kuumentamalla liekki edistää nitraatti-nitriittien välillä tiettyjen aminohapporyhmien kanssa nitrosoamiinien tuottamiseksi: todelliset syöpää aiheuttavat aineet.
C -vitamiinin, kuidun ja polyfenolien pitoisuus vihanneksissa vähentää näiden nitrosoamiinien muodostumista. Siksi nano3 Yksinään se ei ole uhka ruokaa.
Viitteet
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Natriumnitraatti. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus.
- Ullmannin teollisuuskemian tietosanakirja. (1990). Viides painos. Vch verlagsgellschaft mbh.
- Kaatama, h.R -. ja Ravanbod, M. (2015). Mg/nanon kineettinen tutkimus3 Pyrotechnic käyttämällä ei-ooseathermaalista TG/DSC-tekniikkaa. J Thermal Calim (2015) 119: 2281-2288. Linkki palautettu.Jousto.com.
- Jarosz, J. et al. (2016). Natriumnitraatti vähentää agriinin indusoimaa asetyylikoliiniklusterireseptoria. BMC -farmakologia ja toksikologia (2016) 17:20. Haettu bmcpharmacoloksicolista.biolääketieteellinen.com.
- Puuvilla, f. Albert ja Wilkinson, Geoffrey. (1980). Edistynyt epäorgaaninen kemia. Neljäs painos. John Wiley & Sons.
- Yksityinen, m.J -. (2003). Syöpä. Karsinageenit ruokaketjussa. Elintarviketieteiden ja ravitsemuksen tietosanakirjassa (toinen painos). ScienEdirect.com.
- Zakhodyaeva ja.-Lla. et al. (2019). Metallien kompleksi uutto vesipitoisessa kaksifaasijärjestelmässä, joka perustuu poly (etyleenioksidiin) 1500 ja natriumnitraattiin. Molekyylit 2019, 24, 4078. MDPI toipui.com.
- Clements, W.T. et al. (2014). Nitraatin nauttiminen: Katsaus terveys- ja fyysisiin suorituskykyvaikutuksiin. Ravinteet 2014, 6, 5224-5264. MDPI toipui.com.

