Atominumero
- 2555
- 486
- Kelly Kilback
Mikä on atominumero?
Kemiallisen elementin atomiluku osoittaa mainitun elementin atomien ytimessä olevien protonien lukumäärän. Jos se oli neutraali atomi, silloin atominumero vastaa mainitun elementin elektronien lukumäärää.
Kuten tiedetään, atomien ydin koostuu protoneista ja neutroneista. Protoneilla on positiivinen varaus ja niiden arvo vastaa elektronin negatiivisen kuorman absoluuttista arvoa, joka on 1,6 x 10-19 Coulomb kansainvälisissä järjestelmäyksiköissä.
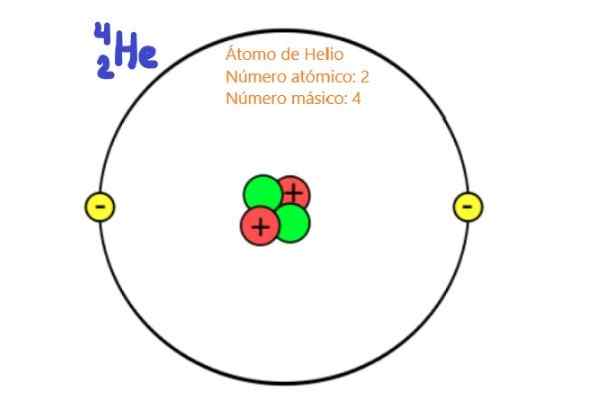
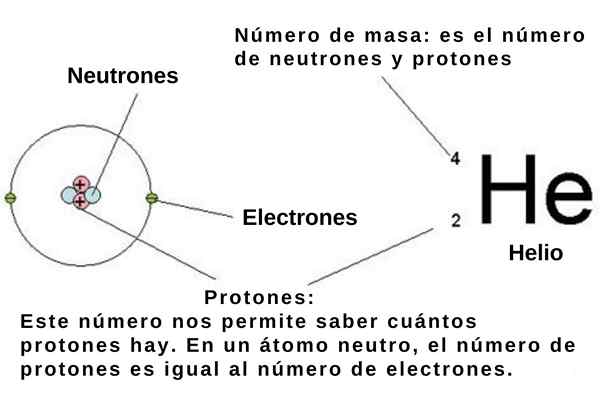
 Kuvio 1. Helium -atomin (He) kaavio. Protonien lukumäärä on atominumero. Neutronien lukumäärä plus protonien lukumäärä on massamäärä. Lähde: Wikimedia Commons.
Kuvio 1. Helium -atomin (He) kaavio. Protonien lukumäärä on atominumero. Neutronien lukumäärä plus protonien lukumäärä on massamäärä. Lähde: Wikimedia Commons. Koska ne ovat atomien ytimen hiukkasia, protonit ja neutronit tunnetaan nimellä Nukleonit. Juuri nämä hiukkaset käytännössä määräävät atomin massan, koska nukleonit ovat noin kaksi tuhatta kertaa massiivisempia kuin atomin elektronit. Tästä syystä kutsutaan nukleonien lukumäärää atomissa Massamäärä.
Kuitenkin atominumero Se määrittelee atomielementtien kemiallisen affiniteetin, koska neutraalissa atomeissa tämä luku osuu samaan aikaan elektronien lukumäärän kanssa.
Atomilukujen esitys
Jaksollisessa taulukossa kemiallisen elementin X -symbolia seuraa vasemmalla alakulmassa luvun Z kanssa, joka edustaa mainitun elementin atomi -määrää, kun taas elementin kemiallisen symbolin vasemmassa yläosassa, jonka massamäärä on osoitettu.
Voi palvella sinua: Andromeda: löytö, alkuperä, ominaisuudet, rakenneSeuraava kuva näyttää tämän merkinnän:
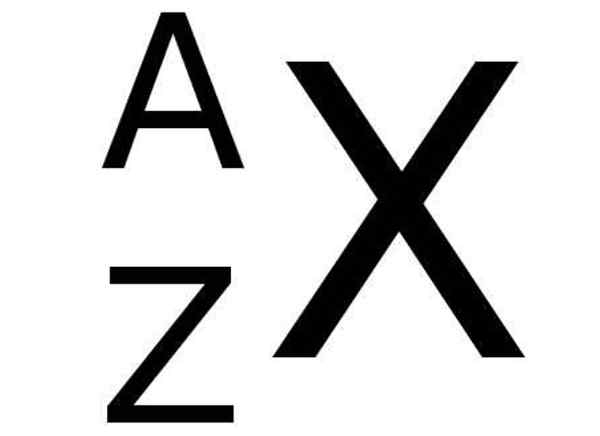 Kuva 2. Kemiallisen elementin X kemiallisen elementin X atominumero Z z ja massa numero A jaksollisessa taulukossa käytetyn yleissopimuksen mukaan. Lähde: Wikimedia Commons.
Kuva 2. Kemiallisen elementin X kemiallisen elementin X atominumero Z z ja massa numero A jaksollisessa taulukossa käytetyn yleissopimuksen mukaan. Lähde: Wikimedia Commons. Ja sitten, taulukko 1 näyttää joitain esimerkkejä kemiallisista elementeistä vastaavilla merkinnällään sekä atomi- ja massamäärällä:
pöytä 1
| Elementti | Merkintä | Atominumero z | Massa numero A |
|---|---|---|---|
| Vety | 1 1 H | 1 | 1 |
| Hiili | 12 6 C | 6 | 12 |
| Happi | 16 8 JOMPIKUMPI | 8 | 16 |
| Uraani | 238 92 TAI | 92 | 238 |
Atomien lukumäärä ja elementtien järjestys jaksollisessa taulukossa
Määräaikainen taulukko Kemialliset elementit sallivat elementtien peräkkäisen ja kasvavan järjestyksen niiden atomilukujen arvon mukaan.
Heistä vähintään 118 tunnetaan, alkaen vedystä, kunnes se saavuttaa elementin 118, joka on Oganeseon -Ennen soittamista Aakti-, jonka kemikaali on OG ja massamäärä on 294.
Ensimmäiset 10 kemiallista elementtiä, joiden tilaus on atomiluku, ovat paljon tutumpia. Siten esimerkiksi meillä on tunnetuin:
- Vety, h
- Helio, hän
- Litium, Li
- Beryllium, ole
- Boro, b
- Hiili, c
- Typpi, n
- Happi, o
- Fluori, f
- Neon, NE
 Kuva 3. Yksinkertaistettu jaksollinen taulukko, joka näyttää kemiallisten elementtien symbolit ja niiden atomiluku
Kuva 3. Yksinkertaistettu jaksollinen taulukko, joka näyttää kemiallisten elementtien symbolit ja niiden atomiluku Elektroninen kokoonpano
Atomiluku osoittaa protonien lukumäärän kemiallisen elementin atomien ytimessä ja jokaisella protonilla, kuten olemme sanoneet, on alkuainepositiivinen kuorma 1.602 x 10-19 C.
Jos atomi on neutraali, niin elektronien lukumäärä, jonka negatiivinen kuormitus on -1.602 x10-19 C: n on oltava yhtä suuri kuin atomiluku. Joten kemiallisen elementin numeerisen sijainnin tuntemus jaksollisessa taulukossa sen elektronien lukumäärä on myös tiedossa.
Voi palvella sinua: Power TransistoriAtomisessa nämä elektronit miehittävät alueet, joita kutsutaan Kiertoradat, jotka ovat riippuvaisia elektronin energiasta ja kulmamäärästä. Sekä atomin elektronien energia ja kulmavirta on kvantisoitu. Tämä tarkoittaa, että he voivat ottaa vain joitain erillisiä arvoja.
Nyt kiertoradalla asutut elektronilla alemmasta suurempaan energiaan noudattaen tiettyjä sääntöjä, jotka määrittävät elektronisen kokoonpanon.
Tällä tavoin elektronien lukumäärä orbitaaleilla tai atomin ulkoisilla tasoilla muodostaa yhteydet, jotka se voi muodostaa muiden atomien kanssa molekyylien muodostamiseksi. Tämä numero riippuu elektronisesta kokoonpanosta ja atomilukua.
 Lähde: Käyttäjä: MaterialScientist, CC0, Wikimedia Commonsin kautta
Lähde: Käyttäjä: MaterialScientist, CC0, Wikimedia Commonsin kautta Kvantinumerot
Atomin elektronin energia määritetään sen päämäärän perusteella n, jotka voivat ottaa kokonaisia arvoja 1, 2, 3 ..
Atomin elektronin kulmavirta määritetään toissijaisella kvanttiluvulla lens (kirjain ele) ja sen arvot riippuvat n.
Esimerkiksi n = 2 toissijainen kvanttiluku vie arvot välillä 0-N-1, toisin sanoen: 0 ja 1. Samoin n = 1, joka on alhaisin energiataso, toissijainen kvantinumero L vie vain arvon 0.
Toissijaiset kvantinumerot 0, 1, 2, 3 on vuorotellen merkitty kirjaimilla S, P, D ja F. S -kiertoradat ovat pallomaisia ja orbitaalit p lohkotaan.
Kvanttinumeroita on vielä kaksi:
- Magneettinen kvanttiluku ml, Se vie arvot -L: stä +l kulkee nollan läpi.
- Kvanttiluku Spin s, Se vie vain arvot+½ ja -½ ja on elektronin ominaisuus.
Lopuksi on Paulin syrjäytymisperiaate, jossa todetaan, että kahdella elektronilla ei voi olla neljä identtistä kvanttilukua. Tämän periaatteen seurauksena kiertoradalla voi olla korkeintaan kaksi elektronia, joilla on vastakkainen spin.
Elektroninen kokoonpanokaavio
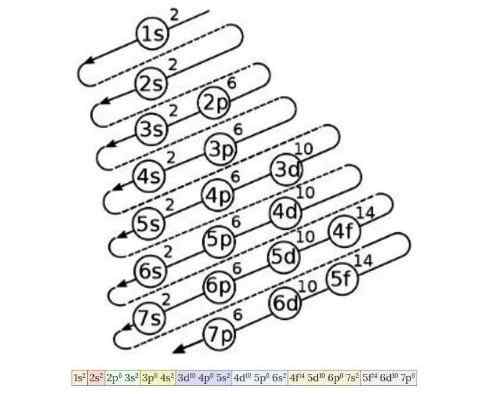
Elektronisen konfiguraatiokaavion avulla voidaan tietää elektronien täyttämisjärjestys pienemmästä energian kiertorauhasta korkeimpaan energiaan, kun kemiallisen elementin atomimäärän on tiedossa. Kuvio 4 näyttää tämän kaavion:
 Kuva 4. Elektroninen kokoonpano. Lähde: Wikimedia Commons.
Kuva 4. Elektroninen kokoonpano. Lähde: Wikimedia Commons. Kaavioidea idea on seuraava: Ensimmäinen numero osoittaa pääkvantinumeron, sitten kirjain osoittaa toissijaisen kvantinumeron, ja lopuksi kyselynumero osoittaa kyseisen kiertoradan mahdolliset elektronit.
Esimerkki
Elektroninen hiili- ja piiskokoonpano
Kuten edellä on todettu, hiilellä on atominumero 6, mikä tarkoittaa, että siinä on 6 elektronia, jotka jakautuvat seuraavasti: 1S2 2S2 2P2. Pidellä on puolestaan atominumero 14 ja sen elektronit jakautuvat tässä muussa muodossa: 1S2 2S2 2P6 3S2 3P2.
Molemmat elementit ovat samassa jaksollisen taulukon sarakkeessa, koska vaikka niillä olisi erilaiset atomilukut, niillä on sama elektroninen kokoonpano Lisää ulkoista kiertorata.
Viitteet
- Connor, n. Mikä on nukleoni - atomien ytimen rakenne - määritelmä. Haettu: jaksollisesta-rable.org.
- Huippukokous. Atominumero: Mikä se on, miten se on edustettuna. Palautettu: huippukokous.org
- Nostaja. Mikä on kemiallinen jaksollisuus? Haettu: Lifer.com
- Wikipedia. Elektroninen kokoonpano. Palautettu: on.Wikipedia.com
- Wikipedia. Atominumero. Palautettu: on.Wikipedia.com

