Koordinaationumero mikä on, laskelma, esimerkit

- 1648
- 258
- Joshua Emmerich
Hän Koordinointinumero Ionin ja koordinaatioyhdisteiden keskuksen kanssa on vuorovaikutuksessa atomien, ionien tai molekyylien määrä. Tätä käsitettä voidaan soveltaa myös molekyyleihin ottaen huomioon, kuinka monta atomia on kytketty toisiinsa linkkien lukumäärän sijasta.
Tämä luku on tärkeä, koska se määrittelee kompleksien geometriat, niiden materiaalifaasien tiheydet ja jopa niiden reaktiivisuuksien stereokemiallisen (alueellisen) luonteen. Määritelmänsä yksinkertaistamiseksi heitä pidetään ollenkaan atomin naapurina, joka ympäröi tiettyä keskustaa.
 Kolikoiden alueella voimme arvostaa sitä, mitä tarkoitetaan koordinaationumerolla
Kolikoiden alueella voimme arvostaa sitä, mitä tarkoitetaan koordinaationumerolla Harkitse esimerkiksi ylemmän kuvan kolikoista koostettua lattiaa. Kaikki kolikot ovat samankokoisia, ja jos jokaista havaitaan, sitä ympäröivät kuusi muuta; toisin sanoen heillä on kuusi naapuria ja siksi koordinointinumero (C.N.) Kolikoille se on 6. Sama ajatus ulottuu nyt kolmeen dimensioiseen tilaan.
Jos niiden radiot ovat epätasa -arvoisia, kaikilla ei ole samaa koordinointinumeroa. Esimerkiksi: Mitä suurempi valuutta, sitä enemmän naapureita, se pystyy vuorovaikutukseen suuremman määrän kolikoiden kanssa sen ympärillä. Päinvastoin tapahtuu pienten kolikoiden kanssa.
[TOC]
Koordinointinumerokonsepti
Vs ioniradiot. Koordinointinumero
Koordinointinumero on lähimpien naapureiden lukumäärä ja joka periaatteessa on vuorovaikutuksessa suoraan keskuksen kanssa, joka on enimmäkseen metalli -ioni. Joten laitamme kolikot syrjään sen sijaan palloja.
Tämä metallinen ioni mn+, missä n Se on yhtä suuri kuin sen hapettuminen tai Valencia. Mitä korkeampi se n (+2, +3, jne.), pienempi on mn+ Ja siten ligandit pakotetaan lähestymään enemmän vuorovaikutukseen m: n kanssan+.
Voi palvella sinua: Butiarus -rasva: hankkiminen, tyypit, koostumus, käytöt, edutSeuraava kuva kuvaa yllä:
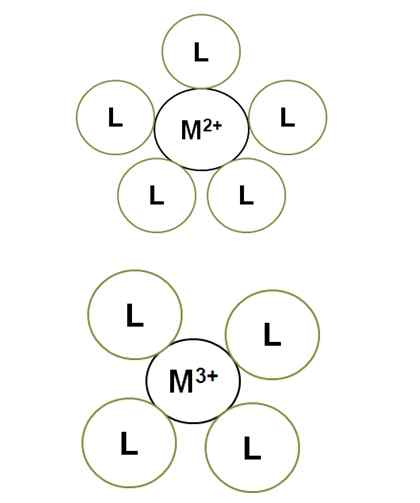 Koordinaatioluvun vaihtelu keskus -ionikuorman kanssa. Lähde: Gabriel Bolívar.
Koordinaatioluvun vaihtelu keskus -ionikuorman kanssa. Lähde: Gabriel Bolívar. M2+ Valaistuneessa kompleksissa sen koordinointinumero on 5: sitä ympäröi 5 ligandia l. Sillä välin m3+ on 4 koordinaationumero. Tämä johtuu siitä, että m3+, Sillä enemmän kuormitusta, sen säteen sopimuksia ja siksi sideaineiden on lähestyttävä enemmän, mikä lisää heidän elektronisia torjuntaansa.
Siksi tilaa vieviä keskus -ioneja, kuten lohkometalleihin kuuluvat F, tai lohkon toiseen tai kolmanteen jaksoon d -d, Heillä on yleensä korkeampi koordinaatioluku (C.N. > 6).
Tiheys
Oletetaan nyt, että M -kompleksi3+ Paineta. Paine saapuu pisteeseen, että toinen linkki on todennäköinen koordinoitu tai vuorovaikutuksessa m: n kanssa3+. Ts.
Yleensä paineet lisäävät koordinaatiolukuja, kun naapurit pakottavat toisiaan keskus -ioniin tai atomiin. Näin ollen näiden aineiden materiaalifaasit muuttuvat tiheämmäksi, kompaktiksi.
Geometriat
Korkeammat kuvat eivät sano mitään g -geometrioista M: n ympärillä2+ tai m3+. Tiedämme kuitenkin, että neliöllä on neljä kärkeä tai kulmaa, aivan kuten tetraedri.
Tämä päättely päätellään, että geometria M: n ympärillä3+, kenen c.N. Se on 4, sen on oltava tetraedrista tai neliötä. Mutta mikä kahdesta? Samaan aikaan g -geometriat2+, kenen c.N. Se on 5, ne voivat olla neliöpyramidi tai trigonaalinen bipiramidi.
Jokainen c.N. Se on liittynyt useisiin mahdollisiin geometrioihin, jotka asettavat sideaineet suotuisan etäisyyteen, niin että niiden välillä on pienintäkään.
Voi palvella sinua: interatomiset linkitKuinka koordinaationumero lasketaan tai määritetään?
Koordinointinumero voidaan laskea joskus suoraan kyseisestä yhdistelmäkaavasta. Oletetaan, että anioninen kompleksi [Ni (CN)5-3-. Mikä on nikkeli -ionin koordinointinumero, tai2+? Se riittää tarkkailemaan stökiömetristä kerrointa 5, mikä osoittaa, että on 5 CN -anionia- koordinoitu tai vuorovaikutuksessa Ni: n keskuksen kanssa2+.
Se ei kuitenkaan ole aina helppoa. Esimerkiksi CUCN -yhdisteellä näyttää olevan koordinaationumero 1 molemmille CU: lle2+ CN: n suhteen-. Se koostuu kuitenkin tosiasiallisesti cu-cn-cu-cn -polymeeriketjuista, joten oikea koordinaationumero on 2.
Siksi koordinaatioluku on parempi määrittää se sen laskemisen sijasta. Kuten? Yhdisteiden ionisten tai molekyylirakenteiden määrittäminen. Tämä on mahdollista instrumentaalitekniikoiden, kuten x -rayndiffraktion, neutronien tai elektronien, ansiosta.
Esimerkkejä koordinointinumeroista
Seuraavaksi ja lopuksi joitain esimerkkejä yhdisteistä mainitaan jokaiselle yleisimmalle koordinaatioluvulle. Samoin sanotaan, mitä heidän geometriat ovat.
C.N. 2
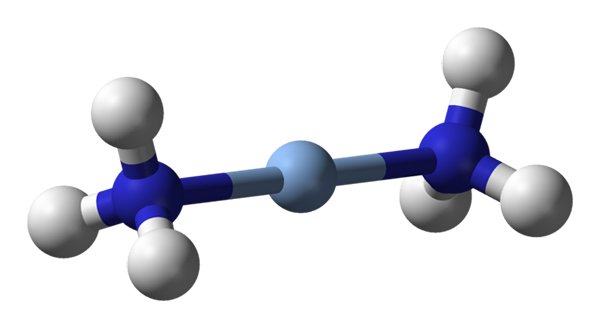 Tässä havaitaan [AG (NH3) 2] lineaarinen geometria+. Lähde: Benjah-BMM27 / julkinen verkkotunnus
Tässä havaitaan [AG (NH3) 2] lineaarinen geometria+. Lähde: Benjah-BMM27 / julkinen verkkotunnus A c.N. yhtä suuri kuin 2 tarkoittaa, että keskusatomilla tai ionilla on vain kaksi naapuria. Siksi puhumme yhdisteistä, jotka ovat pakollisesti lineaarisista geometrioista. Niiden välillä meillä on:
-HG (CH3-A2
-[AG (NH3-A2-+
-PHE3Pykälä
C.N. 3
 Jokainen tämän grafiittiarkin hiiliatomi on kytketty kolmeen muuhun, joten siinä on kolme naapuria. Lähde: Benjah-BMM27 / julkinen verkkotunnus
Jokainen tämän grafiittiarkin hiiliatomi on kytketty kolmeen muuhun, joten siinä on kolme naapuria. Lähde: Benjah-BMM27 / julkinen verkkotunnus A c.N. yhtä suuri kuin 3 tarkoittaa, että keskusatomi tai ionia ympäröivät kolme naapuria. Sitten meillä on geometriat, kuten: trigonaalinen (kolmion muotoinen) taso, trigonaalinen pyramidi ja t -muoto. Esimerkkejä yhdisteistä, joilla on tämä koordinointinumero, ovat:
Se voi palvella sinua: Atomi -massa: Määritelmä, tyypit, kuinka laskea, esimerkkejä-[Cu (CN)3-2-
-[PT (PCY3-A3], Missä PCY viittaa trikoheksylofospiiniligandiin
-Grafiitti
C.N. 4
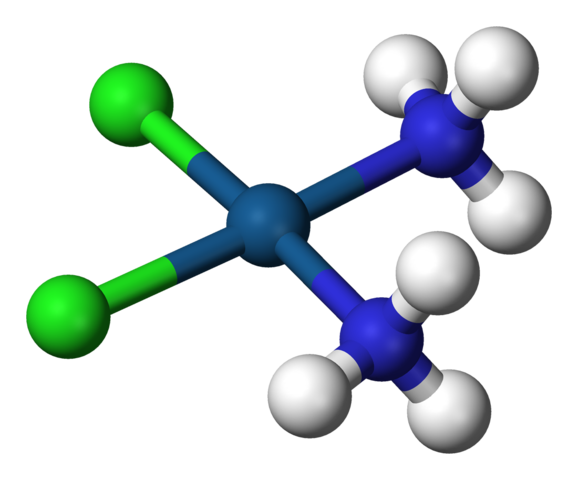 Sisplatiinin neliögeometria, cis-ptcl2 (NH3) 2. Lähde: Benjah-BMM27 / julkinen verkkotunnus
Sisplatiinin neliögeometria, cis-ptcl2 (NH3) 2. Lähde: Benjah-BMM27 / julkinen verkkotunnus A c.N. yhtä suuri kuin 4 tarkoittaa, että keskusatomi tai ionia ympäröivät neljä naapuria. Sen mahdolliset geometriat ovat tetraedrisia tai neliöitä. Esimerkkejä tämän koordinointinumeron yhdisteistä on seuraavat:
-CH4
-Cocl2tyrmätä2
-Cis-ptcl2(NH3-A2
-[Alcl4--
-[Moo4-2-
-Sncl4
-[CRO4-2-
-[MNO4-2-
Kaikki nämä esimerkit, lukuun ottamatta cis-ptcl2(NH3-A2, Ne ovat tetraedrisia geometrioita.
C.N. 5
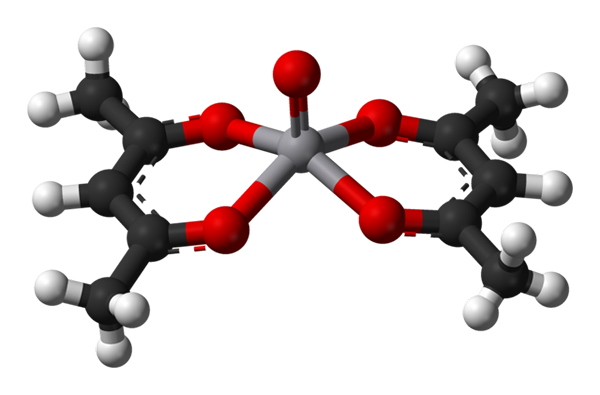 Neliöpyramidigeometria VO (ACAC) 2: lle. Lähde: Benjah-BMM27 / julkinen verkkotunnus.
Neliöpyramidigeometria VO (ACAC) 2: lle. Lähde: Benjah-BMM27 / julkinen verkkotunnus. A c.N. yhtä suuri kuin 5 tarkoittaa, että atomi tai keskus -ioni on koordinoitu tai vuorovaikutuksessa viiden naapurin kanssa. Sen geometriat, jo mainittu, ovat neliöpyramidi tai trigonaalinen bipiramidi. Esimerkiksi meillä on seuraavat:
-[Cobrn (ch2CH2NME2-A3-
-[Fe (CO)5-
-VO (Acac)2, Acac on asetyyliasetonaattiligandi
C.N. 6
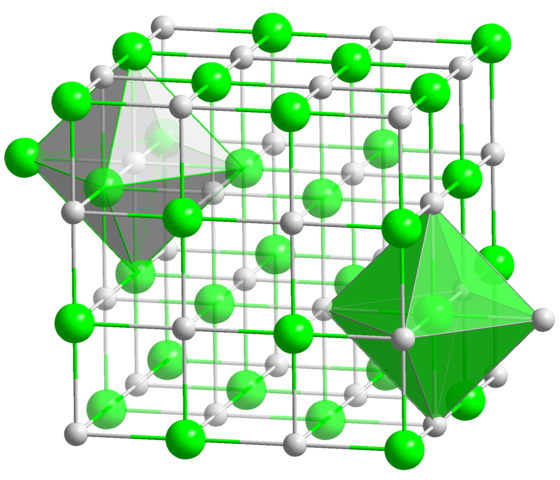 NaCl: n kiteisessä rakenteessa jokaisella Na+ -ionilla ja Cl- on kuusi naapuria, joten tämä on molemmille ionille koordinointinumero (katso oktaedra). Lähde: Solid State / Julkinen verkkotunnus
NaCl: n kiteisessä rakenteessa jokaisella Na+ -ionilla ja Cl- on kuusi naapuria, joten tämä on molemmille ionille koordinointinumero (katso oktaedra). Lähde: Solid State / Julkinen verkkotunnus Tämä on ylivoimaisesti yleisin koordinointimäärä kaikkien yhdisteiden välillä. Muista esimerkki periaatteellisista kolikoista. Mutta sen suosikkigeometrian sijasta on litteän kuusikulmion geekagonia, joka vastaa oktaedron (normaalia tai vääristynyttä), trigonaalisen prisman lisäksi. Jotkut monista esimerkeistä tämän koordinaatioluvun yhdisteistä ovat:
-[ALF6-3-
-[Co (NH3-A6-3+
-[ZR (valitse3-A6-2-
-NaCl (kyllä, pöytäsuola)
-Moss2, Huomaa, että c.N. Tälle yhdisteelle ei ole 2
Toiset
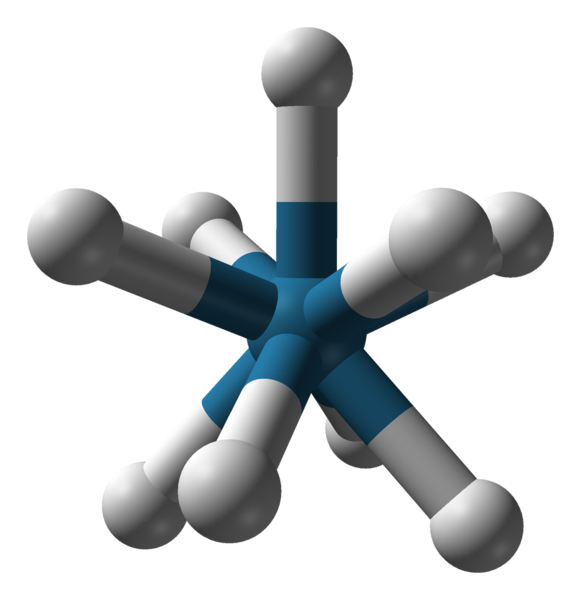 Anionin [Reh9] 2 Tripdaded Tripadic Prisma -geometria [Reh9]-. Lähde: Benjah-BMM27 / julkinen verkkotunnus.
Anionin [Reh9] 2 Tripdaded Tripadic Prisma -geometria [Reh9]-. Lähde: Benjah-BMM27 / julkinen verkkotunnus. On myös muita koordinointinumeroita, 7-15. Niin että c.N. Ole korkea, keskus -ionin tai atomin on oltava erittäin suuri, siinä on vähän kuormaa, ja samalla ligandien on oltava hyvin pieniä. Joitakin esimerkkejä sellaisista yhdisteistä, joilla on sellainen c.N. Ne ovat alla ja päättyvät:
-K -k -3[NBOF6], C.N. 7 ja Octaedro -geometria
-[MO (CN)8-3-
-[ZR (OX)4-2-, Oxalaattiligandi oksina
-[Reh9-2-
-[Kulmata3-A6-2-, C.N. yhtä suuri kuin 12
Viitteet
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Wikipedia. (2020). Koordinointinumero. Haettu: vuonna.Wikipedia.org
- Enyclopaedia Britannica -toimittajat. (S.F.-A. Koordinointinumero. Toipunut: Britannica.com
- Prof. Robert J. Lancashire. (15. elokuuta 2020). Koordinaatioluvut ja geometria. Kemian librettexts. Palautettu: Chem.Librettexts.org
- Helmestine, Anne Marie, PH.D -d. (28. elokuuta 2020). Koordinointinumero Kemian määritelmä. Toipunut: Admingco.com
- « Argumentatiiviset resurssien käsitteet, tyypit ja esimerkit
- 10 esimerkkiä sovelletusta tutkimuksesta »

