Kolminkertainen
- 2316
- 610
- Kelly Kilback
Mikä on kolminkertainen kohta?
Hän Kolminkertainen Se on termodynamiikan kentällä, joka viittaa lämpötilaan ja paineeseen, jossa termodynaamisessa tasapainotilassa on samanaikaisesti kolme vaihetta. Tämä kohta on olemassa kaikille aineille, vaikka olosuhteet, joissa ne saavutetaan, vaihtelevat suuresti kunkin välillä.
Kolminkertainen piste voi myös sisältää useamman kuin yhden samantyyppisen vaiheen tietyn aineen kannalta; Eli havaitaan kaksi erilaista kiinteää, neste- tai kaasuvaihetta. Helium, erityisesti sen Helio-4-isotooppi, on hyvä esimerkki kolminkertaisesta pisteestä, joka sisältää kaksi yksittäistä nestefaasi: normaalia ja tarpeetonta nestettä.
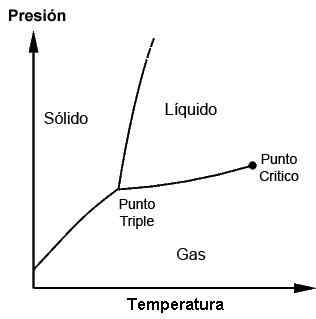
 Vaihekaavio, joka näyttää kolminkertaisen pisteen ja kriittisen pisteen
Vaihekaavio, joka näyttää kolminkertaisen pisteen ja kriittisen pisteen Mihin se on ja milloin kolminkertaista pistettä käytetään?
Kolminkertaista vettä käytetään Kelvinin määrittelemiseen, termodynaamisen lämpötilan perusyksikön kansainvälisessä yksikössä (SI). Tämä arvo asetetaan määritelmän mukaan mittauksen sijasta.
Kunkin aineen kolminkertaiset pisteet voidaan havaita käyttämällä vaihekaavioita, jotka ovat piirrettyjä kuvaajia, jotka mahdollistavat aineen kiinteän, nestemäisen, kaasumaisen vaiheen (ja muiden erityistapauksissa) rajoittavien olosuhteiden osoittamisen, kun ne tekevät muutoksia lämpötila, paine ja/tai liukoisuus.
Aine löytyy sen sulamispisteestä, jossa kiinteä aine kohtaa nesteen; Se löytyy myös kiehumiskohdasta, jossa neste kohtaa kaasun. Kuitenkin se on kolminkertainen pisteessä, jolloin kolme vaihetta saavutetaan. Nämä kaaviot ovat erilaisia jokaiselle aineelle, kuten myöhemmin nähdään.
Voi palvella sinua: API Gravity: Scale and luokittelu raakaöljynKolminkertaista pistettä voidaan käyttää tehokkaasti lämpömittarien kalibroinnissa käyttämällä kolminkertaisia soluja.
Nämä ovat aineiden näytteitä eristetyissä olosuhteissa (lasin "soluissa"), jotka ovat niiden kolminkertaisessa pisteessä tunnetuilla lämpötila- ja paine -olosuhteilla, ja siten helpottavat lämpömittarin mittausten tarkkuuden tutkimusta.
Tämän konseptin tutkimusta Planet Marsin tutkimuksessa on myös käytetty, jossa merenpinta yritettiin 1970 -luvulla suoritetuissa tehtävissä.
Kolminkertainen vesi
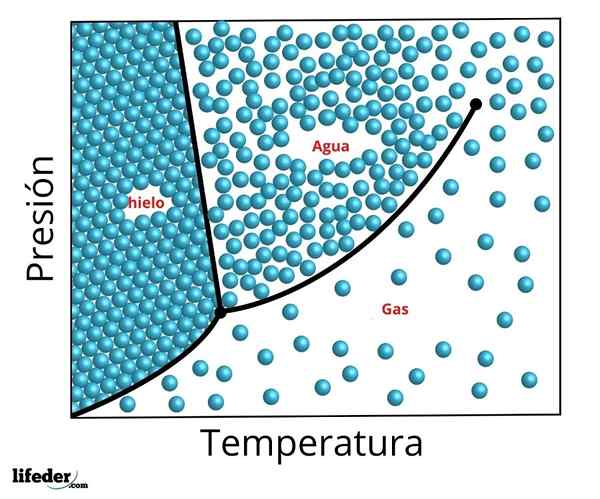 Veden kolminkertaisen pisteen vaihekaavio. Kolminkertainen kohta on alempi piste ja kriitikko ylempi piste
Veden kolminkertaisen pisteen vaihekaavio. Kolminkertainen kohta on alempi piste ja kriitikko ylempi piste Tarkat paineen ja lämpötilan olosuhteet, joissa vesi esiintyy samanaikaisesti sen kolmessa vaiheessa tasapainossa - nestemäisessä vedessä, jäällä ja höyryllä - esiintyy tarkalleen 273,16 K (0,01 ºC) ja höyryn 611 656 PASCALS (0,00603659 ATM: n höyryn osittaisessa paineessa (0,00603659 -A.
Tässä vaiheessa on mahdollista muuntaa aine mihin tahansa kolmesta vaiheesta, joiden lämpötilan tai paineen muutokset ovat vähäisiä. Jopa silloin, kun järjestelmän kokonaispaine voisi sijaita kolminkertaisen pisteen vaaditun yläpuolelle, jos osittainen höyrynpaine on 611 656 PA, järjestelmä saavuttaa kolminkertaisen pisteen samalla tavalla.
Edellisessä kuvassa on mahdollista havaita kolminkertaisen pisteen esitys (tai Kolminkertainen, englanniksi) aineesta, jonka kaavio on samanlainen kuin veden, tämän arvon saavuttamiseksi vaaditun lämpötilan ja paineen mukaan.
Veden tapauksessa tämä kohta vastaa vähimmäispainetta, jolla nestemäistä vettä voi olla. Painettaa vähäisiä tähän kolminkertaiseen pisteeseen (esimerkiksi tyhjiössä) ja kun käytetään vakiopainekämmitystä, kiinteä jää muuttuu suoraan vesihöyryksi menemättä nesteen läpi; Tämä on prosessi nimeltään sublimaatio.
Se voi palvella sinua: Big Bang -teoria: Ominaisuudet, vaiheet, todisteet, ongelmatTämän vähimmäispaineen ulkopuolella (PTP), jää sulaa ensin nestemäisen veden muodostamiseksi, ja vain siellä se haihtuu tai kiehuu höyryn muodostamiseksi.
Monille aineille lämpötila -arvo sen kolminkertaisessa pisteessä on vähimmäislämpötila, jolla nestefaasi voi olla, mutta tätä ei tapahdu veden tapauksessa. Vesille tätä ei tapahdu, koska jään sulamispiste pienenee paineen perusteella, kuten edellisen kuvan vihreällä katkoviivalla esitetään.
Korkeassa painevaiheessa vedellä on melko monimutkainen vaihekaavio, joka näyttää viisitoista tunnettua jäävaihetta (eri lämpötiloissa ja paineissa), kymmenen erilaisen kolminkertaisen pisteen lisäksi, jotka esitetään seuraavassa kuvassa:
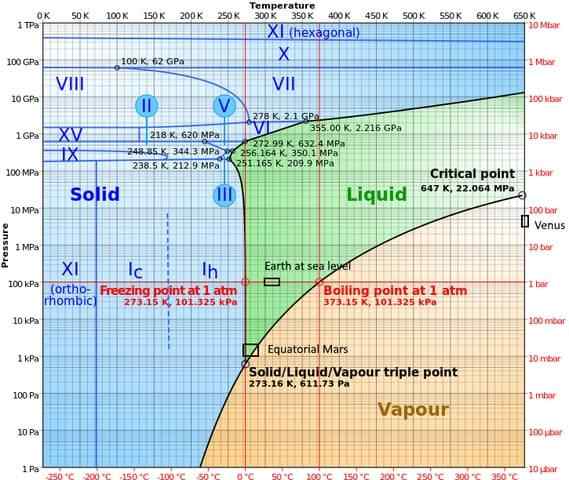
Voidaan huomata, että korkeapaine -olosuhteissa jää voi olla tasapainossa nesteen kanssa; Kaavio osoittaa, että sulautumispisteet kasvavat paineen kanssa. Matalassa vakiona lämpötiloissa ja kasvavassa paineessa höyry voidaan muuttaa suoraan jääksi menemättä nestefaasin läpi.
Erilaiset olosuhteet, joita esiintyy planeetoilla, joissa kolminkertainen piste (maa merellä ja Marsin päiväntasaajan alueella) on myös esitetty tässä kaaviossa).
Kaavio tekee selväksi, että kolminkertainen piste vaihtelee sijainnin mukaan paineen ja ilmakehän lämpötilan vuoksi, ei vain kokeilijan interventiolla.
Sykloheksaanin kolminkertainen piste
Sykloheksan on syklokano, jolla on C: n molekyylinen kaava6H12. Tällä aineella on erityispiirteet, joissa on kolminkertainen pisteen olosuhteet, jotka voidaan helposti toistaa, kuten veden tapauksessa, koska tämä piste sijaitsee lämpötilassa 279,47 K ja paine 5 388 kPa.
Se voi palvella sinua: Live -maksut: Konsepti, ominaisuudet, esimerkitNäissä olosuhteissa on havaittu Hirar -yhdiste, kiinteitä ja sulaa pienin lämpötilan ja paineen muutokset.
Kolminkertainen bentseenipiste
Sykloheksanin samanlaisessa tapauksessa bentseeni (orgaaninen yhdiste kemiallisella kaavalla C6H6) on helposti toistettavia kolminkertaisia olosuhteita laboratoriossa.
Sen arvot ovat 278,5 K ja 4,83 kPa, joten myös tämän aloittelijatason kokeilu on yleistä.
Viitteet
- Wikipedia. (S.F.-A. Wikipedia. Saatu.Wikipedia.org
- Britannica, e. (1998). Britannica Encyclopedia. Saatu Britannicalta.com
- Voima, n. (S.F.-A. Ydinvoiman ydin. Saatu ydinvoimalta.netto
- Wagner, W., Saul, a., & PRUB,. (1992). Kansainväliset yhtälöt painetta varten sulamis- ja tavallisen veden sublimointikäyrän varrella. Bochum.
- Penoncello, S. G., Jacobsen, R. T., & Goodwin, a. R -. (tuhatyhdeksänsataayhdeksänkymmentäviisi). Sykloheksaanin termodynaamiseen ominaisuuksien formulaatioon.

