Alumiinisulfidi (AL2S3) rakenne, ominaisuudet, käyttää
- 1354
- 204
- Gabriel Fahey
Hän Alumiinisulfidi (2S3) Se on vaaleanharmaa kemiallinen yhdiste, joka muodostuu metallisen alumiinin hapetuksella menettäessään viimeisen energiatason elektroneja ja muuttumalla kationiksi ja vähentämällä ei -metallista rikkiä, saamalla elektroneja, jotka ovat siirtäneet alumiinia ja tulemalla anioniksi.
Jotta tämä tapahtuisi ja alumiini voi tuottaa elektroneja, on välttämätöntä, että esität kolme hybridi -orbitaalia SP3, jotka antavat mahdollisuuden muodostaa linkkejä rikki elektroneihin.
Veden alumiinisulfidiherkkyys tarkoittaa, että ilmassa löydetyn vesihöyryn läsnä ollessa se voi reagoida alumiinihydroksidia (Al (OH)3), rikkivety (H2S) ja vety (H2) kaasumainen; Jos jälkimmäiset kertyvät, voi aiheuttaa räjähdyksen. Siksi alumiinisulfidipakkaukset tulisi tehdä hermeettisten astioiden avulla.
Toisaalta, koska alumiinisulfidilla on reaktiivisuus veden kanssa, tämä tekee siitä elementin, jolla ei ole liuotinliuotinta.
Kemiallinen rakenne
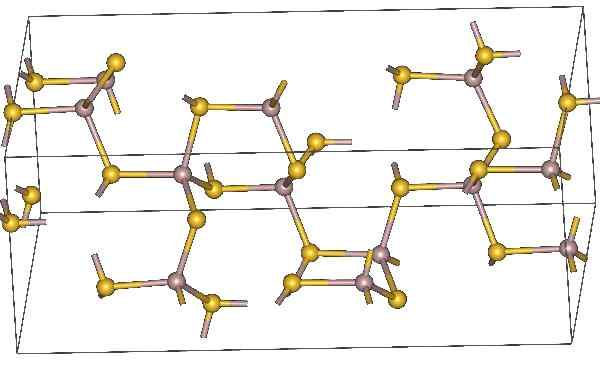
 Alumiinisulfidin kemiallinen rakenne. Keltaiset atomit edustavat rikkiä. Lähde: MaterialScientist, CC BY-SA 3.0, Wikimedia Commons
Alumiinisulfidin kemiallinen rakenne. Keltaiset atomit edustavat rikkiä. Lähde: MaterialScientist, CC BY-SA 3.0, Wikimedia Commons Molekyylikaava
Siihen2S3
Rakennekaava
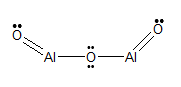 Nimikkeistö
Nimikkeistö
- Alumiinisulfidi.
- Di -alumiini trisulfidi.
- Alumiinisulfidi (III).
- Alumiinisulfidi.
Alumiinisulfidiominaisuudet
 Alumiinisulfidin ulkonäkö
Alumiinisulfidin ulkonäkö Kemiallisilla yhdisteillä on enimmäkseen kahden tyyppisiä ominaisuuksia: fysikaaliset ja kemialliset.
Fyysiset ominaisuudet
Moolimassa
150 158 g/mol
Tiheys
2,02 g/ml
Sulamispiste
1100 ° C
Vesiliukoisuus
Liukenematon
Kemialliset ominaisuudet
Yksi alumiinisulfidin pääreaktioista on vedellä, kuten substraatti tai pääreaktiivinen:

Tässä reaktiossa voidaan havaita alumiinihydroksidin ja rikkivetyrekisterin muodostuminen, jos se on kaasun muodossa, tai sulfidihappoa, jos se liuentuu veteen liuoksen muodossa. Hänen läsnäolonsa tunnistetaan mätäisten munien haju.
Voi palvella sinua: kemialliset ratkaisutKäyttö ja sovellukset
Super CardPisors
Alumiinisulfidia käytetään nanoverkkojen rakenteiden valmistuksessa, jotka parantavat erityistä pinta -alaa ja sähkönjohtavuutta, jotta voidaan saavuttaa korkea kapasitanssi ja energiatiheys, jonka sovellettavuus on Supercaugades.
Grafeenioksidi (GO) - Grafeeni on yksi hiilen alotrooppisista muodoista - on toiminut alumiinisulfidituena (Al2S3) Hierarkkisella morfologialla, joka on samanlainen kuin nanorambután, joka on valmistettu hydrotermisellä menetelmällä.
Grafeenioksidivaikutus
Grafeenioksidin ominaisuudet tukena sekä korkean sähkönjohtavuus ja pinta -ala tekevät nanorambutaanista2S3 olla sähkökemiallisesti aktiivinen.
Erityiset CV -kapasitanssikäyrät, joissa on hyvin määriteltyjä redox -piikkejä2S3 Hierarkkinen, kestävä grafeenioksidissa NaOH 1M -elektrolyytissä. Käyrästä saadut erityiset CV -kapasitanssiarvot ovat: 168,97 5MV/s etsintänopeudella.
Lisäksi on havaittu hyvää galvanostaattista purkausaika 903 µs, mikä on suuri spesifinen kapasitanssi 2178,16 3 mA/cm virran virtaan2. Galvanostaattisesta purkauksesta laskettu energiatiheys on 108,91 Wh/kg, virrantiheyteen 3 mA/cm2.
Sähkökemiallinen impedanssi vahvistaa siten hierarkkisen nanorambutane -elektrodin pseudokapaktiivisen luonteen2S3. Elektrodin stabiilisuustesti osoittaa 57,84 %: n retentiota jopa 1000 syklin erityiskapasitanssiin.
Koetulokset viittaavat siihen, että nanorambutaani2S3 Hierarkkinen sopii ylimääräisiin sovelluksiin.
Voi palvella sinua: Kromihydroksidi: rakenne, ominaisuudet, synteesi, käyttääToissijaisissa litiumparistoissa
Tarkoituksena kehittää sekundaarinen litiumakku, jolla on korkea energiatiheys, tutkittiin alumiinisulfidia (Al2S3) aktiivisena materiaalina.
Alkuperäinen latauskapasiteetti Mitta2S3 Se oli noin 1170 mAh G-1-100 m G-1. Tämä vastaa 62 % sulfidin teoreettisesta kapasiteetista.
AL2S3 Hänellä oli huono kapasiteetin pidättäminen potentiaalivälillä välillä 0,01 V - 2,0 V, pääasiassa kuormitusprosessin rakenteellisen peruuttamattomuuden tai LI: n louhinnan vuoksi.
XRD- ja K-XES-analyysi alumiinille ja rikki osoitti, että AL: n pinta2S3 Reagoi palautuvasti lastaus- ja purkamisprosessien aikana, kun taas AL: n ydin2S3 Hän osoitti rakenteellista peruuttamattomuutta, koska Lial ja Li2S perustettiin AL: sta2S3 Alkuperäisessä latauksessa ja sitten ne pysyivät sellaisina kuin ne olivat.
Riskejä
- Kosketuksessa veden kanssa vapauttaa syttyviä kaasuja, jotka voivat polttaa spontaanisti.
- Aiheuttaa ihon ärsytystä.
- Aiheuttaa vakavaa silmä ärsytystä.
- Voi aiheuttaa hengityselinten ärsytystä.
Tiedot voivat vaihdella ilmoitusten välillä epäpuhtauksien, lisäaineiden ja muiden tekijöiden mukaan.
Ensiapu
Yleinen hoito
Etsi lääketieteellistä hoitoa, jos oireet jatkuvat.
Erityiskohtelu
Ei mitään
Tärkeät oireet
Ei mitään
Inhalaatio
Ottaa uhri ulkopuolelle. Toimittaa happea, jos hengitys on vaikeaa.
Nieleminen
Hallitse yhtä tai kahta lasillista vettä ja indusoi oksentelua. Älä koskaan indusoi oksentelua tai antaa mitään suussa tajuttomalle henkilölle.
Turki
Pese vaurioitunut alue pehmeällä saippualla ja vedellä. Poista saastuneet vaatteet.
Silmät
Pese silmäsi vedellä, vilkkuu usein useita minuutteja. Poista piilolinssit, jos sinulla on niitä ja jatka huuhtelua.
Se voi palvella sinua: Crucible for Crucible: Ominaisuudet, toiminnot, käytä esimerkkejäPalontorjuntatoimenpiteet
Tuleen
Ei syttyvä.
Sukupuuttoon
Reagoi veden kanssa. Älä käytä vettä: käytä co₂-, hiekkaa ja pölyn sammutin.
Taistelumenettely
Käytä autonomista hengityslaitetta täydellisellä suojalla. Käytä vaatteita välttääksesi kosketusta ihon ja silmien kanssa.
Viitteet
- Terveys ja riskit.com, (s.f), määritelmä, käsitteet ja artikkelit terveydestä, riskeistä ja ympäristöstä. Haettu: terveys ja riskit.com
- Alumiinisulfidi. (S.F). Wikiwandissa. Haettu 9. maaliskuuta 2018: Wikiwand.com
- Web -elementit.(S.F).Dialuminium trisulpfide, palautettu 10. maaliskuuta 2018: WebElements.com
- LTS Research Laboratories, Inc (2016), Turvallisuustietolomake -alumiinisulfidi: LTSCHEM.com

