Renio Discovery, ominaisuudet, rakenne, käyttää

- 670
- 1
- Edgar VonRueden
Hän Renio Se on metallielementti, jonka kemiallinen symboli on RE ja sijaitsee jaksollisen taulukon ryhmässä 7, kaksi asemaa mangaanin alapuolella. Jaa tämän ja Technecion omistusoikeuden kanssa useiden numeroiden tai hapettumistilojen kanssa +1: stä +7: een. Muodostaa myös anionin nimeltä Perenato, vanki4-, Analoginen permanganaatin kanssa, MNO4-.
Tämä metalli on yksi harvinaisimmista ja niukimmista luonnossa, joten sen hinta on korkea. Se uutetaan molybdeenin ja kuparin louhinnan sivutuotteena. Yksi Renion merkittävimmistä ominaisuuksista on sen korkea sulamispiste, tuskin hiili ja volframi ja sen suuri tiheys, joka on kaksinkertainen lyijyn tiheys.
 Renio Metal -pallo. Lähde: Hi-Res-kuvat kemiallisista elementeistä/CC kirjoittanut (https: // creativecommons.Org/lisenssit/by/3.0)
Renio Metal -pallo. Lähde: Hi-Res-kuvat kemiallisista elementeistä/CC kirjoittanut (https: // creativecommons.Org/lisenssit/by/3.0) Hänen löytöllä on kiistanalaisia ja valitettavia vivahteita. 'Renio' -nimi on peräisin latinalaisesta sanasta 'RHENUS', joka tarkoittaa Rin, kuuluisaa saksalaista jokea lähellä sijaitsevaa sivustoa, jossa saksalaiset kemistit, jotka eristivät ja tunnistivat tämän uuden elementin, toimivat.
Reniolla on lukuisia käyttötarkoituksia, joiden joukossa bensiinitelineiden oktaanin hienosäätö.
[TOC]
Löytö
Kahden raskaan elementin olemassaolo, jolla on kemiallisia ominaisuuksia kuin mangaanin, oli jo ennustettu vuoden 1869 jälkeen Venäjän kemian Dmitri Mendelevin jaksollisen taulukon kautta. Siihen mennessä ei kuitenkaan ollut tiedossa, minkä heidän atomilukujensa tulisi olla; Ja se oli täällä vuonna 1913, kun englannin fyysikon Henry Moseleyn ennuste esiteltiin.
Moseleyn mukaan näillä mangaaniryhmään kuuluvien kahden elementin on oltava atomisluvut 43 ja 75.
Pari vuotta aiemmin japanilainen kemisti Masataka Ogawa oli kuitenkin löytänyt väitetyn elementin 43 näytteestä mineraalista Torianita. Ilmoitettuaan sen tulokset vuonna 1908 hän halusi kastaa tämän elementin nimellä Niponio. Valitettavasti kemistit osoittivat tuolloin, että Ogawa ei ollut löytänyt elementin 43.
Se voi palvella sinua: sykloalques: kemiallinen rakenne, ominaisuudet, nimikkeistöJa niin, muut vuodet kuluivat, kun vuonna 1925 kolme saksalaista kemistiä: Walter Noddack, Ida Noddack ja Otto Berg, löysivät elementin 75 Columbitan, Gadolinite- ja molybdenite -mineraalinäytteissä. Ne antoivat hänelle nimen Renio, Saksan Rin Rinin ('Rhenus', latinan) kunniaksi.
Masataka Ogawan virheen oli tarkoitus olla poissulkeminen elementin tunnistamisessa: hän oli löytänyt Renion, ei elementin 43, nimeltään Tecnecio tänään.
Renio -ominaisuudet
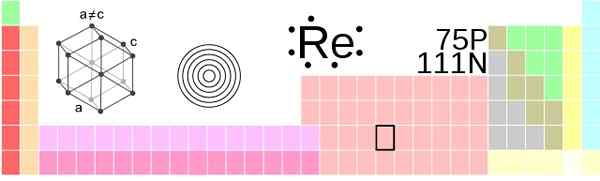 Renio -tilanne jaksollisessa taulukossa. !Alkuperäinen: AhoTeseierVector: Sushant Savla/CC BY-S (https: // creativecommons.Org/lisenssit/by-SA/3.0)
Renio -tilanne jaksollisessa taulukossa. !Alkuperäinen: AhoTeseierVector: Sushant Savla/CC BY-S (https: // creativecommons.Org/lisenssit/by-SA/3.0) Fyysinen ulkonäkö
Renioa markkinoidaan yleensä harmahtavan pölyn muodossa. Sen metallipalat, yleensä pallomaiset tipat, ovat hopeaharmaa, jotka ovat myös erittäin kirkkaita.
Moolimassa
186,207 g/mol
Atominumero
75
Sulamispiste
3186 ºC
Kiehumispiste
5630 ºC
Tiheys
-Huoneenlämpötilassa: 21,02 g/cm3
-Aivan sulamispisteessä: 18,9 g/cm3
Renio on metalli, joka on melkein kaksi kertaa tiheämpi kuin sama lyijy. Siten 1 grammaa painaava Renio -pallo voidaan rinnastaa saman massan voimakkaalla lyijykiteellä.
Elektronegatiivisuus
1.9 Pauling -asteikolla
Ionisaatioenergiat
Ensimmäinen: 760 kJ/mol
Toinen: 1260 kJ/mol
Kolmas: 2510 kJ/mol
Molaarinen lämpökapasiteetti
25,48 j/(mol · k)
Lämmönjohtokyky
48,0 W/(M · K)
Sähkövastus
193 nω · m
Mohsin kovuus
7
Isotoopit
Renio -atomit esitetään luonteeltaan kahtena isotooppina: 185Re, runsaasti 37,4%; ja 187Re, runsaasti 62,6%. Renio on yksi niistä elementeistä, joiden runsain isotooppi on radioaktiivinen; Kuitenkin puoli -elämän aika 187Re on erittäin suuri (4,12 · 1010 vuotta), joten sitä käytännössä pidetään vakaana.
Voi palvella sinua: Nikkeli: Historia, ominaisuudet, rakenne, käyttö, riskitReaktiivisuus
Metallinen Renio on hapettumisen vastustuskykyinen. Kun hän tekee, hänen oksidin, Re2JOMPIKUMPI7, Se haihtuu korkeissa lämpötiloissa ja palovammoissa kellertävän vihreän liekin kanssa. Renion kappaleet vastustavat Hnon hyökkäystä3 keskitetty; Mutta kuuma, liukenee generointiin Reniinihappoa ja typpidioksidia, joka värittää liuosta:
Re + 7hno3 → Hreo4 + 7 Ei2 + 3H2JOMPIKUMPI
Renion kemia on laaja, koska se kykenee muodostamaan yhdisteitä, joilla on laaja hapettumislukujen spektri, samoin kuin määrittämään nelikarvon sidos kahden Renio-atomin välillä (neljä uudelleenkovalenttia sidosta).
Elektroninen rakenne ja kokoonpano
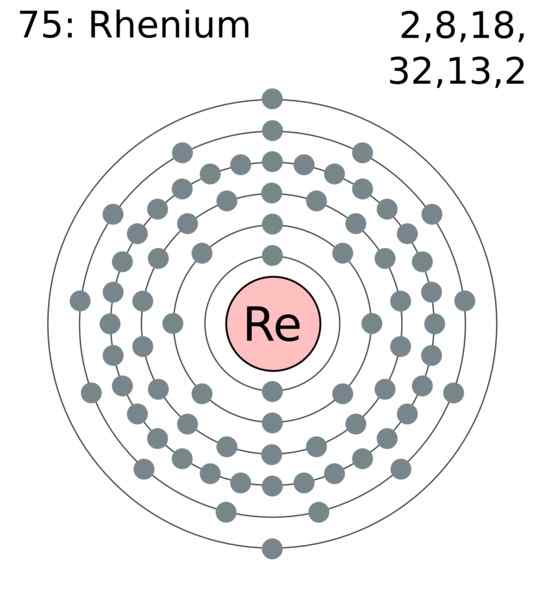 Renio -elektronikerros. Kirjoittaja: Käyttäjä: Gregrobson (Greg Robson). Wikimedia Commons
Renio -elektronikerros. Kirjoittaja: Käyttäjä: Gregrobson (Greg Robson). Wikimedia Commons Renio -atomit on ryhmitelty kiteisiinsä aiheuttaen kompakti kuusikulmainen rakenne, HCP, jolle on ominaista erittäin tiheä. Tämä on yhtä mieltä siitä, että se on suuren tiheyden metalli. Metallinen linkki, ulkoisten kiertoratojen päällekkäisyyden tuote, pitää atomit voimakkaasti yhtenäisinä.
Tässä metallisessa linkissä Valencian elektronit osallistuvat uudelleen elektronisen kokoonpanon mukaan:
[Xe] 4f14 5 D5 6s2
Periaatteessa 5D- ja 6S -kiertoradalla on päällekkäisyys kompakti RE -atomit HCP -rakenteessa. Huomaa, että elektronit lisäävät yhteensä 7, mikä vastaa ryhmäsi numeroa jaksollisessa taulukossa.
Hapetusluvut
Renio -elektroninen konfiguraatio heti välttää, että sen atomi pystyy menettämään jopa 7 elektronia, tullakseen hypoteettiseksi kationiksi7+. Kun RE: n olemassaolo oletetaan7+ Missä tahansa Renio -yhdisteessä, esimerkiksi RE: ssä2JOMPIKUMPI7 (Uudelleen27+JOMPIKUMPI72-), Sanotaan, että sillä on hapettumismäärä +7, re (vii).
Muut Renion positiiviset hapettumisnumerot ovat: +1 (Re+), +2 (Re2+), +3 (Re3+), Ja niin edelleen +7. Samoin Renio voi saada elektroneja tulemaan anioniksi. Näissä tapauksissa sanotaan, että sillä on negatiivinen hapettumisnumero: -3 (Re3-), -2 (Re2-) ja -1 (Re--A.
Se voi palvella sinua: hydrolyysi: mikä se on ja esimerkkejä reaktioistaSovellukset
Bensiini
Renioa yhdessä platinan kanssa käytetään luomaan katalyyttejä, jotka lisäävät bensiinin oktaanin astetta, samalla kun vähentävät sen lyijypitoisuutta. Toisaalta Renio -katalyyttejä on tarkoitettu useisiin hydrausreaktioihin, mikä johtuu niiden vastustuskyvystä myrkytystypen, fosforin ja rikin kanssa.
Tulenkestävät ylikuormitukset
Renio on tulenkestävä metallituote sen korkeasta sulamispisteestä. Siksi nikkeliseokset lisätään kääntämään ne tulenkestäväksi ja kestävät suuria paineita ja lämpötiloja. Näitä superleateja käytetään enimmäkseen turbiinien ja moottorien suunnitteluun ilmailu-.
Volframifilamentit
Renio voi myös muodostaa seoksia volframilla, mikä parantaa sen taipuisuutta ja helpottaa filamenttien valmistusta. Näitä Renio-Tungsten-filamentteja käytetään röntgenlähteinä ja lämpötilojen pystyvän lämpötilojen suunnittelussa 2200 ° C.
Samoin näitä Renio -filamentteja käytettiin kerran arkaaisissa kameroissa vilkkuissa ja tällä hetkellä hienostuneille laitevalaisimille; kuten massaspektrofotometri.
Viitteet
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Sarah Pierce. (2020). Rhenium: käyttö, historia, tosiasiat ja isotoopit. Opiskelu. Toipunut: Opiskelu.com
- Kansallinen bioteknologiatietojen keskus. (2020). Renium. Pubchem -tietokanta., CID = 23947. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- Wikipedia. (2020). Renium. Haettu: vuonna.Wikipedia.org
- DR. Doug Stewart. (2020). Rhenium -elementti tosiasiat. Toipunut: Chemicool.com
- Eric Scerri. (18. marraskuuta 2008). Renium. Kemia sen elementteissä. Toipunut: ChemistryWorld.com
- « Ei ominaisia elektrolyyttejä ja esimerkkejä
- Alfa-Cotogl Ominaisuudet, toiminnot ja sovellukset »

