Metyylisalisylaatti
- 2608
- 215
- Ronald Reilly
Mikä on metyylisalisylaatti?
Hän metyylisalisylaatti Se on orgaaninen kemikaali, jota pidetään yhdisteenä, jolla on suurempi myrkyllisyys tunnetuissa salisylaateissa, huolimatta värittömästä ja miellyttävästä hajustaan lievällä makealla kosketuksella. Tämä laji tunnetaan paremmin nimellä Gaulteria Oil. Sen kaava on c8H8JOMPIKUMPI3.
Se on nestemäisessä tilassa vakiolämpötila- ja paineolosuhteissa (25 ° C ja 1 atm), joka muodostaa orgaanisen esterin, joka luonnollisesti on peräisin monista kasveista. Sen tuotannon havainnoinnista ja tutkimuksesta oli mahdollista siirtyä metyylisalisylaatin synteesiin.
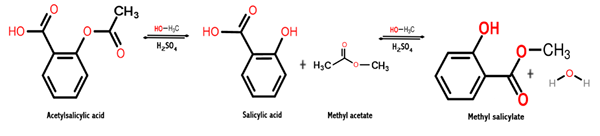
Tämä synteesi suoritettiin kemiallisella reaktiolla esterin välillä salisyylihaposta ja sen yhdistelmä metanolin kanssa. Tällä tavoin tämä yhdiste on osa salviaa, valkoviiniä ja hedelmiä, kuten luumu ja omena, muun muassa luonnollisesti löydettyjä.
Synteettistä, metyylisalisylaattia käytetään aromatisoivien aineiden tuotannossa, samoin kuin tietyissä aterioissa ja juomissa.
Kemiallinen rakenne
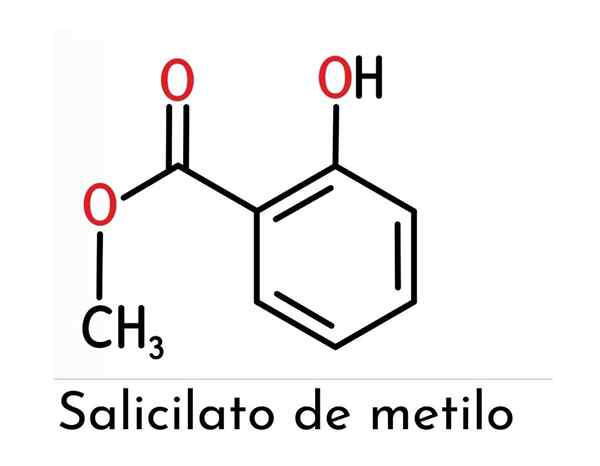
Metyylisalisylaatin kemiallinen rakenne muodostuu kahdesta pääfunktionaalisesta ryhmästä (esteri ja fenoli, joka on kiinnitetty tähän), kuten ylemmässä kuvassa esitetään.
Havaitaan, että se muodostaa benterinen rengas (joka edustaa suoraa vaikutusta yhdisteen reaktiivisuuteen ja stabiilisuuteen), salisyylihaposta, josta se on johdettu.
Niiden nimeämiseksi erikseen voidaan sanoa, että ne yhdistyvät orto -asentoon (1,2) hydroksyyliryhmä ja metyyliesteri edellä mainittuun renkaaseen.
Voi palvella sinua: tertiäärinen alkoholi: rakenne, ominaisuudet, esimerkitJoten kun OH -ryhmä on yhteydessä bentseenirenkaan, muodostuu fenoli, mutta ryhmä, jolla on suurin ”hierarkia” tässä molekyylissä.
Siten sen kemiallinen nimi esitetään metyylin 2-hydroksibentsoaattina, jonka IUPAC myöntää, vaikka sitä käytetään harvemmin viitaten tähän yhdisteeseen.
Ominaisuudet metyylisalisylaatti
- Se on kemiallinen laji, joka kuuluu salisylaattiryhmään, jotka ovat luonnollisia tuotteita joidenkin kasvi -organismien aineenvaihdunnasta.
- Lääketieteellisissä hoidoissa on tietoa salisylaattien terapeuttisista ominaisuuksista.
- Tätä yhdistettä esiintyy tietyissä juomissa, kuten valkoviini, tee, salvia ja tietyt hedelmät, kuten papaija tai kirsikka.
- Sitä löytyy luonnollisesti suuren määrän kasvien lehdistä, etenkin tietyissä perheissä.
- Se kuuluu orgaanisten esterien ryhmään, joka voidaan syntetisoida laboratoriossa.
- Se saadaan nestemäisessä tilassa, jonka tiheys on noin 1 174 g/ml tavanomaisissa paine- ja lämpötila -olosuhteissa (1 atm ja 25 ° C).
- Se muodostaa väritöntä, kellertävää tai punertavaa nestemäistä faasia, jota pidetään vesiliukoisena (joka on epäorgaaninen liuotin) ja muissa orgaanisissa liuottimissa.
- Sen kiehumispiste on noin 222 ° C, mikä osoittaa sen lämpöhajoamisen noin 340 - 350 ° C.
- Se esittelee useita sovelluksia, jotka vaihtelevat aromatisoivasta aineesta karkkiteollisuudessa kipulääkkeisiin ja muihin lääketeollisuuden tuotteisiin.
Voi palvella sinua: Natrium Azid (NAN3): rakenne, ominaisuudet, käytöt, riskit- Sen molekyyl kaava on esitetty c -muodossa8H8JOMPIKUMPI3 Ja sen molaarimassa on 152,15 g/mol.
Käyttää/sovelluksia
Rakenteellisten ominaisuuksiensa vuoksi, koska se on metyyliesteri salisyylihaposta, metyylisalisylaatilla on suuri määrä käyttöä eri alueilla.
Yksi tämän aineen päätarkoituksista (ja tunnetuimmista) on eri tuotteiden aromatisoiva aine: kosmetiikkateollisuudesta tuoksuna elintarviketeollisuuteen makeisten aromina (pureskeleva kumi, karkkeja, jäätelöä).
Sitä käytetään myös kosmetiikkateollisuudessa lämmitysaineena ja lihashierontaan urheilusovelluksissa. Jälkimmäisessä tapauksessa se toimii Rubefactory; toisin sanoen se aiheuttaa ihon pinnan punoituksen ja limakalvojen kalvoja, kun ne ovat kosketuksissa näiden kanssa.
Samalla tavalla sitä käytetään kerman ajan ajankohtaiseen käyttöön sen kipulääke- ja anti -inflammatorisiin ominaisuuksiin reumaattisten olosuhteiden käsittelyissä.
Toinen sen sovelluksista sisältää nestemäisen käytön aromaterapiaistunnoissa sen eteeristen öljyominaisuuksien vuoksi.
Tutkitaan sen lisäksi, että se on käytetty agenttina ultraviolettisäteilyä vastaan ultraviolettisäteilyä vastaan, sen ominaisuuksia valon edessä teknisiä sovelluksia tutkitaan, kuten lasersäteiden tuotantoa tai arkaluontoisten lajien luomista molekyylien tietojen varastointiin.
Synteesi jstk metyylisalisylaatti
Ensinnäkin on syytä mainita, että metyylisalisylaatti voidaan saada luonnollisesti tiettyjen kasvien haarojen, kuten gaulterian haarojen, tislauksesta (Gaultheria Procumbens) tai makea koivu (Hitaasti betula-A.
Se voi palvella sinua: ei metalleja: historia, ominaisuudet, ryhmät, käyttötarkoituksetTämä aine uutettiin ja eristettiin ensimmäistä kertaa vuonna 1843 ranskalaisen alkuperän tutkijan nimeltä Auguste Cahours; Gaulteriasta se saadaan tällä hetkellä laboratorioiden synteesin ja jopa kaupallisen kautta.
Tämän kemiallisen yhdisteen saamiseksi annettu reaktio on prosessi, jota kutsutaan esteröintiin, jossa esteri saadaan reaktiolla alkoholin ja karboksyylihappon välillä. Tässä tapauksessa se tapahtuu metanolin ja salisyylihapon välillä, kuten alla on esitetty:
CH3OH + C7H6JOMPIKUMPI3 → C8H8JOMPIKUMPI3 + H2JOMPIKUMPI
On huomattava, että hydroksyylialkoholilla (OH).
Joten mitä näiden kahden kemiallisen lajin välillä tapahtuu, on kondensaatioreaktio, koska vesimolekyyli poistetaan reagenssien kesken, kun taas muut reagoivat lajit tiivistetään metyylisalisylaatin saamiseksi.
Seuraava kuva näyttää metyylisalisylaatin synteesin salisyylihaposta, missä esitetään kaksi peräkkäistä reaktiota.