Amorfinen kiintoaine rakenne, ominaisuudet, esimerkit

- 880
- 93
- Edgar VonRueden
Se kiinteä aine He ovat niitä, joilla ei ole järjestettyä pitkän aseman rakennetta. Ne ovat päinvastaisia kuin kiteinen kiinteä. Niiden hiukkaset liittyvät sotkuisella tavalla, samanlaisia kuin nesteitä, mutta riittävällä voimalla koheesioon kiinteässä rakenteessa.
Tämä amorfinen luonne on yleisempi kuin voitaisiin ajatella; Itse asiassa yksi mahdollisista valtioista, jotka tiivistetty aine voi hyväksyä. Tämä ymmärtää, että mikä tahansa yhdiste, joka kykenee kiinteyttämään ja siten kiteyttämään, voidaan myös kiinnittää häiriöllisesti, jos kokeelliset olosuhteet sallivat sen.
 Sokeripuuvilla on esimerkki kiinteästä amorfisesta. Lähde: Pixabay.
Sokeripuuvilla on esimerkki kiinteästä amorfisesta. Lähde: Pixabay. Yllä olevaa käytetään yleensä puhtaisiin aineisiin, ovatko elementit tai yhdisteet. Mutta se on myös pätevä seosten tapauksessa. Monet kiinteät seokset ovat amorfisia, kuten sokerin, suklaan, majoneesin tai perunasoseen puuvillaa.
Se, joka kiinteä on amorfinen, ei tee siitä vähemmän arvokasta kuin kiteinen. Rakenteellinen häiriö antaa sille joskus ainutlaatuisia ominaisuuksia, joilla ei ole kiteistä tilaa. Esimerkiksi amorfinen pii on suositeltava aurinkosähköteollisuudessa ennen linssiä tietyille pienimuotoisille sovelluksille.
[TOC]
Amorfisten kiinteiden aineiden rakenne
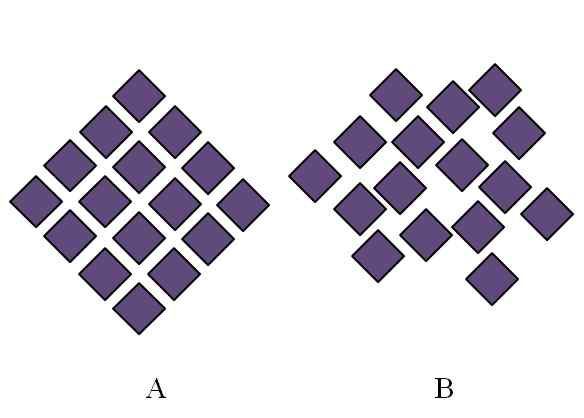 Ero kiteisen rakenteen ja amorfisen rakenteen välillä. Lähde: Gabriel Bolívar.
Ero kiteisen rakenteen ja amorfisen rakenteen välillä. Lähde: Gabriel Bolívar. Amorfisen kiinteän aineen rakenne on sotkuinen; Siitä puuttuu jaksollisuus tai rakenteellinen kuvio. Ylivoimainen kuva kuvaa tätä asiaa. Se vastaa kiteistä kiinteää ainetta, kun taas B edustaa kiinteää amorfista. Huomaa, että B -purppuran rhombusten on järjestetty mielivaltaisesti, jopa kun molemmat ja B on samantyyppisiä vuorovaikutuksia.
Voi palvella sinua: Fenolphthalein (C20H14O4)Jos B näkyy myös, nähdään, että on tiloja, jotka näyttävät olevan tyhjiä; toisin sanoen rakenne aiheuttaa vikoja tai väärinkäytöksiä. Siksi osa amorfisen kiinteän aineen mikroskooppisesta tai sisäisestä häiriöstä johtuu siitä, että sen hiukkaset "sopivat" siten, että tuloksena olevalla rakenteella on monia puutteita.
Aluksi laajuus tehtiin amorfisten kiinteiden aineiden tilaamisasteessa. B: ssä on tuskin pari roomia, jotka näyttävät olevan linjassa järjestyksessä. Alueita voidaan olla; Mutta vain lyhyellä alueella.
Sitten sanotaan, että amorfinen kiinteä aine on valmistettu mittaamattomista kiteistä, jotka ovat pieniä eri rakenteita. Kaikkien näiden rakenteiden summa päätyy labyrintiiniin ja merkityksettömään: globaalista rakenteesta tulee amorfinen, koostuva joukosta kiteisiä lohkoja, jotka ovat hajallaan kaikkialla.
Ominaisuudet
Amorfisen kiinteän kiinteän kiinteän kiinteiden hiukkasten luonteen ominaisuudet vaihtelevat. On kuitenkin tiettyjä yleisiä ominaisuuksia, jotka voidaan mainita. Amorfiset kiintoaineet voivat olla lasimaisia, kun niiden näkökohdat ovat kistalla kaltaisia näkökohtia; tai jielnelous, hartsimainen tai pölyinen.
Niiden sotkuiset rakenteet eivät tuota luotettavia X -ray -diffraktiospektriä. Sen sulamispisteet eivät myöskään ole tarkkoja, mutta kattavat arvojen väliaika.
Esimerkiksi amorfisen kiinteän aineen sulamispiste voi vaihdella 20 - 60 ºC. Sillä välin kiteiset kiinteät aineet sulavat tietyllä lämpötilassa tai kapealla aikavälillä, jos ne sisältävät monia epäpuhtauksia.
Toinen amorfisten kiinteiden aineiden ominaisuus on, että kun ne rikkoutuvat tai murtuvat, ne eivät aiheuta geometrisiä ja litteitä pintoja, vaan epäsäännöllisiä fragmentteja, joissa on kaarevat kasvot. Kun ne eivät ole lasimaisia, ne esitetään pölyisinä ja läpinäkymättöminä kappaleilla.
Se voi palvella sinua: AliLo: Allyic Unit, Carbocation, Radical, EsimerkitValmistautuminen
Enemmän kuin amorfinen kiinteä kiinteä, on kätevää käsitellä tätä käsitettä "amorfisena tilana". Kaikki yhdisteet (ioninen, molekyyli, polymeerinen, metalli jne.) Ne kykenevät jossain määrin, ja jos kokeelliset olosuhteet sallivat sen, muodostavat amorfisia ja ei -kiteisiä kiinteitä aineita.
Esimerkiksi orgaanisessa synteesissä kiinteät yhdisteet saadaan alussa pölyisinä massoina. Sen epäpuhtauksien pitoisuus on niin korkea, että nämä vaikuttavat sen pitkän matkan molekyylijärjestykseen. Siksi, kun tuote palautetaan uudestaan ja uudestaan, kiinteä aine muuttuu yhä kiteisemmäksi; menettää amorfisen hahmonsa.
Tämä ei tarkoita, että amorfiset kiintoaineet ovat välttämättä epäpuhtaita materiaaleja; Useat heistä ovat amorfisia omaa kemiallista luonnettaan.
Puhdas aine voi kiinteyttää amorfisesti, jos neste jäähtyy voimakkaasti, niin että niiden hiukkaset eivät kiteytyy, vaan omaksuvat lasimaisen kokoonpanon. Jäähdytys on niin nopeaa, että hiukkasilla ei ole tarpeeksi aikaa sovittaa tuskin "syntyneet" kiteiset lohkot.
Esimerkiksi vesi pystyy olemaan lasimaisessa tilassa, amorfisessa, eikä vain jään tavoin.
Esimerkkejä amorfisista kiinteistä aineista
Mineraalit ja muovi
 Obsidian on yksi harvoista amorfisista mineraaleista, jotka tunnetaan. Lähde: Pixabay.
Obsidian on yksi harvoista amorfisista mineraaleista, jotka tunnetaan. Lähde: Pixabay. Lähes mikä tahansa kiteinen materiaali voi sopeutua amorfiseen muotoon (ja päinvastoin). Näin tapahtuu joidenkin mineraalien kanssa, jotka geokemiallisista syistä ei voinut muodollisesti vahvistaa heidän tavanomaisia kiteitään. Toisaalta toiset eivät muodosta kiteitä, vaan lasia; Näin on obsidian.
Toisaalta polymeerit yleensä kiinteyttävät amorfisesti, koska niiden molekyylit ovat liian suuria määrittelemään järjestettävä rakenne. Tässä ovat hartsit, kuivia, polystyreenivaahtoa (anime), muovit, teflon, baquelita, muun muassa.
Voi palvella sinua: esteritBiologinen kudos
Biologiset kiinteät aineet ovat enimmäkseen amorfisia, kuten: elinkudos, iho, hiukset, sarveiskalvo jne. Myös rasva ja proteiinit muodostavat amorfisia massoja; Riittävällä valmistuksella ne voivat kuitenkin kiteyttää (DNA -kiteet, proteiinit, rasvat).
Lasi
 Lasi, amorfinen kiinteä kiinteä
Lasi, amorfinen kiinteä kiinteä Vaikka melkein viimeinen, edustavin amorfinen kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä kiinteä aine on itse lasi. Sen koostumus on pohjimmiltaan sama kuin kvartsin: SiO2. Sekä kvartsikide että lasi ovat kolmiulotteisia kovalenttisia verkkoja; Vain lasiverkko on sotkuinen, eripituuksilla olevat si-tai linkit.
 Metallilasinäyte
Metallilasinäyte Lasi on amorfinen kiinteä par excellence, ja samanlaisen ulkonäön hankkimien materiaalien sanotaan olevan lasimainen tila.
Hiili- ja metallit
Meillä on amorfinen hiili, joka on hiili aktivoitu yksi tärkeimmistä sen absorboivista kyvyistä. Siellä on myös piitä ja Saksa amorfisia, elektronisilla sovelluksilla, joissa ne toimivat puolijohdina.
Ja lopuksi, on amorfisia seoksia, että niiden mukautuneiden metalliatomien eron vuoksi ne eivät muodosta kiteistä rakennetta.
Viitteet
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Rachel Bernstein ja Anthony Carpi. (2020). Kiinteiden aineiden ominaisuudet. Toipunut: VisionLearning.com
- Wikipedia. (2020). Amorfinen kiinteä. Haettu: vuonna.Wikipedia.org
- Richard Zallen, Ronald Walter Douglas ja muut. (31. heinäkuuta 2019). Amorfinen kiinteä. Encyclopædia britannica. Toipunut: Britannica.com
- Elsevier B.V. (2020). Amorfinen kiinteä. Tiede. Haettu: ScienEdirect.com
- Danielle Reid. (2020). Amorfinen kiinteä: Määritelmä ja esimerkki. Opiskelu. Toipunut: Opiskelu.com
- Rubikin kuutiotaide. (2008). Mikä on amorfinen materiaali? Haettu: Web.Fysiikka.UCSB.Edu
- « Sosiaalinen roolikonsepti Talcott Parsonsin, tyyppien ja esimerkkien mukaan
- Kiteiset kiinteät rakenteet, ominaisuudet, tyypit, esimerkit »

