Typtofaanin ominaisuudet, rakenne, toiminnot, edut
- 3920
- 487
- Shawn Stanton II
Hän Tryptofaani (TRP, W) on aminohappo, joka on luokiteltu välttämättömien aminohappojen ryhmään, koska ihmisen organismi ei pysty syntetisoimaan sitä ja sen on saatava se ruokavalion kautta.
Jotkut elintarvikkeet, kuten maito ja niiden johdannaiset, lihat, munat ja jotkut viljat, kuten quinoa ja soija, sisältävät välttämättömiä aminohappoja, ja siksi ne ovat tärkeä tryptofaanin lähde.
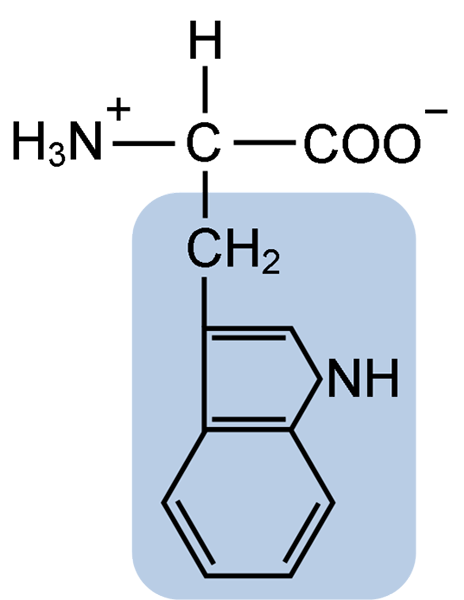
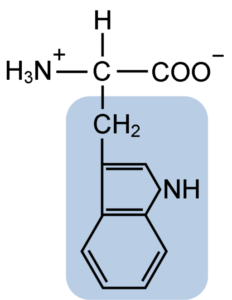 Typtofaanin aminohapon kemiallinen rakenne (lähde: Clavecin [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)] Wikimedia Commonsin kautta)
Typtofaanin aminohapon kemiallinen rakenne (lähde: Clavecin [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)] Wikimedia Commonsin kautta) Luonnossa tunnetaan yli 300 erilaista aminohappoa ja vain 22 muodostaa soluproteiinien monomeeriset yksiköt. Jälkimmäisten joukossa 9 on välttämättömiä aminohappoja, mukaan lukien tryptofaani, kunkin olennaisuus eroaa yhden lajin ja toisen välillä.
Tryptofaanilla on erilaisia toimintoja, joista niiden osallistuminen proteiinisynteesiin, serotoniinin synteesissä, joka on voimakas verisuontenstriktori ja välittäjäaine, melatoniinin ja CO -Founder NAD: n synteesi.
Kasvien valtakunnassa tryptofaani on auksiinina tunnetun kasvihormonin perustavanlaatuinen edeltäjä (indoli-3-etikkahappo). Jotkut bakteerit voivat syntetisoida sen, kuten JA. koli Corismatosta, jota tuotetaan joistakin glykolyyttisistä johdannaisista, kuten fosfoenoliruvatoitu ja erytrosa-4-fosfaatti.
Sen hajoaminen nisäkkäissä tapahtuu maksassa, missä sitä käytetään asetyylikoentsyymin A (asetyyli-CoA) synteesiin, ja tästä syystä sitä kuvataan aminohappo kutsuu glukogeeniseksi, koska se voi päästä glukoosimuodostussykliin.
Tryptofaanin käyttöön liittyvät kiistanalaiset tulokset on raportoitu erilaisilla tutkimuksilla ruokavalion lisäravinteena joidenkin patologioiden, kuten masennuksen ja joidenkin unihäiriöiden, hoitoon.
Aminohappojen aineenvaihdunnan synnynnäisiin vikoihin liittyy joitain sairauksia. Typtofaanin tapauksessa Hartnupin tauti voidaan nimittää tryptofaanin -2,3 -monoksigenaasin, recessiivisen perinnöllisen taudin vuoksi, jolle on ominaista henkinen hidastuminen ja ihotyyppisen pelagra -tyypin muutokset ja muutokset Pelagra -tyyppinen.
[TOC]
Ominaisuudet
Yhdessä fenyylialaniinin ja tyrosiinin kanssa tryptofaania löytyy aromaattisten ja hydrofobisten aminohappojen ryhmästä.
Tryptofaanille on kuitenkin ominaista olla hiukan hydrofobinen aminohappo sen aromaattisen sivuketjun jälkeen, sillä polaariset ryhmät heikentävät tätä hydrofobisuutta.
Yhdistettyjen renkaiden vuoksi niillä on voimakas valon imeytyminen spektrialueella lähellä ultraviolettia, ja tätä ominaisuutta käytetään usein proteiinien rakenteellisiin analyyseihin.
Se imee ultraviolettivaloa (välillä 250 - 290 nm) ja vaikka tämä aminohappo ei ole kovin runsaasti suurimman osan ihmiskehon proteiinien rakenteessa, sen läsnäolo edustaa tärkeätä vaikutusta valon valon imeytymiskykyyn alueen alueella 280 nm useimmista proteiineista.
Tryptofaanin päivittäiset vaatimukset eroavat iän myötä. 4–6 kuukauden imeväisillä keskimääräinen tarve on noin 17 mg kilogrammaa painoa päivässä; 10–12 -vuotiailla lapsilla se on 3,3 mg kilogrammaa painoa päivässä ja aikuisilla se on 3,5 mg kilogrammaa päivässä päivässä.
Tryptofaani absorboi suolen reitti ja on ketogeeninen ja glykogeeninen aminohappo samanaikaisesti.
Koska se on serotoniinin edeltäjä, tärkeä välittäjäaine, tryptofaanin on päästävä keskushermostoon (CNS) ja tämän vuoksi sen on ylitettävä veren aivoesde, jolle on olemassa erityinen aktiivinen kuljetusmekanismi.
Voi palvella sinua: Biggy Agar: Perusta, valmistelu ja käyttötarkoituksetRakenne
Tryptofaanilla on molekyylinen kaava C11H12N2O2 ja tällä välttämättömällä aminohapolla on aromaattinen sivuketju.
Kuten kaikki aminohapot, tryptofaanilla on aminoharyhmään kiinnitetty a -hiiliatomi (NH2), vetyatomiin (H), karboksyyliryhmään (COOH) ja sivuketjuun (R), jotka on muodostettu heterosyklisellä rakenteella, indoliryhmällä.
Sen kemiallinen nimi on 2-amino-3-propionihappo, sen molekyylimassa on 204,23 g/mol. Sen liukoisuus 20 ° C: ssa on 1,06 g 100 g vettä ja tiheys on 1,34 g/cm3.
Funktiot
Ihmisessä tryptofaania käytetään proteiinisynteesiin ja se on välttämätöntä serotoniinin muodostumiselle (5-hydroksitriptamiini) voimakas vasokonstriktori, stimuloimalla sileän lihaksen supistumista (etenkin ohutsuolessa) ja neurotransmitterin, joka kykenee tuottamaan psyykkistä stimulaatiota, combat masennuksen masennusta ja säätele ahdistusta.
Tryptofaani on melatoniinin synteesin edeltäjä, ja siksi sillä on vaikutuksia unen ja valppauden sykliin.
Mainittu aminohappoa käytetään esiasteena yhdellä kolmesta tapaa NAD-kofaktorin muodostumiseen, erittäin tärkeään kofaktoriin, joka osallistuu moniin entsymaattisiin reaktioihin, jotka liittyvät oksidin vähentämistapahtumiin.
Tryptofaania ja joitain sen prekursoreista käytetään kasvillisuushormonin muodostumiseen, jota kutsutaan auksiiniksi (indol-3-aktiivinen happo). Auksiinit ovat kasvihormoneja, jotka säätelevät kasvien kasvua, kehitystä ja monia muita fysiologisia toimintoja.
Biosynteesi
Organismeissa, jotka kykenevät syntetisoimaan sitä, tryptofaanin hiili luuranko on peräisin fosfoenolypyruvaatista ja erytrosa-4-fosfaatista. Nämä puolestaan muodostuvat Krebs -syklin välittäjältä: oksalastaatti.
Fosfoenoliruvaattia ja erytryhmä-4-fosfaattia käytetään korismaattisynteesiin seitsemällä entsymaattisella reitillä. Fosfoenoliruvaatti (PEP) on glykolyysin ja pentoosifosfaattireitin erytryhmä-4-fosfaatin tuote.
Kuinka corismate -synteesireiti?
Korismato-oireiden ensimmäinen vaihe on PEP: n liitokset erytrosa-4-fosfaatin kanssa 2-Zo-3-disoxxi-d-anabino-heptulosonato-7-fosfaatin (DAHP) (DAHP) muodostamiseksi (DAHP) (DAHP).
Tätä reaktiota katalysoi entsyymi 2-Zo-3-Dexxi-D-anabino-heptulosonato-7-fosfaattisyntaasi (DAHP Syntasa), jota korisaatti estää.
Toinen reaktio merkitsee DAHP: n siklaatiota syntaasin dehydrokinaatin, entsyymin, joka vaatii co -tekijän NAD: n, joka vähenee tämän reaktion aikana; Seurauksena on, että 5-dishydrokinaattia tapahtuu.
Tämän reitin kolmas vaihe viittaa 5-dehydrokinaatin vesimolekyylin eliminointiin, reaktio, jota katalysoi entsyymi-dehydraasi-dehydrokinaali, jonka lopputuote vastaa 5-dishydro Shikimato.
Tämän molekyylin ketoryhmä pelkistetään hydroksyyliryhmään ja sen seurauksena Shikimato muodostuu. Tätä reaktiota katalysoi entsyymi on NADPH-riippuvainen riippuvainen riippuvainen riippuvainen riippuvainen.
Reitin viides vaihe merkitsee 5-fosfaatti-shikimaation muodostumista ja ATP-molekyylin kulutusta entsyymillä, joka tunnetaan nimellä Kinaasi Shikimato, joka vastaa shikimaation fosforylaatiota asennossa 5.
Myöhemmin 5-fosfaatin shikimaatista ja 3-enlappiruvil Shikimato-5-fosfaattisyntaasin vaikutuksesta, 3-enlappiruvil Shikimato 5-fosfaatti syntyy. Edellä mainittu entsyymi edistää toisen PEP-molekyylin fosforyyliryhmän siirtymistä hiilen hydroksyyliryhmällä. 5-fosfaattisen shikimaation asennossa 5.
Se voi palvella sinua: miksi on tärkeää huolehtia biologisesta monimuotoisuudesta?Seitsemännen ja viimeisen reaktion katalysoi syntaasin korismi, joka eliminoi fosfaatin 3-enlappate-shikimatimasta 5-fosfaatista ja tekee siitä korisoitteen.
Sienissä N. Crassa, Yksi monitoiminen entsymaattinen kompleksi katalysoi viisi tämän reitin seitsemästä reaktiosta ja tämä kompleksi lisätään kolme muuta entsyymiä, jotka lopulta tuottavat tryptofaania.
Tryptofaanisynteesi bakteereissa
Sisään JA. koli, Tryptofaanikorismin muutos sisältää viisi ylimääräistä entsymaattista reittiä:
Ensinnäkin antranilaatin syntaasentsyymi muuntaa korisminan antranilaateiksi. Tässä reaktiossa osallistuu glutamiinimolekyyli, jonka luovuttaa aminoheryhmä, joka sitoutuu tryptofaanin indolirenkaan ja tulee glutamaatiksi.
Toista vaihetta katalysoi fosforibosyylitransferaasin antranilaatti. Tässä reaktiossa 5-fosforribosyyli-1-pyrofosfaatin (PRPP) (PRPP) (PRPP) pyrofosfaattimolekyyli liikkuu runsaasti energiaa, ja N- (5'-fosforribosyyli) muodostuu.
Tämän tryptofaanisynteesireitin kolmas reaktio merkitsee fosforribosyyli-isomeraasientsyymin osallistumista. Tässä N- (5'-Phorribosyyli) -santranylotti.
Myöhemmin indoli-3-glyserolifosfaatti muodostuu reaktiossa, jota katalysoi indol-3-glyserolin sympatian syntaasi, jossa CO2 ja H2O-molekyyli vapautuu ja 1- (O-karboksyphenyyliamiini) -1-desoksyyribulosa 5 -fosfaatti.
Tämän reitin viimeinen reaktio lopulta muodostaa tryptofaanin, kun tryptofaanisyntaasi katalysoitu.
Heikkeneminen
Nisäkkäissä tryptofaani hajoaa maksassa asetyyli-CoA: ksi reitillä, johon liittyy kaksitoista entsymaattista vaihetta: kahdeksan a-zo-stodipaatin saavuttamiseksi ja vielä 4 muuta α-zo-dotadipaton muuttamiseksi asetyylikoentsyymiksi.
Hajoamisjärjestys, kunnes α-ceetadipato on:
Typtofaani → N-Kinureniiniformil → kinureniini → 3-hydroksi kinureniini → 3-hydroksi-antranilaatti → ε-semialdehydi 2-amino-3-muconcycix paljon → ε-semialdehido a-amino Muconic Amouz.
Näitä reaktioita katalysoivat entsyymit ovat:
Typtofaani 2-3-dioksigenaasi, formamidaasi-kinureniini, NADPH-riippuvainen monooksigenaasi NADPH-riippuvainen.
Kun a-cethoadipate on muodostettu, oksidatiivinen dekarboksylaatio muodostuu gluteral-CoA: sta. Tämä ß-hapettumisella glutakonyyli-CoA-muodossa, joka menettää bikarbonaattihiiliatomin (HCO3-), voittaa vesimolekyylin ja päättyy Crotonil-CoA: na.
Crotonil-CoA, myös ß-hapettumista varten, tuottaa asetyyli-CoA: n. Mainittu asetyyli-CoA voi noudattaa useita tapoja, joiden joukossa glukoneogeneesi muodostaa glukoosin ja Krebs-syklin, ATP: n muodostamiseksi tarvittaessa tarvittaessa, tarvittaessa.
Tämä molekyyli voidaan kuitenkin suunnata myös ketonirunkojen muodostumiseen, joita voidaan lopulta käyttää energialähteenä.
Ruoat, joissa on rikas tryptofaania
Punainen liha yleensä kana ja kalat (erityisesti siniset kalat, kuten lohi ja tonnikala) ovat erityisen runsaasti tryptofaania. Maito ja sen johdannaiset, munat, erityisesti keltuainen, ovat myös ruokia, joissa on runsaasti tryptofaanisisältöä.
Muita ruokia, jotka toimivat tämän aminohapon luonnollisena lähteenä, ovat:
- Pähkinät, kuten pähkinät, mantelit, pistaasipähkinät ja anacardot, muun muassa.
- Riisivilat.
- Kuivat jyvät, kuten pavut, linssit, kahviherneet, soijapavut, quinoa jne.
- Oluthiiva ja tuoreet pavut, banaanit ja banaanit, ananas tai ananá, avokado, luumut, vesikrassi, parsakaali, pinaatti ja suklaa.
Se voi palvella sinua: sukellusvene haisi: historia, todellisuus tai fiktio?Saannisi edut
Typtofaanin kulutus on ehdottoman välttämätöntä kaikkien niiden proteiinien syntetisoimiseksi, jotka sisällyttävät sen rakenteeseensa, ja sen eri toimintojen kautta se mahdollistaa mielialan, unen ja valppausjaksojen säätämisen sekä monenlaisia biokemiallisia prosesseja, joihin NAD osallistuu.
Tunnelman tunnettujen vaikutusten lisäksi serotoniini (tryptofaaniryhmä) puuttuu useisiin oppimiseen ja muistiin liittyviin kognitiivisiin toimintoihin, jotka siksi liittyvät myös tryptofaaniin.
On tietoja, jotka osoittavat mielialan, serotoniinin ja maha-suolikanavan ja akselin välisen suhteen kaksisuuntaisten vaikutusten järjestelmänä aivojen emotionaalisten ja kognitiivisten keskuksien ja ruuansulatuksen perifeerisen toiminnan välillä.
Käyttö ruokavalion lisäyksenä joidenkin häiriöiden, etenkin keskushermostoon liittyvien häiriöiden hoitoon, on ollut erittäin kiistanalainen, koska sen kilpailukykyinen kuljetus neutraalien aminohappojen kanssa, paljon runsaampi, vaikeuttaa tryptofaanin merkittävien ja jatkuvien lisääntymisten saavuttamista jälkeen sen suun kautta annettava hallinto.
Näistä kiistoista huolimatta sen käyttö on oletettu apulaisena:
- Kipuhoito
- Univaikeudet
- Masennushoito
- Maniahoito
- Ruokahalun vähentäminen
Puutoshäiriöt
Keskeiseen eliminointiin tai tryptofaanin puutteeseen liittyy masennus, huomion epäonnistumiset, muistin väheneminen, unen ja ahdistuneisuushäiriöt.
Masentuneista potilaista ja itsemurha -suuntauksista on löydetty muutoksia veren ja aivo -selkäydinnesteen pitoisuuksiin. Lisäksi joillakin hermostuneiden anoreksian potilailla on alhainen seerumin tryptofaanitasot.
Joillakin polyurisilla potilailla, jotka menettävät B6 -vitamiinin ja sinkin, on usein fobioita ja ahdistusta ja paranevat ravinnon lisäravinteilla, joissa on runsaasti triptofaania.
Karsinoidioireyhtymälle on ominaista pienen suolen kasvainten läsnäolo, jotka aiheuttavat ripulia, verisuonitauteja ja keuhkoputkien supistumista ja liittyvät niasiini- ja tripofaanin alijäämään
Pelagra on patologinen tila, johon liittyy ripuli, dementia, ihottuma ja voi aiheuttaa kuolemaa, tätä hoidetaan myös niasiini- ja tryptofaanilisäaineilla.
Hartnupin taudin on tehtävä joistakin asioista, joilla on vika useiden aminohappojen aineenvaihdunnassa, mukaan lukien tryptofaani.
Typtofaanin -2,3-monoksigenaasientsyymin alijäämän tapauksessa tämä on recessiivinen perinnöllinen sairaus, jolle on ominaista henkinen vajaatoiminta ja ihotyyppinen ihon muutokset.
Viitteet
- Halvorsen, k., & Halvorsen, S. (1963). Hartnup -tauti. Lastenlääketiede, 31(1), 29-38.
- S, s. D -d., Kello, c. J -., Argyropoulos, S. V., & Nutt, D. J -. (2016). Donin paniikki. Opas tryptofaanin ehtymiseen häiriökohtaisella ahdistuksen provokaatiolla. Lehti psykofarmakologiasta, 30(11), 1137-140.
- Jenkins, t. -Lla., Nguyen, J. C., Polglaze, k. JA., & Bertrand, P. P. (2016). Tryptofaanin ja serotoniinin vaikutus mielialaan ja kognitioon, jolla on mahdollinen rooli suolisto-akselilla. Ravintoaineet, 8(1), 56.
- Kaye, W. H., Barbarich, n. C., Putnam, k., Gendall, k. -Lla., Fernstrom, J., Fernstrom, m.,… & Kishore, a. (2003). Akuutin tryptofaanin ehtymisen anoreksia nervosassa. Kansainvälinen syömishäiriöiden lehti, 33(3), 257-267.
- Murray, r. K -k -., Granner, D. K -k -., Mayes, P., & Rodwell, V. (2009). Harperin kuvitettu biokemia. 28 (p. 588). New York: McGraw-Hill.
- Nelson, D. Lens., Lehninger, a. Lens., & Cox, M. M. (2008). Lehninger -biokemian periaatteet. Macmillan.

