Etyleenioksidirakenne, ominaisuudet, riskit ja käytöt
- 4693
- 702
- Shawn Stanton II
Hän etyleenioksidi Se on epoksidien perheen orgaaninen yhdiste. Huoneen lämpötilassa se on kaasumainen, väritön ja vaikka se on melkein wc, sillä on pehmeä makea haju, samanlainen kuin eetterien haju.
Se on erittäin monipuolinen kemiallinen rakennuslohko, koska sitä käytetään monenlaisissa teollisuussovelluksissa muiden kemiallisten yhdisteiden valmistukseen, joissa on useita käyttötarkoituksia. Tämä johtuu sen korkeasta reaktiivisuudesta, toisin sanoen sen helppoutta reagoida muiden aineiden kanssa.
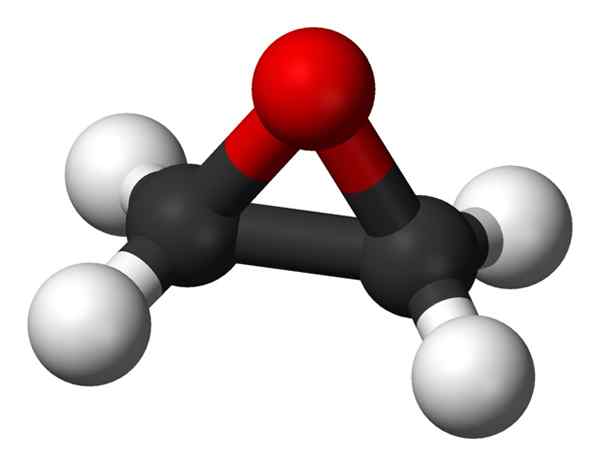
 Etyleenioksidin alueellinen rakenne. Mustat pallot: hiiliatomit; Valkoiset pallot: vetyatomit; Punainen pallo: happiatomi. Benjah-BMM27 [julkinen alue]. Lähde: Wikimedia Commons.
Etyleenioksidin alueellinen rakenne. Mustat pallot: hiiliatomit; Valkoiset pallot: vetyatomit; Punainen pallo: happiatomi. Benjah-BMM27 [julkinen alue]. Lähde: Wikimedia Commons. Yksi sen tärkeimmistä sovelluksista on raaka -ainetta jäätymisautojen säteilijöiden antifreeze -komponenttien valmistuksessa. Sen johdannaisia käytetään teollisuus- tai kodinpuhdistusaineiden, kosmeettisten tuotteiden ja shampoiden, plastisointi-, lääkevalmisteiden tai voiteiden ainesosina.
Se on laajalti käytetty desinfiointiaine, esimerkiksi lääketieteellisten ja hammaslääketieteellisten laitteiden steriloinnissa, koska se pystyy tuhoamaan virukset, bakteerit, sienet ja itiöt, etenkin kuivissa olosuhteissa. Lisäksi sitä on käytetty pakattujen elintarvikkeiden haisemiseen, vaikka tämä käyttö kyseenalaistetaan.
Hyödyllisyydestään huolimatta sitä on manipuloitava erittäin varovaisesti, koska se voi aiheuttaa silmien ja ihon ärsytystä. Eteenioksidin hengittäminen pitkään voi vaikuttaa hermostoon. Siksi ihmisten tai ratkaisuille altistuneiden ihmisten on käytettävä suojavarusteita ja vaatteita.
[TOC]
Rakenne
Sen molekyyl kaava on c2H4JOMPIKUMPI. Se kuuluu epoksidiryhmään, joka on yksinkertaisin ja tärkein näistä. Sen muoto on kolmen jäsenen rengas.
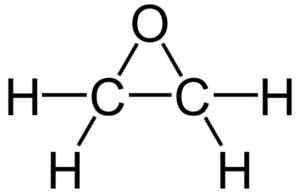 Etyleenioksidirakenne. Lähde: Wikimedia Commons
Etyleenioksidirakenne. Lähde: Wikimedia Commons Kolmionmuotoisen rengasrakenteensa vuoksi etyleenioksidi on erittäin reaktiivinen, mikä johtuu renkaan avautumisesta. Linkkikulut ovat keskimäärin 60º, mikä tekee niiden linkeistä heikot. Molekyyli on vähemmän stabiili kuin lineaarinen eetteri ja pyrkii reagoimaan helposti muiden kemiallisten yhdisteiden kanssa.
Voi palvella sinua: natriumnitriitti (nano2): rakenne, ominaisuudet, käytöt, riskitOminaisuudet
Muut nimet
- Oksyran.
- Epoksitano.
Fyysinen tila
Huoneenlämpötilassa ja ilmakehän alaisessa paineessa se on kaasu. Alle 10,6 ºC ja ilmakehän paineen alaisena, se on neste. Alle -111 ºC on kiinteä.
Molekyylipaino
44,05 g/mol.
Leimahduspiste
Alle 0 ºF (-17,8 ºC).
Tiheys
Sen tiheys on pienempi kuin veden tiheä, koska se on 0,882 - 10 ºC. Heidän höyrynsä puolestaan ovat raskaampia kuin ilma.
Liukoisuus
Se liukenee veteen, bentseeniin, asetoniin, etanoliin ja eetteriin. Se on sekoittumassa hiilitetrakloridin kanssa.
Itsensuuntainen lämpötila
428,9 ºC.
Muut ominaisuudet
- Jos se lämmittää lämmitys tai saastuminen, se voi polymeroida eksotermisesti (tuottaa suuren määrän lämpöä). Jos polymerointi tapahtuu säiliön sisällä, se voidaan rikki väkivaltaisesti.
- Voi reagoida hapettavien materiaalien kanssa.
- Se on erittäin myrkyllinen, syöpää ja hyviä mutaatioita generaattorina bakteereissa ja nisäkässoluissa.
Tuotanto
Teollisessa mittakaavassa se valmistetaan hapettamalla eteeni happea (tai2) ilmasta. Tämän reaktion nopeutta lisääntyy hopeametallin (AG) ja lämpötilan vaikutuksen myötä. Seuraavaksi reaktio näkyy:
AG, 250ºC
2 c2H4 + JOMPIKUMPI2 -> 2c2H4JOMPIKUMPI
Etyleenioksidi
Riskejä
Terveydelle
- On todettu, että se tuottaa neurologisia häiriöitä ja että kuolema voi aiheuttaa. Alempi pitoisuus, joka voi tuottaa myrkyllisiä vaikutuksia hengittämällä, on 12.500 ppm/10 sekuntia (ppm tarkoittaa: osat miljoonaa).
- Se on voimakas ärsyttävä iho, silmät ja hengitystie.
Voi palvella sinua: Samario: Ominaisuudet, rakenne, hankkiminen, käyttötarkoitukset- Höyryn altistuminen korkealla eteenioksidin pitoisuudella voi aiheuttaa silmien ärsytystä, silmukalvon tulehduksia ja sarveiskalvovaurioita.
- Kaihien kehitykseen on liitetty altistuminen heidän höyryille ja roiskeille. Keskittyneillä liuoksilla silmille aiheutuu vakavia vaurioita.
- Eteenioksidin vesipitoisten liuosten kosketus ihon kanssa aiheuttaa ärsytystä ja voi johtaa vakavaan ihottumaan ampulleilla ja palovammaisilla.
- Sen hengitys voi vaikuttaa hermostoon, aiheuttaen päänsärkyä ja pahoinvointia muun muassa oireiden joukossa.
Antaa potkut
- Kun altistuu liekkille tai lämmölle, on räjähdyksen vaara. Lämmitettyä ne tuottavat vaarallisia höyryjä.
- Höyry muodostaa räjähtäviä seoksia, joissa on ilma monissa pitoisuuksissa.
- Sitä tulisi välttää sen manipulointi laitteilla, jotka sisältävät metalleja, kuten kuparia, hopeaa, elohopeaa, magnesiumia, alumiini- tai rautaoksideja, samoin kuin välttämään muun muassa ammoniakkia, hapettavia aineita, happoja tai orgaanisia emäksiä. Kaikki nämä materiaalit voivat nopeuttaa niiden polymerointia ja/tai räjähdyksiä.
Sovellukset
Teollisuussovellus
Sitä käytetään välittäjänä muiden kemikaalien tuotannossa, joita puolestaan käytetään polyesterikuitujen valmistuksessa vaatteiden, verhoilun, mattojen ja tyynyjen valmistuksessa.
Etyleenioksidilla etyleeniglykolia käytetään jäätymisajoneuvoissa ajoneuvojen moottoreissa. Etyleeniglykolia käytetään myös lasikuituvalmistuksessa ja muovikalvoissa pakkaamiseen.
Muita eteenioksidista tuotettuja kemikaaleja ovat ei -ioniset pinta -aktiiviset aineet, joita käytetään pesuaineissa ja kaavoissa astiat pesemään.
Voi palvella sinua: Isobutil: nimikkeistö, koulutus, rakenne ja ominaisuudetLääketieteelliset sovellukset
Sitä käytetään lääkinnällisten laitteiden steriloivana aineena, kuten kirurgiset instrumentit, ihohenkilöt ja injektorit tai proteesit.
Sitä käytetään myös koneiden sterilointiin hemodialyysiin, laboratoriolaitteisiin, hammaslääketieteellisiin instrumentteihin, eläinlääketieteellisiin instrumentteihin, lämpömittareihin, kirurgisiin vaatteisiin tai ensiapuvälineisiin.
 Sterilointihuone. Lähde: Pixabay.com
Sterilointihuone. Lähde: Pixabay.com Vaikka lääketieteellisten laitteiden sterilointiin on saatavana useita menetelmiä, joissakin käyttötarkoituksissa ei ole käytettävissä olevaa hoitoa ei voi korvata eteenioksidin.
Tämä pätee tiettyjen lämpöherkkyyden ja säteilyn sterilointiin, samoin kuin joitain instrumentteja ja esineitä, jotka vaativat sterilointia itse sairaalopaikassa.
Kirjastot ja museot
Näissä paikoissa etyleenioksidia käytetään tuholaisten, kuten sienten ja hyönteisten, hallintaan. Tämä käyttö ei kuitenkaan ole niin yleistä ja sitä käytetään, kun muut vaihtoehdot eivät ole tehokkaita.
Maatalous ja ruoka
Sitä on käytetty torjunta -aineena, sienitarnaa, fumiganttia, rikkakasvien torjunta -aineita, hyönteismyrkkyä, jyrsijöitä, muun muassa. Vähentää merkittävästi bakteerien ja mausteiden sieniä.
Turvallisuus- ja ympäristöongelmien vuoksi etyleenioksidin käyttö elintarvikkeiden hakuutukseen on kuitenkin kielletty Euroopan unionissa ja Yhdysvalloissa.
Viitteet
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Eethyleenioksidi. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus
- Kemialliset turvallisuustiedot. (2019). Eethyleenioksidi. Talteenotettu kemikaalista.org
- Morrison, Robert Thornton; ja Boyd, Robert Neilson. 1992. Orgaaninen kemia. Prentice-sali.
- Moerman, f. ja mager, k. (2016). Puhdistaminen ja disffektio kuivien elintarvikkeiden jalostuslaitoksissa. Hygienian hallinnan käsikirjassa elintarviketeollisuudessa (toinen painos). Scientirectistä toipunut.com.
- Eastmond, David A. ja Balakrishnan, Sharada. (2010). Torjunta -aineiden genotoksisuus. Hayesin torjunta -aineiden toksikologian käsikirjassa (kolmas painos). ScienEdirect.com
- Atungulu, g.G. ja leipä, z. (2012). Pähkinöiden ja mausteiden mikrobinen puhdistaminen. Mikrobien puhdistamisessa elintarviketeollisuudessa. ScienEdirect.com
- « Rautaoksidi (II) rakenne, nimikkeistö, ominaisuudet, käyttää
- Yksinkertaiset tasaiset epiteeliominaisuudet, toiminnot ja tyypit »

