Acrilonitriilirakenne, ominaisuudet, tuotanto, käyttö

- 1210
- 339
- Shawn Stanton II
Hän aukko Se on orgaaninen yhdiste, jonka tiivistetty kaava on CHO2CHCN. Se on yksi yksinkertaisimmista nitrileistä, joita on olemassa. Kemia ja rakenteellisesti se ei ole muuta kuin vinyyliryhmän välisen unionin tuote, Cho2= CH- ja nitriili, syanidiryhmä, C≡N. Se on aine, jolla on suuri teollisuusvaikutus muovien maailmaan.
Fyysisesti se on väritön neste, jolla on tietty sipuli haju, ja se epäpuhtaassa tilassa on kellertäviä sävyjä. Se on erittäin syttyvä, myrkyllinen ja mahdollisesti syöpää aiheuttava, joten se luokitellaan erittäin vaaralliseksi aineeksi. Ironista kyllä, ne ovat valmistettuja muoveja ja leluja jokapäiväisestä elämästä, kuten Tupperware ja LEGO -lohkot.
 Acrilonitriil -polymeerejä on läsnä Tupperware -muovissa. Lähde: Stebulus Wikipedian kautta.
Acrilonitriil -polymeerejä on läsnä Tupperware -muovissa. Lähde: Stebulus Wikipedian kautta. Teollisuusasteikolla, Acrilonitriil. Lähes kaikki tuotettu määrä on tarkoitettu muovien valmistukseen, joka perustuu homopolymeereihin, kuten polyakryylinitriiliin, tai kopolymeereihin, kuten acrilonitriili-butadieeni-styreeniin.
[TOC]
Acrilonitriilirakenne
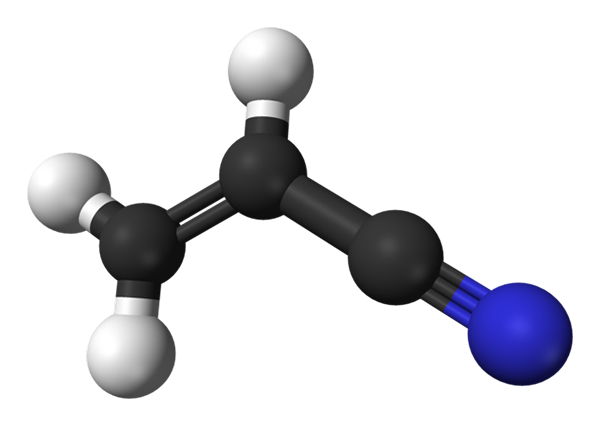 Acrilonitriilin molekyylirakenne. Lähde: Benjah-BMM27 / julkinen verkkotunnus
Acrilonitriilin molekyylirakenne. Lähde: Benjah-BMM27 / julkinen verkkotunnus Yläkuvassa on acrilonitriilimolekyyli, jota edustaa malli palloja ja palkkeja. Mustat pallot vastaavat hiiliatomeja, kun taas valkoinen ja sininen vety- ja typpiatomeihin, vastaavasti. Vasen, ch2= CH- vastaa vinyyliryhmää ja oikeaa syaaniryhmää, C≡N.
Koko molekyyli on tasainen, koska vinyyliryhmän hiilihiileillä on SP -hybridisaatio2. Samaan aikaan Ciano -ryhmän hiilellä on SP -hybridisaatio, joka on typpiatomin vieressä linjalla, joka lepää samalla tasolla kuin muu molekyyli.
CN -ryhmä myötävaikuttaa polaarisuuteen molekyyliin, joten molekyyli Cho2CHCN perustaa pysyvän dipolin, jossa korkein elektroninen tiheys on suunnattu typpiatomiin. Siksi dipoli-dipoli.
Voi palvella sinua: mikä on kemiallinen jaksollisuus?Molekyylit ch2CHCN ovat tasaisia, ja ne odottavat, että niiden kiteissä (jähmettyneet -84 ºC) niitä on saatavana toisilleen, kuten arkkeja tai paperiarkkeja, jotta heidän dipolit eivät hylkää.
Ominaisuudet
Fyysinen ulkonäkö
Väritön neste, mutta kellertävien sävyjen kanssa, kun se aiheuttaa joitain epäpuhtauksia. Kun niin, he suosittelevat sen tislaamista ennen sen käyttöä. Se on haihtuvaa ja sillä on myös voimakas haju kuin sipuli.
Moolimassa
53 064 g/mol
Sulamispiste
-84 ºC
Kiehumispiste
77 ºC
Leimahduspiste
-5 ºC (suljettu kuppi)
0 ºC (avoin kuppi)
Itsensuuntainen lämpötila
481 ºC
Tiheys
0,81 g/cm3
Höyryn tiheys
1,83 ilmassa.
Höyrynpaine
109 mmHg 25 ºC: n lämpötilassa
Liukoisuus
Vedessä sen liukoisuus on 74 g/l - 25 ºC. Acrilonitriili on myös huomattavasti liukoinen asetonin, öljyn, etanolin, etyyliasetaatin ja bentseenin etaniliin.
Hajoaminen
Kun termisesti vapauttaa myrkyllisen syanidin, hiilioksidit ja typpioksidit.
Tuotanto
Sohio -prosessi
Acryonitriili voi tapahtua massiivisten asteikkojen avulla lukuisten reaktioiden ja kemiallisten prosessien kautta. Kaikista niistä Sohio -prosessi on eniten käytetty, joka koostuu propeenin katalyyttisestä amaksidaatiosta. Fluidisarin reaktorissa propeenia sekoitetaan ilman ja ammoniakin kanssa lämpötilassa noin 400 ja 510 ºC, missä ne reagoivat kiinteissä katalyytteissä.
Reagenssit tulevat reaktoriin kerran, seuraavan reaktion tapahtuessa:
2CH3−CH = ch2 + 2 NH3 + 3 o2 → 2 ch2= CH-CÖN + 6 H2JOMPIKUMPI
Huomaa, että happi pelkistetään veteen, kun taas propeeni hapettaa acrilonitriilin. Siksi nimi 'amoksidaatio', koska se on hapettuminen, joka sisältää ammoniakin osallistumisen.
Voi palvella sinua: Keittäminen: Konsepti, tyypit ja esimerkitVaihtoehtoiset prosessit
Sohio -prosessin lisäksi voidaan mainita muita reaktioita, jotka sallivat acrilonitriilin saamisen. Ilmeisesti kaikki niistä eivät ole skaalautuvia tai ainakin riittävästi kannattavaa tapaa, eivätkä tuota tuotteita, joilla on korkea suorituskyky tai puhtaus.
Akryylinitriili syntetisoidaan jälleen propeenista, mutta tekemällä siitä reagoimaan typpioksidin kanssa PBO -katalyytteissä2-Zro2 ilma -alue. Reaktio on seuraava:
4 CH3−CH = ch2 + 6 EI → 4 CHO2= CH-CÖN + 6 H2Tai + n2
Reaktio, johon ei liity propeenia, on se, joka alkaa eteenioksidilla, joka reagoi vetysyanidin kanssa muuttumaan etyleenisyanohydriiniksi; Ja myöhemmin se kuivuu Acrilonitriilin lämpötilassa 200 ºC:
ETO + HCN → CH2Ojamainen2CN
CH2Ojamainen2CN + Q (200 ºC) → CH2= CH-CÖN +H2JOMPIKUMPI
Toinen paljon suorempi reaktio on syanidin vety -asetyleenin lisääminen:
Hc irtich + hcn → ch2= CH-CÖN
Muodostuu kuitenkin monia toissijaisia tuotteita, joten acrilonitriilin laatu on alhaisempi verrattuna Sohio -prosessin laatuun.
Edellä mainittujen aineiden, laktonitriilin, propionitriilin lisäksi.
Sovellukset
 Legot valmistetaan pääasiassa ABS -muovilla, kopolymeerillä, jossa acrilonitriili on osa. Lähde: Pxhere.
Legot valmistetaan pääasiassa ABS -muovilla, kopolymeerillä, jossa acrilonitriili on osa. Lähde: Pxhere. Acrilonitriili on välttämätön aine muoviteollisuudelle. Useat hänen johdetut muovit tunnetaan hyvin. Näin on Acrilonitrilo-butadieeni-styreenikopolymeerien (ABS) tapauksessa, joiden kanssa maallikkojen palat valmistetaan. Meillä on myös akryylikuituja, jotka on kehitetty polyakryylinitriilihomopolymeerillä (PAN).
Voi palvella sinua: saponifikaatioMuiden muovien joukossa, jotka sisältävät acilonitriiliä monomeerinä tai jotka riippuvat siitä sen valmistukseen, meillä on: akryyliventäminen (SAN), butadieeniakryylinitriili (NBR), acilonitriili -venytysakrylaatti (ASA), polyakryyliamidi ja synteettiset kaarevat ja nitriilihartsit.
Käytännössä mitä tahansa luonnollista polymeeriä, kuten puuvillaa, voidaan modifioida sisällyttämällä sen molekyylirakenteet Acrilonitriiliin. Siten saadaan nitriilijohdannaiset, mikä tekee erittäin laajan akryylitriilin kemiasta.
Yksi sen käytöstä muovien maailman ulkopuolella on kuin torjunta -aine sekoitettuna hiilitetrakloridin kanssa. Kuitenkin sen kauhistuttavan vaikutuksensa vuoksi meren ekosysteemiin, tällaiset torjunta -aineet ovat kuitenkin kiellettyjä tai ovat voimakkaita rajoituksia.
Riskejä
Acrilonitriili on vaarallinen aine, joten sitä on manipuloitava äärimmäisellä hoidolla. Mahdolliset sopimattomat tai liian pitkäaikaiset altistukset tälle yhdisteelle voi olla tappavaa joko hengittämällä, saannilla tai fysikaalisella kosketuksella.
Sitä tulisi ylläpitää niin pitkälle kuin mahdollista mistä tahansa lämmönlähteestä, koska se on haihtuva ja erittäin syttyvä neste. Hän ei myöskään saa olla yhteydessä veteen, koska hän reagoi väkivaltaisesti hänen kanssaan.
Tämän lisäksi se on mahdollisesti karsinogeeninen aine, joka on liitetty maksa- ja keuhkosyöpiin. Niiden, jotka ovat alttiina tälle aineelle.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5. painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. (10. painos.-A. Wiley Plus.
- Wikipedia. (2020). Akryylinitriili. Haettu: vuonna.Wikipedia.org
- Kansallinen bioteknologiatietojen keskus. (2020). Akryylinitriili. Pubchem -tietokanta., CID = 7855. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- Elsevier B.V. (2020). Akryylinitriili. Tiede. Haettu: ScienEdirect.com
- Korry Barnes. (2020). Mikä on akryylinitriili? - Käyttö ja ominaisuudet. Opiskelu. Toipunut: Opiskelu.com
- Pajonk, G.M., Manzalji, t. (1993). Akryylinitriilin synteesi propeenin ja typpioksidiseoksista PBO: lla2-Zro2 Ilma -katalyytit. Katalit kaksikymmentäyksi, 361-369. doi.org/10.1007/BF00769488
- « Dynaamiset ohjelmointiominaisuudet, esimerkki, edut, haitat
- Mikä on isoterminen prosessi? (Esimerkkejä, harjoituksia) »

