Karboksihemoglobiinin ominaisuudet ja vaikutukset
- 2625
- 718
- Louis Moen
Se karboksihemoglobiini Se on hemoglobiini, joka on kiinnitetty hiilimonoksidiin (CO). Hemoglobiini on proteiini, joka kuljettaa happea veren läpi ihmisiin ja monissa muissa selkärankaisissa.
Hapen kuljettamiseksi hemoglobiinin on liityttävä tähän. Max Perutz, Wienissä vuonna 1914 syntynyt kemisti- ja Nobel-palkinto ja tapettiin Cam-siltassa vuonna 2002, nimeltään "hemoglobiinihappea.
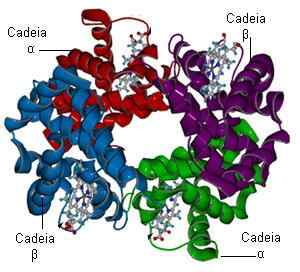
 Hemoglobiinirakenne (lähde: Bielabio Wikimedia Commonsin kautta)
Hemoglobiinirakenne (lähde: Bielabio Wikimedia Commonsin kautta) Kuvittele kaksi hemoglobiinimolekyyliä, jotka kykenevät yhdistämään jokaisen neljään happimolekyyliin. Yhdellä on jo kolme happimolekyyliä ja toisessa ei. Jos toinen happimolekyyli näyttää, kysymys on seuraava: sitoutuuko se "rikkaaseen", jolla on jo kolme, tai "köyhä", jolla ei ole? Todennäköisyys on 100 - 1, että rikas molekyyli on suunnattu.
Kuvittele nyt kaksi muuta hemoglobiinimolekyyliä. Toisessa on 4 happimolekyyliä (se on kylläinen) ja toisella on vain yksi. Mikä molekyyleistä antaa todennäköisimmin happea kudoksille, rikkaille tai köyhille? Köyhimmät tuottavat happea helpommin kuin rikkaat.
Hapen jakautuminen hemoglobiinimolekyylissä voidaan pitää raamatullisena vertauksena: "... kuka on, se annetaan ja jolla ei ole, edes mitä hänellä on poistettu ..." (MT, 13:12 -A. Fysiologisesta näkökulmasta tämä "moraaliton" hemoglobiinimolekyylin käyttäytyminen on täynnä merkitystä, sijainti myötävaikuttaa hapen vaikutukseen kudoksiin.
Hiilimonoksid. Toisin sanoen runsaasti CO: n läsnä ollessa kaikki hemoglobiiniin kiinnitetyt hapet korvataan CO: lla.
[TOC]
Rakenteelliset ominaisuudet
Puhuminen karboksihemoglobiinista, joka ei ole muuta kuin hiilimonoksidiin liittyvää hemoglobiinia, on tarpeen viitata ensin hemoglobiiniin yleisesti.
Hemoglobiini on proteiini, joka koostuu neljästä alayksiköstä, jotka on muodostettu kukin polypeptidiketjulla, joka tunnetaan nimellä globiini ja ei -proteiiniryhmä (proteesiryhmä), nimeltään Hemo.
Voi palvella sinua: Bioestadistiikka: Historia, opintokenttä ja sovelluksetJokainen Hemo -ryhmä sisältää rautatomin rautatilassa (usko2+-A. Nämä ovat atomit, jotka kykenevät liittämään happea hapettumatta.
Hemoglobiini -tetrameeri muodostuu kahdella alfa -globiinin alayksiköllä, 141 aminohappoa ja kahdella beeta -globiinin alayksiköllä, 146 aminohappoa kukin.
Hemoglobiinimuodot tai rakenteet
Kun hemoglobiinia ei ole kytketty mihinkään happiatomiin, hemoglobiinin rakenne on jäykkä tai jännittynyt, suolaliuossillan muodostumisen tuote sisällä.
Hemoglobiinin kvaternäärinen rakenne ilman happea (deoksigenada) tunnetaan nimellä "T" tai jännittynyt rakenne, ja hapetettua hemoglobiinia (oksihemoglobiini) tunnetaan nimellä "R" tai rento rakenne.
Siirtyminen rakenteesta T rakenteeseen R tapahtuu hapen liiton avulla rauta -atomiin (usko2+) jokaiseen globin -ketjuun kiinnitetystä hemo -ryhmästä.
Osuuskuntakäyttäytyminen
Hemoglobiinin rakenteen muodostavat alayksiköt osoittavat yhteistyökäyttäytymistä, joka voidaan selittää seuraavalla esimerkillä.
Voit kuvitella deoksigoituneen hemoglobiinimolekyylin (rakenteessa t) villakuorena, jossa on hyvin piilotettu happea sitoutumiskohtia (HEM -ryhmiä).
Kun tämä jännittynyt rakenne liittyy happimolekyyliin, unionin nopeus on erittäin hidas, mutta tämä liitto on riittävä löysäämään palloa hiukan ja saattavan seuraavan HEMO -ryhmän pintaan, mikä tekee nopeuden, jolla se sitoo seuraavaa happea, on suurempi, suurempi, suurempi, prosessin toistaminen ja affiniteetin lisääminen jokaisen liiton kanssa.
Hiilimonoksidivaikutukset
Hiilimonoksidin vaikutusten tutkimiseksi kaasujen verenkuljetukseen on ensin välttämätöntä.
Voi palvella sinua: briologia: mikä on, historia, mitä tutkimuksiaOxihemoglobiinikäyrällä on sigmoidi tai "S" -muoto, joka vaihtelee osittaisen happipaineesta riippuen. Käyräkaavio on selkeä sen rakentamiseen käytetyille verinäytteille tehdyistä analyyseistä.
Käyrän kallistuvin alue saadaan alle 60 mmHg: n paineilla ja suuremmilla paineilla, käyrä pyrkii tasoittumaan, ikään kuin se saavuttaa tasangon.
Kun tiettyjen aineiden läsnäollessa käyrä voi osoittaa merkittäviä poikkeamia. Nämä poikkeamat osoittavat muutoksia, joita tapahtuu hemoglobiinin affiniteetissa happea johtuen samaan PO: hen2.
Tämän ilmiön kvantifioimiseksi otettiin käyttöön hemoglobiinin affiniteetin mitta, joka tunnetaan nimellä P -arvoviisikymmentä, joka on osittainen happipaine -arvo, jolle hemoglobiini on 50% tyydyttynyt; toisin sanoen, kun puolet heidän hemo -ryhmästään yhdistyy happimolekyyliin.
Vakioolosuhteissa, jotka on ymmärrettävä pH 7: ksi.4, osittainen 40 mmHg happipaine ja 37 ° C lämpötila, P, Pviisikymmentä Aikuisen miehen alla on 27 mm Hg tai 3,6 kPa.
Mitkä tekijät voivat vaikuttaa hapen hemoglobiinin affiniteettiin?
Erytrosyytteihin sisältyvän hemoglobiinin hapen affiniteetti voi vähentyä hiilidioksidin (CO 2-3DPG) läsnä ollessa (2-3DPG) (CO2), korkeat protonien pitoisuudet tai lisääntynyt lämpötila; Ja sama koskee hiilimonoksidia (CO).
Toiminnalliset vaikutukset
Hiilimonoksidi kykenee häiritsemään valtimoveren hapen kuljetustoimintaa. Tämä molekyyli pystyy liittymään hemoglobiiniin ja muodostamaan karboksihemoglobiinia. Tämä johtuu siitä, että sillä on affiniteetti hemoglobiiniin noin 250 kertaa suurempi kuin O2, Joten hän pystyy siirtämään sitä jopa silloin, kun hän on linkitetty häneen.
Voi palvella sinua: Czapek Agar: Perusta, valmistelu, käyttö ja rajoituksetKeho tuottaa pysyvästi hiilimonoksidia, vaikkakin pieninä määrinä. Tämä kaasu, väritön ja wc, liittyy Hemo -ryhmään samalla tavalla kuin se tai2, Ja yleensä veren hemoglobiinista on noin 1%, kuten karboksihemoglobiini.
Koska orgaanisen aineen epätäydellinen palaminen tuottaa CO: ta, karboksihemoglobiinin osuus tupakoitsijoissa on paljon suurempi, kykenevä saavuttamaan arvot välillä 5-15% hemoglobiinista 5–15%. Karboksihemoglobiinipitoisuuden krooninen kasvu on haitallista terveydelle.
Yli 40% karboksihemoglobiinin tuottavan CO: n määrän kasvu uhkaa elämää. Kun rautaraudan sitoutumispaikka on CO: n miehittämä, et voi lyödä O: ta2.
CO -liitto tuottaa siirtymisen hemoglobiinista rakenteeseen R, niin että hemoglobiini vähentää edelleen kykyä toimittaa tai2 Veriskapillaareissa.
Carboksyhemoglobiinilla on vaaleanpunainen väri. Joten CO: lla myrkytetyt potilaat omaksuvat vaaleanpunaisen värin, jopa koomassa ja hengityselimissä. Paras hoito näiden potilaiden hengen pelastamiseksi on tehdä puhdasta, jopa hyperbaarista happea hengitystä, yrittää syrjäyttää raudan liiton CO: n kanssa.
Viitteet
- Kettu, s. Yllyttää. (2006). Ihmisen fysiologia 9. painos (PP. 501-502). McGraw-Hill Press, New York, USA.
- Murray, r. K -k -., Granner, D. K -k -., Mayes, P. -Lla., & Rodwell, V. W -. (2014). Harperin kuvitettu biokemia. McGraw-Hill.
- Rawn, j. D -d. (1998). Biokemia (1989). Burlington, Pohjois -Carolina: Neil Patterson Publishers (C) N. Lalioti, cp raptopoulou, a. Terzis, a. Panagiotopoulos, sp perlepes ja. Manessi-zoupa, J. Kemia. Soc. Dalton Trans, 1327.
- Robert M. Berne, Matthew N. Perimä. (2001) Fysiologia. (3. painos.) Harcourt Editions, S.-Lla.
- West, J. B -. (1991). Lääketieteellisen käytännön fysiologinen perusta. Williams & Wilkins
- « Laadulliset arviointiominaisuudet, edut, esimerkit
- Havainnollista oppimisteoriaa, ominaisuuksia, esimerkkejä »

