Kysteiinin ominaisuudet, rakenne, toiminnot, biosynteesi
- 3362
- 470
- Juan Breitenberg V
Se Kysteiini (Cys, c) on yksi 22 aminohapposta, joita löytyy luonnosta osana polypeptidiketjuja, jotka muodostavat elävien olentojen proteiinit. Se on välttämätöntä proteiinien tertiääristen rakenteiden stabiilisuudelle, koska se auttaa molekyylin disulfidisiltojen muodostumista.
Sen lisäksi, että se pätee muihin aminohapoihin, kuten alaniiniin, arginiiniin, asparagiiniin, glutamaattiin ja glutamiiniin, glysiiniin, proliiniin, seriiniin ja tyrosiiniin, ihmiset kykenevät syntetisoimaan kysteiiniä, joten tätä ei pidetä välttämättömänä aminohappona.
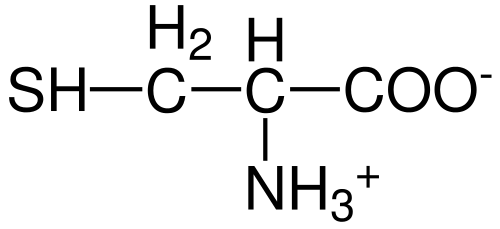
 Kysteiinin aminohapon rakenne (lähde: Hattrich [julkinen domeeni] Wikimedia Commonsin kautta)
Kysteiinin aminohapon rakenne (lähde: Hattrich [julkinen domeeni] Wikimedia Commonsin kautta) Huolimatta tästä ja sen vuoksi, että synteesinopeudet eivät aina toimita kehon vaatimuksia, jotkut kirjoittajat kuvaavat kysteiiniä "ehdollisesti" olennaisesti "aminohappona.
Tämän aminohapon nimettiin "kystinnä", joka oli vuonna 1810 löydettyjen vesikulaaristen laskelmien komponentti, jonka nimi keksittiin vuonna 1832 A. Baudrimont ja f. Malaguti. Muutamaa vuotta myöhemmin, vuonna 1884, ja. Baumann havaitsi, että kysteiini oli kystiinin vähentämisen tuote.
Baumanin tekemän työn jälkeen vuonna 1899 määritettiin, että kysteiini on proteiinin pääosa, joka muodostaa eri eläinten sarvet, mikä ehdotti sen mahdollista käyttöä polypeptidisynteesiin.
Tällä hetkellä tiedetään, että kehon kysteiini on peräisin ruoasta, proteiinien kierrätyksestä ja endogeenisestä synteesistä, joka esiintyy pääasiassa hepatosyyteissä.
[TOC]
Ominaisuudet
Kysteiinin molekyylipaino on 121.16 g/mol ja sitä löytyy yhdessä leusiinin, isoleusiinin, valiinin, fenyylialaniinin, tryptofaanin, metioniinin ja tyrosiinin kanssa hydrofobisimmista aminohapoista.
Se kuuluu polaaristen aminohappojen ryhmään ilman kuormitusta ja kuten muutkin aminohapot, se voidaan hajottaa alkalisella hydrolyysillä korkeissa lämpötiloissa.
Kuten tryptofaani, seriini, glysiini ja treoniini, kysteiini on metabolinen edeltäjä glukoneogeneesille ja ketogeneesille (ketonirunkojen muodostuminen).
Tämä aminohappo esiintyy osana proteiinien peptidisekvenssiä, mutta voi myös olla vapaa veriplasmassa homogeenisina disulfideina (kystiini, johdannainen) tai sekoitettuna, koostuen homokysteiinisysteiinimuodosta.
Suurin ero vapaan kysteiinin ja proteiinirakenteen löydetyn välillä on, että ensimmäinen on erittäin ruosteisessa redox -tilassa, kun taas viimeinen on yleensä melko pelkistetty.
Rakenne
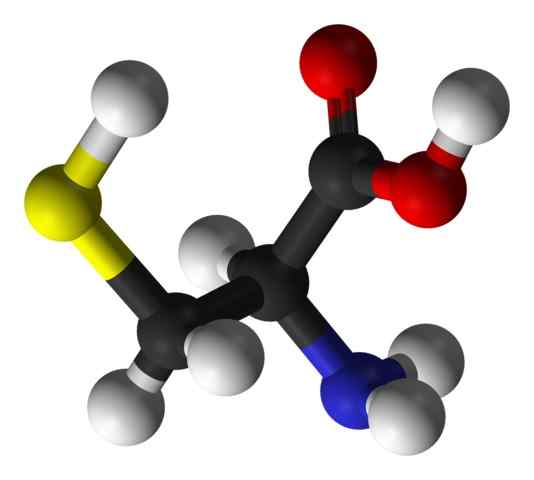
Kuten muihin tähän mennessä kuvattujen aminohappojen kohdalla, kysteiinillä on keskeinen hiiliatomi, joka on kiraalinen ja tunnetaan nimellä hiili a.
Tähän hiiliatomiin liittyy neljä erilaista kemiallista lajia:
- Amino-ryhmä (-NH3+)
- Karboksyyliryhmä (-CO-)
- vetyatomi ja
- Substituentti (-r).
Substituenttiryhmä on se, joka antaa identiteetin jokaiselle aminohapolle ja kysteiinille on ominaista, että se sisältää rikkiatomin osana ryhmää Tioli jompikumpi Sulfhydrillo (-CH2-s).

Juuri tämä ryhmä antaa sen osallistua intermolekulaaristen disulfidisiltojen muodostumiseen. Koska se on nukleofiili, voit myös osallistua substituutioreaktioihin.
Itse asiassa tätä kysteiinin sivuketjua voidaan modifioida kahden yhdisteen muodostumiseksi, jotka tunnetaan nimellä "selenosysteiini" ja "lantioniini". Ensimmäinen on aminohappo, joka myös osallistuu proteiinien muodostumiseen ja toinen on ei -proteiiniaminohappojohdannainen.
Voi palvella sinua: Histonit: Ominaisuudet, rakenne, tyypit ja toiminnotKysteiiniryhmälle on ominaista myös sen suuri affiniteetti hopea- ja elohopea -ioneihin (AG+ ja HG2+).
Funktiot
Kysteiinin päätoiminnot elävissä organismeissa liittyy osallistumiseen proteiinien muodostumiseen. Erityisesti kysteiini osallistuu disulfidisiltojen muodostumiseen, jotka ovat välttämättömiä tertiäärisen proteiinirakenteen muodostumiselle.
Lisäksi tämä aminohappo ei ole vain hyödyllinen proteiinisynteesille, vaan myös osallistuu glutationin (GSH) synteesiin ja tarjoaa vähentyneen rikkiä metioniinille, lipoiinihapolle, tiamiinille, koentsyymille (COA), molybdopteriinille (kofaktori) ja muulle) yhdisteet, joilla on biologinen merkitys.
Epäorgaanisen pyruvaatin ja rikin tuotantoon voidaan käyttää liiallisen määrän rikkipohjaisia aminohappoja, kysteiiniä ja muita siihen liittyviä aminohappoja. Pyruvate onnistuu ohjaamaan kohti glukoneogeenistä reittiä, joka palvelee glukoosin tuotantoa.
Keratiinit, jotka ovat yksi eläinvaltion runsaimmista rakenneproteiineista, ovat runsaasti kysteiinitähteissä. Esimerkiksi lammasvilla sisältää yli 4% rikkiä tästä aminohaposta.
Kysteiini osallistuu myös moniin oksidin vähentämisreaktioihin, joten se on osa joidenkin entsyymien aktiivista kohtaa.
Reagoidessasi glukoosin kanssa, tämä aminohappo tuottaa reaktiotuotteita, jotka tuovat houkuttelevia makuja ja aromeja joihinkin kulinaarisiin valmisteisiin.
Biosynteesi
Aminohappojen biosynteesi ihmiskehossa ja muiden eläinten (nisäkkäiden ja ei-nisäkkäiden) olosuhteissa tapahtuu kudosmuodossa ja soluluokassa; Se on prosessi, joka ansaitsee energiaa ja on yleensä erotettu eri elinten välillä.
Maksa on yksi tärkeimmistä elimistä, jotka osallistuvat useimpien ei -välttämättömien aminohappojen synteesiin, riippumatta tarkasteltavasta lajista.
Tässä ei vain kysteiini syntetisoidaan, vaan myös aspartaatti, asparagiini, glutamaatti ja glutamiini, glysiini, seriini, tyrosiini ja muut sen spesifisistä aminohappojen esiasteista.
Vuonna 1935 Erwin -tuotemerkki päätti, että kysteiini nisäkkäissä syntetisoidaan luonnollisesti metioniinista, joka tapahtuu yksinomaan maksakudoksessa.
Tämä prosessi voi tapahtua metioniinin "lähetys", jossa metyyliryhmät siirretään kukkulalle ja kreatiinille. Kysteiini voidaan kuitenkin muodostaa myös metioniinista transulfuraation ansiosta.
Myöhemmin osoitettiin, että metioniinin lisäksi jotkut synteettiset yhdisteet, kuten N-asetyylikysteiini, kysystamiini ja kystamiini, ovat hyödyllisiä esiasteita kysteiinisynteesille.
N-asetyylikysteiinin tapauksessa solut vievät tämän, missä se muuttuu kysteiiniksi sytosolin entsyymillä sytosolissa.
Synteesimekanismi
Kysteiinin synteesin mekanismi tunnetuimmasta menetelmästä on trans -ululo. Tämä tapahtuu pääasiassa maksassa, mutta se on määritetty myös suolistossa ja haimassa.
Tämä tapahtuu homokysteiinistä, aminohappomenetelmästä johdetusta yhdisteestä; Ja tämän biosynteettisen reitin ensimmäinen reaktio on kondensaatio, jota katalysoi β-sentaasi (CBS) cistationine-entsyymi (CBS).
Voi palvella sinua: Urasiili: rakenne, toiminnot, ominaisuudet, synteesiTämä entsyymi edustaa reitin "sitoutumisen" läpäisyä ja tiivistää homokysteiinin seriinitähteellä, toisella proteiiniaminohapolla, joka tuottaa kystatiinia. Myöhemmin tämä yhdiste "leikataan" tai "jaetaan" Cistationasa -entsyymillä, mikä johtaa kysteiinin vapautumiseen.
CBS -entsymaattisen aktiivisuuden säätelyä välitetään menetelmän saatavuus ja solun redox -tila, jossa tämä prosessi tapahtuu.
Kysteiinisynteesireitin kautta solut voivat käsitellä ylimääräistä menetelmää, koska niiden muuntaminen kysteiiniksi on peruuttamaton prosessi.
Kysteiinisynteesi kasveissa ja mikro -organismeissa
Näissä organismeissa kysteiini syntetisoidaan pääasiassa epäorgaanisesta rikkiä, joka on runsain käyttökelpoisen rikin lähde aerobisessa biosfäärissä.
Tämä otetaan, tulee soluihin ja pelkistetään sitten sulfidiksi (S2-), joka sisällytetään kysteiiniin samalla tavalla kuin mitä ammoniumin kanssa tapahtuu glutamaatin tai glutamiinin synteesissä.
Aineenvaihdunta ja hajoaminen
Katabolismin kysteiini esiintyy pääasiassa maksasoluissa (hepatosyytit), vaikka sitä voi esiintyä myös muun tyyppisissä soluissa, kuten neuroneissa, endoteelisoluissa ja kehon verisuonten sileissä lihassoluissa.
Tietyt kysteiinin katabolismin puutteet tuottavat perinnöllisen taudin, joka tunnetaan nimellä "kystinuria", jolle on ominaista kystiinilaskelmien läsnäolo munuaisissa, virtsarakossa ja virtsajohtimessa.
Kystiini on kysteiinistä johdettu aminohappo ja laskelmat muodostetaan kahden molekyylin liittämällä niiden rikkitomien kautta.
Osa kysteiinin aineenvaihdunnasta johtaa tieteellisen hapon muodostumiseen, josta härkätaistelu, ei-protetinen aminohappo muodostetaan. Reaktiota katalysoi dioksigenasa -kysteiinientsyymi.
Lisäksi formaldehydi voi hapettaa kysteiinin N-Formil-kysteiinin tuottamiseksi, jonka myöhempi prosessointi voi johtaa "tavaroiden" muodostumiseen (kysteiinien kondensaation tuote aromaattisilla yhdisteillä).
Eläimissä käytetään myös kysteiiniä, samoin kuin glutamaattia ja glutamiinia, koentsyymin A, glutationin (GSH), pyruvaatin, sulfaatin ja sulfaatimapapon synteesiä varten.
Yksi kysteiinin muuntamista koskevista menetelmistä pyruvaatiksi tapahtuu kahdessa vaiheessa: ensimmäinen merkitsee rikkiatomin ja toisen A transaminaatioreaktion poistamista.
Munuaiset ovat vastuussa rikkiyhdisteiden, kuten kysteiinin metaboliasta johdettujen sulfaattien ja sulfiitien erittymisestä, kun keuhkot uloshengitysrikkidioksidi ja sulfidihappo.
Glutationi
Glutationi, molekyyli, joka on muodostanut kolmen aminohappojätteen (glysiini, glutamaatti ja kysteiini), on molekyyli, jota on läsnä kasveissa, eläimissä ja bakteereissa.
Sillä on erityisiä ominaisuuksia, jotka tekevät siitä erinomaisen redox -puskurin, koska se suojaa soluja erityyppisiltä oksidatiivisilta stressiltä.
Ruoat, joissa on runsaasti kysteiiniä
Kysteiiniä esiintyy luonnollisesti elintarvikkeissa, jotka sisältävät rikkiä munien (keltaisten), punaisten paprikoiden, valkosipulin, sipulien, parsakaalin, kukkakaalin, colliflow: n, kollilien ja Brysselin choles-, vesikappaleiden ja sinappilehden, vesiklakkien ja sinappilehden keltuaisina (keltaisilla), vesipuistojen, valkosipulin, sipulien, parsakaalin, vesikaatin, vesikulan, vesikulaisten, vesikulan, sinappilehden, munuaisten, vesikulan, sinappilehden kanssa.
Sitä esiintyy myös enimmäkseen proteiinirikkaissa elintarvikkeissa, kuten lihassa, palkokasvissa ja maitotuotteissa, joista ovat:
Voi palvella sinua: ovalbumiinia: rakenne, toiminnot, denaturointi- Lehmänliha, sianliha, kana ja kalat
- Kaura ja linssit
- Auringonkukansiemenet
- Jogurtti ja juusto
Kysteiinin saannin edut
Katsottaan, että sen saanti estää hiustenlähtöä ja stimuloi sen kasvua. Elintarviketeollisuudessa sitä käytetään hyvin panttiliivettäväksi hieronta -aineena ja myös lihan kaltaisten makujen "toistamiseen".
Muut kirjoittajat ovat korostaneet.
Ihmiset käyttävät joitain kysteiiniin liittyviä ravitsemuslisäaineita antioksidantteina, joita pidetään hyödyllisenä ikääntymisen "viiveen" näkökulmasta.
Esimerkiksi N-asetyylisysteiini (esiaste kysteiinin synteesissä) pidetään ravitsemuslisäaineena, koska tämä johtaa glutationin biosynteesin (GSH) lisääntymiseen (GSH).
Liittyvät sairaudet
Jotkut tieteelliset julkaisut liittyvät korkeaan plasmakysteiinitasoon liikalihavuuteen ja muihin siihen liittyviin patologioihin, kuten sydän- ja verisuonisairauksiin ja muihin metabolisiin oireyhtymiin.
Kystinuria, kuten edellä mainittiin, on patologia, joka liittyy kystiinikivien läsnäoloon, vetoketjun johdannaiseen, johtuen geneettisestä virheestä dibasisten aminohappojen, kuten kystiinin, imeytymisessä, kuten kystiini.
Puutoshäiriöt
Kysteiinin puute on liittynyt oksidatiiviseen stressiin, koska tämä on yksi glutationisynteesin tärkeimmistä edeltäjistä. Siksi tämän aminohapon puutteet voivat johtaa ennenaikaiseen ikääntymiseen ja kaikkiin asuntoihin, joita tämä tarkoittaa.
Kokeellisesti on osoitettu, että kysteiinilisäys parantaa luuston lihaksen toimintoja, vähentää rasvan ja ei -rasvaisen kehon massan välistä suhdetta, vähentää tulehduksellisten sytokiinien plasmatasoja, parantaa immuunijärjestelmän toimintoja jne.
1990 -luvun puolivälissä jotkut tutkimukset viittasivat siihen, että hankittu immuunikato (AIDS) -oireyhtymä voisi olla seurausta viruksen aiheuttamasta kysteiinin puutteesta.
Näitä väitteitä tuki se tosiasia.
Viitteet
- Dröge, W. (1993). Kysteiini- ja glutationin vajaatoiminta AIDS-potilailla: Peruste hoitoon N-acyylisysteiinillä. Farmakologia, 46, 61-65.
- Dröge, W. (2005). Oksidatiivinen stressi ja ikääntyminen: ikääntyy kysteiinin vajaatoiminnan oireyhtymä? Kuninkaallisen yhdistyksen filosofiset liiketoimet B: Biologiset tieteet, 360(1464), 2355-2372.
- Elshorbagy, a. K -k -., Smith, a. D -d., Kozich, V., & Refsum, H. (2011). Kysteiini ja liikalihavuus. Liikalihavuus, kaksikymmentä(3), 1-9.
- Kridich, n. (2013). Kysteiinin biosynteesi. Ecosal Plus, 1-30.
- McPherson, R. -Lla., & Hardy, G. (2011). Kysteiinirikastettujen proteiinilisäaineiden kliiniset ja ravitsemukselliset hyödyt. Nykyinen mielipide kliinisessä ravinnossa ja aineenvaihdunnassa, 14, 562-568.
- Mokhtari, V., Afsharian, p., Shahhoseini, m., Kalantar, S. M., & Moini, a. (2017). Katsaus N-asetyylikysteiinin erilaisista käytöistä. Solupäiväkirja, 19(1), 11-17.
- Pisto, p. (2013). Kysteiinimestari antioksidantti. Farmaseuttisen, kemian ja biologisen tieteen kansainvälinen lehti, 3(1), 143-149.
- Quig, d. (1998). Kysteiinimetabolia ja metallimyrkyllisyys. Vaihtoehtoisen lääketieteen katsaus, 3(4), 262-270.
- Wu, g. (2013). Aminohapot. Biokemia ja ravitsemus. Boca Raton, FL: Taylor & Francis -ryhmä.
- « Sosiaalisen oppimisen ominaisuudet, bandura -teoria, esimerkkejä
- Sosio -emotionaalinen koulutuksen ulottuvuudet, merkitys, esikoulu »

