Ominaisuudet, koulutus, esimerkit
- 4200
- 294
- Kelly Kilback
Se Kolmiosaiset yhdisteet Ne ovat kaikki niitä, jotka koostuvat kolmesta eri atomista tai ionista. Ne voivat olla hyvin monimuotoisia hapoista tai perusaineista metalliseoksiin, mineraaleihin tai moderneihin materiaaleihin. Kolme atomia voivat kuulua samaan jaksollisen taulukon ryhmään tai jatkaa mielivaltaisia paikkoja.
Jotta kolmiosainen yhdiste tapahtuu, sen atomien välillä on oltava kemiallinen affiniteetti. Kaikki eivät ole yhteensopivia keskenään, ja siksi et voi yksinkertaisesti valita satunnaisesti, mikä kolme integroi ja määrittelee yhdisteen tai seoksen (olettaen, että kovalenttisten sidosten puute).
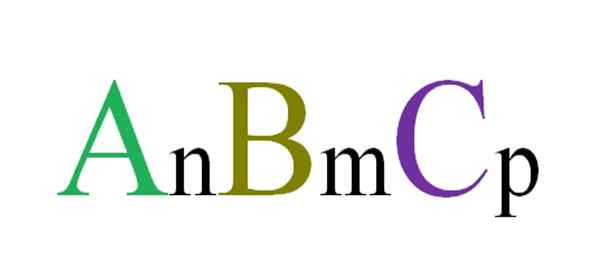 Yleinen ja satunnainen kaava ternaarisille yhdisteille. Lähde: Gabriel Bolívar.
Yleinen ja satunnainen kaava ternaarisille yhdisteille. Lähde: Gabriel Bolívar. Esimerkiksi satunnaisesti valitaan kolme kirjainta, jotka hallitsevat ABC: n kolionaalista yhdistettä (ylivoimainen kuva). Tilaukset n, m ja p osoittavat atomien tai ionien a, b ja c väliset stökiometriset suhteet. Saadaan tällaisten alaindeksien arvojen ja kirjainten identiteettien arvojen ja kirjaimien identiteettien identiteettien.
Kuitenkin kaava AnB -mCp Se on voimassa vain, jos se täyttää elektroneutraalisuuden; Eli maksuesi summan on oltava yhtä suuri kuin nolla. Tätä silmällä pitäen on fysikaalisia (ja kemiallisia) rajoituksia, jotka ohjaavat, onko mainitun kolmen yhdisteen muodostuminen mahdollista.
[TOC]
Kolmiosaisten yhdisteiden ominaisuudet
Sen ominaisuudet eivät ole yleisiä, mutta vaihtelevat niiden kemiallisen luonteen mukaan. Esimerkiksi oksoasidit ja emäkset ovat ternaarisia yhdisteitä, ja jokaisella niistä on tai ei ole sarja edustavia ominaisuuksia.
Nyt, ennen hypoteettista yhdistettä ABC, tämä voi olla ioninen, jos elektronegatiivisuuden erot A, B ja C välillä eivät ole suuria; tai kovalenttinen, linkillä A-B-C. Jälkimmäiset annetaan äärettömiin esimerkeihin orgaanisessa kemiassa, kuten alkoholissa, fenoleissa, eetterissä, hiilihydraateissa jne., jonka kaavat voidaan kuvata C: llänHm JOMPIKUMPIp.
Voi palvella sinua: metallien mekaaniset ominaisuudetSiten ominaisuudet ovat hyvin vaihtelevia ja värähtelevät yhden kolmen kolmen yhdisteen korkealla asteella toiseen. Yhdiste CnHmJOMPIKUMPIp Sanotaan, että se on happea; kun taas cnHmNp, Toisaalta se on typpi (se on amiinia). Muut yhdisteet voivat olla rikkiä, fosforoitua, fluorisoitua tai niillä on merkitty metallinen luonne.
Emäkset ja hapot
Etenemällä epäorgaanisen kemian alalla, sinulla on metallipohjat, MnJOMPIKUMPImHp. Antaa.
Esimerkiksi NaOH -pohja, ottaen huomioon tällaiset alaosat, olisi kirjoitettava nimellä Na1JOMPIKUMPI1H1 (mikä olisi kaoottista). Lisäksi oletetaan, että H on kationin h+, Eikä miten se todella näyttää: kuuluminen anioniin OH-. OH: n toiminnan vuoksi- Iholla nämä emäkset ovat saippuat ja kaustiset.
Metallipohjat ovat ionisia aineita, ja vaikka ne koostuvat kahdesta ionista, mn+ ja oh- (NA+ ja oh- NaOH: lle) ne ovat kolmiosaisia yhdisteitä, joilla on kolme erilaista atomia.
Toisaalta hapot ovat kovalenttisia, ja niiden yleinen kaava on Hao, missä ei -metallinen atomi on yleensä. Kuitenkin, koska se on helppo ionisoitu vedessä vapauttavissa hydrogeissa, sen H -ioneissa+ Coroen ja satuttaa ihoa.
Nimikkeistö
Kuten ominaisuudet, kolmen yhdisteiden nimikkeistö on hyvin monipuolinen. Tästä syystä vain vain emäksiä, oksoasideja ja oksisaleja pidetään pinnallisesti.
Pohjat
Metallipohjat mainitaan ensin sanalla 'hydroksidi', jota seuraa metallin nimi ja sen valenssi roomalaisissa luvuissa suluissa. Siten NaOH on natriumhydroksidi (I); Mutta koska natriumin ainutlaatuinen valenssi on +1, se pysyy yksinkertaisesti natriumhydroksidina.
Se voi palvella sinua: alkeetAl (OH)3, Esimerkiksi se on alumiinihydroksidi (III); ja cu (OH)2, Kuparihydroksidi (II). Tietysti kaikki systemaattisen nimikkeistön mukaan.
Oksoasidit
Oxóakideilla on melko yleinen kaava Hao -tyypistä; Mutta todellisuudessa niitä kuvataan paremmin AOH: ksi. Ha-H: n linkki ilmenee H-julkaistu+.
Perinteinen nimikkeistö on seuraava: Sana 'happo' alkaa, jota seuraa keskusatomin nimi, jota edeltää tai edeltää heidän vastaavat etuliitteet (hypo, Per) tai jälkiliitteet (Bear, ICO) sen mukaan, onko hän työskentelee alaikäistensä kanssa tai vanhemmat valenssit.
Esimerkiksi bromioksoasidit ovat hbro, hbro2, Hehku3 ja hbro4. Nämä ovat happoja: vastaavasti hypobromit, bromiset, bromit ja perbromit. Huomaa, että kaikissa niissä on kolme atomia, joilla on erilaiset arvot niiden alaindeksille.
Oksiaalit
Ne kutsutaan myös Nullion -suoloiksi, ne ovat edustavimpia kolmesta kolmesta yhdisteestä. Ainoa ero mainita niitä on, että Bear ja Ico Sufijos muuttuu vastaavasti Itolle ja Atolle. Lisäksi H korvataan metallikationilla, happo-emäs neutraloinnin tuotetta.
Jatkamalla bromia, sen natriumoksisalit olisivat: Nabro, Nabro2, Nabro3 ja Nabro4. Heidän nimistään tulee: Hipobromito, Bromito, Bromato ja Natrium perbromaatti. Epäilemättä mahdollisten oksisalien lukumäärä ylittää oksoasidien lukumäärän.
Koulutus
Jälleen jokaisella kolmannen yhdistyksen tyyppi on oma alkuperänsä tai koulutusprosessi. On kuitenkin kohtuullista mainita, että nämä voidaan muodostaa vain, jos kolmen atomin jäsenen välillä on riittävä affiniteetti. Esimerkiksi metallipohjat ovat olemassa kationien ja OH: n välisten sähköstaattisten vuorovaikutusten ansiosta-.
Voi palvella sinua: sitruunahappoHapoilla tapahtuu jotain vastaavaa, jota ei voitu muodostaa, jos sellaista kovalenttista sidosta a-o-h ei olisi ollut.
Kysymyksen perusteella miten pääyhdisteet muodostuvat? Suora vastaus on seuraava:
- Metallimaiset emäkset muodostetaan liuostamalla veteen tai alkaliseen liuokseen (yleensä NaOH: n tai ammoniakin).
- Oksoasidit ovat ei -metallisten oksidien liukenemisen tuote veteen; Heistä, yhteistyökumppani2, Pylväs2, EI2, Sw3, P4JOMPIKUMPI10, jne.
- Ja sitten oksisalit syntyvät, kun oksoasidit alkalisoidaan tai neutraloidaan metallipohjalla; Siitä tulee metallikationien, jotka toimittavat h+.
Muut kolmiosaiset yhdisteet muodostuvat monimutkaisemman prosessin jälkeen, kuten tietyissä seoksissa tai mineraaleissa.
Esimerkit
Lopuksi, sarja kaavoja eri kolmiosaisille yhdisteille esitetään luettelona:
- Mg (OH)2
- Cr (OH)3
- Kmno4
- Naa3Bo3
- CD (OH)2
- Vanhempi veli3
- Feaso4
- Bacr2JOMPIKUMPI7
- H2Sw4
- H2Teo4
- HCN
- Thragh
Muita vähemmän yleisiä (ja jopa hypoteettisia) esimerkkejä ovat:
- Kofecu
- Alus
- UCAPB
- Tyyni2
Tilaukset N, M ja P jätettiin pois, jotta kaavoja ei monimutkaista; Vaikka todellisuudessa sen stökiometriset kertoimet (paitsi BEMGO: n parasta2), voi olla jopa desimaalit.
Viitteet
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- ROUVA. Hilfstein. (S.F.-A. Kolmiosainen comununds. Toipunut: Tenafly.K12.NJ.meille
- Wikipedia. (2019). Kolmen kolmen comund. Haettu: vuonna.Wikipedia.org
- Carmen Bello, Arantxa Isaasi, Ana Puerto, Germán Tomás ja Ruth Vicente. (S.F.-A. Kolmiosaiset yhdisteet. Toipunut: IESDMJAC.Koulutus.Aragon.On
- « Kvaternääriset yhdisteet ominaisuudet, koulutus, esimerkit
- Erityiset yhdisteiden ominaisuudet, koulutus, käyttö »

