Oksidatiiviset fosforylaatiovaiheet, toiminnot ja estäjät
- 4304
- 1050
- Shawn Stanton II
Se oksidatiivinen fosforylaatio Se on prosessi, jossa ATP -molekyylit syntetisoidaan ADP: stä ja P: stäYllyttää (Epäorgaaninen fosfaatti). Tämän mekanismin suorittavat bakteerit ja eukaryoottiset solut. Eukaryoottisissa soluissa fosforylaatio suoritetaan ei -fotosynteettisten solujen mitokondriaalimatriisissa.
ATP -tuotantoa ohjataan elektronien siirtämällä NADH- tai Fadh -koentsyymeistä2 O2. Tämä prosessi edustaa solun suurinta energiantuotantoa ja on johdettu hiilihydraattien ja rasvojen hajoamisesta.
 Lähde: Robot8a [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)]
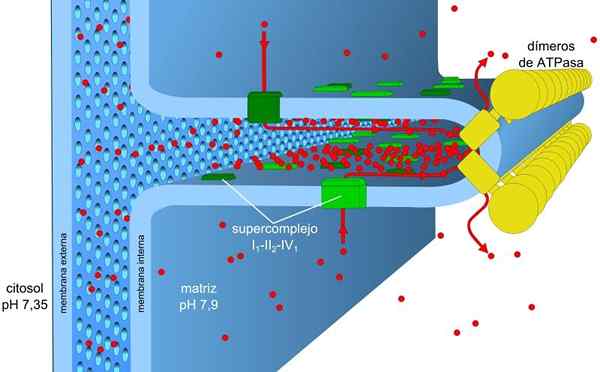
Lähde: Robot8a [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by-SA/4.0)] Kuormitukseen ja pH -gradienteihin, jotka tunnetaan myös nimellä protoninen moottorivoima, säilytetty energia mahdollistaa tämän prosessin suorittamisen. Generoitu protongradientti aiheuttaa kalvon ulkoisen osan positiivisesta kuormasta protonien pitoisuuden vuoksi (H+) ja mitokondriomatriisi on negatiivinen.
[TOC]
Missä tapahtuu oksidatiivinen fosforylaatio?
Elektronien kuljetus- ja oksidatiiviset fosforylaatioprosessit liittyvät kalvoon. Prokaryooteissa nämä mekanismit suoritetaan plasmamembraanin läpi. Eukaryoottisoluissa ne liittyvät mitokondriokalvoon.
Soluista löydettyjen mitokondrioiden lukumäärä vaihtelee solutyypin mukaan. Esimerkiksi nisäkkäissä punasoluista puuttuu nämä organelit, kun taas muilla solutyypeillä, kuten lihassoluilla, voi olla miljoonia niitä.
Mitokondriaalikalvo koostuu yksinkertaisesta ulkoisesta kalvosta, hiukan monimutkaisemmasta sisäisestä kalvosta ja keskellä niiden keskellä olevaa membraniaalista tilaa, jossa monet ATP: stä riippuvat entsyymit sijaitsevat.
Ulkoskalvo sisältää Porina -nimisen proteiinin, joka muodostaa kanavat pienten molekyylien yksinkertaiseen diffuusioon. Tämä kalvo on vastuussa mitokondrioiden rakenteen ja muodon ylläpidosta.
Sisäisen kalvon tiheys on suurempi ja siinä on runsaasti proteiinia. Se on myös vedenpitävä molekyyleille ja ionille, joten sen ylittämiseksi he tarvitsevat väliaikaisia proteiineja, jotka kuljettavat niitä.
Matriisin sisällä sisäkalvon taitteet ulottuvat, muodostaen harjanteet, jotka sallivat sen suuren alueen pienessä tilavuudessa.
Soluenergiakeskus
Mitokondrioita pidetään solujenergiakeskuksena. Siinä ovat entsyymit, jotka osallistuvat sytriinihapposyklin prosesseihin, rasvahappojen hapettumiseen ja elektronien kuljetuksen ja PHD.
Protonien (pH -gradientti) pitoisuusgradientti ja kuormitusgradientti tai sähköpotentiaali mitokondrioiden sisäisessä kalvossa ovat syynä korkeaan moottorivoiman voimaan. Ionien sisäisen kalvon pieni läpäisevyys (muut kuin h+) sallii mitokondrioiden olevan vakaa jännitegradientti.
Elektroninen kuljetus, protonit ja ATP saavat samanaikaisesti mitokondrioissa protonisen moottorin voiman ansiosta. PH -gradientti ylläpitää happamia olosuhteita membraanin ja mitokondrioiden matriisissa alkalisissa olosuhteissa.
Jokaiselle kahdelle elektronille siirrettynä O: lle2 Kalvo pumppaa noin 10 protonia, mikä luo sähkökemiallisen gradientin. Tässä prosessissa irrotettu energia tuotetaan vähitellen kuljettamalla elektroneja kuljetinketjun läpi.
Tasot
Energia, joka vapautui NADH: n ja FADH: n oksidien vähentämisreaktioiden aikana2 Se on huomattavasti korkea (noin 53 kcal/mol kullekin elektroniparille), joten ATP -molekyylien valmistuksessa käytettäväksi se on tuotettava vähitellen elektronien kulkiessa kuljettajien läpi.
Nämä on järjestetty neljään kompleksiin, jotka sijaitsevat sisäisessä mitokondriaalikalvossa. Näiden reaktioiden kytkentä ATP -synteesiin suoritetaan viidennessä kompleksissa.
Voi palvella sinua: B Lymfosyytit: ominaisuudet, rakenne, toiminnot, tyypitElektronin kuljetusketju
NADH siirtää pari elektronia, jotka tulevat elektronien kuljetusketjun kompleksi I. Elektronit siirretään flavinan mononukleotidiin ja sitten ubikinoniin (koentsyymi Q) rauta-sokerikuljettimen kautta. Tämä prosessi vapauttaa suuren määrän energiaa (16,6 kcal/mol).
Ubiquinona kuljettaa elektroneja kalvon läpi kompleksi III. Tässä kompleksissa elektronit käyvät sytokromien B ja C läpi1 Rauta-sokerin kuljettajan ansiosta.
Kompleksista III, elektronit kulkevat IV -kompleksiin (sytokromi c -oksidaasi), siirretään yksi sytokromi c: llä (perifeerinen membraaniproteiini). IV -kompleksissa elektronit kulkevat parin kupari -ionien läpi (Cu-lla2+), sitten sytokromi c-lla, sitten toiseen pariin kuparioneja (Cub -2+) ja tästä sytokromi3.
Lopuksi, elektronit siirretään O: lle2 joka on viimeinen vastaanottaja ja muodostaa vesimolekyylin (H2O) jokaiselle vastaanotetulle elektroniparille. Elektronien kulku kompleksista IV - O2 Se tuottaa myös paljon ilmaista energiaa (25,8 kcal/mol).
Succinato coq reduktaasi
II -kompleksi (Coq -reduktaasin sukkinaatti) vastaanottaa elektroniparin sitruunahapposyklistä johtuen sukkinaattimolekyylin hapettumisesta fumaraattiin. Nämä elektronit siirretään FAD: hen, kulkevat sitten rauta-azufre-ryhmän läpi Ubiquinonaan. Tästä koentsyymistä he menevät Complex III: lle ja seuraavat aiemmin kuvattua reittiä.
Elektroninsiirtoreaktiossa vapautuva energia FAD: hen ei riitä lisäämään protoneja kalvon läpi, niin että ketjun tässä vaiheessa ei ole prottotonista moottorivoimaa, ja näin ollen FADH tuottaa vähemmän H+ kuin nadh.
Energiakytkentä tai transduktio
ATP -tuotantoon tulisi käyttää aikaisemmin kuvatussa elektronien kuljetusprosessissa tuotettua energiaa, ATP -syntaasi- tai kompleksientsyymi V -katalysoimaa reaktiota. Tällaisen energian säilyttäminen tunnetaan energian kytkentänä, ja mekanismia on ollut vaikea karakterisoida.
Tätä energiansiirtoa on kuvattu useita hypoteeseja. Paras hyväksytty on kemosmoottinen kytkentähypoteesi, kuvattu alla.
Kemosmoottinen kytkentä
Tämä mekanismi ehdottaa, että ATP -synteesiin käytetty energia tulee protonisesta gradientista solukalvoissa. Tämä prosessi puuttuu mitokondrioihin, kloroplastiin ja bakteereihin ja liittyy elektronien kuljetukseen.
Elektronisen kuljetuksen I ja IV -kompleksit toimivat protonipumppuina. Nämä kärsivät konformaatiomuutoksista, joiden avulla ne voivat pumpata protonit väliaikaiseen tilaan. Kummankin elektroniparin IV -kompleksissa kaksi protonia pumpataan kalvon ulkopuolelle ja kaksi muuta pysyy matriisin muodostuessa H2JOMPIKUMPI.
Ubiquinona kompleksissa III hyväksyy kompleksien I ja II protonit ja vapauttaa ne kalvon ulkopuolella. I ja III -kompleksit sallivat kumpikin neljän protonin läpikulun jokaiselle kuljetetulle elektronille.
Mitokondriaalimatriisilla on alhainen protonien pitoisuus ja negatiivinen sähköpotentiaali, kun taas välinen välinen tila esittelee käänteiset olosuhteet. Protonien virtaus tämän kalvon läpi merkitsee sähkökemiallista gradienttia, joka tallentaa tarvittavan energian (± 5 kcal/mol protonin mukaan) ATP -synteesille.
ATP -synteesi
ATP -syntetaasientsyymi on viides kompleksi, joka osallistuu oksidatiiviseen fosforylaatioon. On vastuussa sähkökemiallisen gradientin energian hyödyntämisestä ATP: n muodostamiseksi.
Tämä transmembraal -proteiini koostuu kahdesta komponentista: F0 - ja f1. Komponentti f0 - Mahdollistaa protonien paluun mitokondriaaliseen matriisiin, joka toimii kanavana ja F1 katalysoi ATP: n synteesiä ADP: n ja P: n kauttaYllyttää, mainitun paluun energian käyttäminen.
Voi palvella sinua: Kalvokuljetinproteiinit: toiminnot ja tyypitATP -synteesiprosessi vaatii rakenteellisen muutoksen F: ssä1 ja komponenttien kokoonpano f0 - ja f1. Protonien siirtäminen F: n kautta0 - Se aiheuttaa konformaatiomuutoksia F: n kolmessa alaluokassa1, Antaa tämän toimia kiertomoottorina, ohjaamalla ATP: n muodostumista.
Alayksikkö, joka vastaa ADP: n liitosta p: n kanssaYllyttää siirtyy heikosta tilasta (l) aktiiviseen (t). Kun ATP muodostuu, toinen alayksikkö siirtyy avoimeen tilaan (O), joka sallii tämän molekyylin vapautumisen. Kun ATP on vapautettu, tämä alayksikkö siirtyy avoimesta tilasta passiiviseen tilaan (L).
ADP- ja P -molekyylitYllyttää He liittyvät alayksikköön, joka on mennyt valtiosta tai valtiosta L.
Tuotteet
Elektronikuljetinketju ja fosforylaatio tuottavat ATP -molekyylejä. NADH -hapettuminen tuottaa noin 52,12 kcal/mol (218 kJ/mol) vapaata energiaa.
NADH: n hapettumisen globaali reaktio on:
Nadh+1⁄2 tai2 +H+ H2O+nad+
Elektronien siirto NADH: sta ja Fadhista2 Se tapahtuu useiden kompleksien kautta, jolloin vapaan energian ΔG ° muutos voidaan jakaa pienempiin ”pakkauksiin”, jotka on kytketty ATP -synteesiin.
NADH -molekyylin hapettuminen tuottaa kolmen ATP -molekyylin synteesin. Kun taas fadh -molekyylin hapettuminen2 Se on kiinnitetty kahden ATP: n synteesiin.
Nämä koentsyymit tulevat glykolyysin ja sitruunahapposyklin prosesseista. Jokaiselle hajotetulle glukoosimolekyylille 36 tai 38 ATP -molekyyliä on päättymässä solujen sijainnista riippuen. Aivoissa ja luurankoissa 36 ATP tuotetaan, kun taas 38 ATP: tä tuotetaan lihaskudoksessa.
Funktiot
Kaikki organismit, yksisoluiset ja monisoluiset, tarvitsevat minimin energian soluissaan niiden sisällä olevien prosessien suorittamiseksi ja puolestaan ylläpitää elintärkeitä toimintoja koko kehossa.
Aineenvaihduntaprosessit vaativat energian suorittamista. Suurin osa käyttökelpoisesta energiasta saadaan hiilihydraattien ja rasvojen hajoamisella. Tämä energia johtuu oksidatiivisesta fosforylaatioprosessista.
Oksidatiivinen fosforylaation hallinta
ATP: n käyttöaste soluissa, säätelee saman synteesiä ja puolestaan johtuen oksidatiivisen fosforylaation kytkemisestä elektronien kuljetusketjun kanssa, se myös yleensä säätelee elektronista kuljetusnopeutta.
Oksidatiivisella fosforylaatiolla on tiukka kontrolli, joka varmistaa, että ATP: tä ei luoda nopeammin kuin se kulutetaan. Elektronien kuljetusprosessissa on tiettyjä vaiheita ja energiantuotannonopeutta säätelevässä kytketyssä fosforylaatiossa.
ATP -tuotannon koordinoitu hallinta
Tärkeimmät energiantuotannon reitit (solu ATP) ovat glykolyysi, sitruunahapon sykli ja oksidatiivinen fosforylaatio. Näiden kolmen prosessin koordinoitu hallinta säätelee ATP -synteesiä.
Fosforylaation hallinta ATP -massan vaikutuksella riippuu elektronien tarkasta vaikutuksesta kuljetusketjussa. Tämä puolestaan riippuu suhteesta [nadh]/[nad+] sitä säilyy glykolyysin ja sitruunahapposyklin vaikutuksella.
Tämä koordinoitu kontrolli suoritetaan säätelemällä glykolyysin kontrollipisteitä (sitraatti estänyt PFK) ja sytriinihapposykliä (dehydrogenaasi-pyruvaatti, cutease-sitraatti, kutchitraattidehydrogenaasi ja a-zetoglutaraatti-dehydrogenaasi).
Vastaanottajan hallinta
IV -kompleksi (sytokromi c -oksidaasi) on entsyymi, jota säätelee yksi sen substraateista, ts. Sen aktiivisuutta säätelee vähentynyt sytokromi c (C2+), mikä puolestaan on tasapainossa [nadh]/[nad+] ja [ATP]/[ADP] + [p: n massavaikutussuhdeYllyttää-.
Se voi palvella sinua: sävy: ominaisuudet ja toiminnotMitä korkeampi [nadh]/[nad+] ja alenna [ATP]/[ADP]+[PYllyttää], enemmän konsentraatiota on sytokromi [c2+] ja suurempi on kompleksin IV aktiivisuus. Tätä tulkitaan esimerkiksi, jos vertaamme organismeja erilaisiin lepotoimintoihin ja korkeaan aktiivisuuteen.
Yksilöllä, jolla on korkea fyysinen aktiivisuus, ATP: n kulutus ja siksi sen hydrolyysi ADP + P: ksiYllyttää Se on erittäin korkea, mikä tuottaa eron massan toimintasuhteessa, joka aiheuttaa [C: n lisääntymisen2+ja siksi ATP -synteesin lisääntyminen. Lepo -yksilössä käänteinen tilanne esiintyy.
Lopulta oksidatiivisen fosforylaation nopeus kasvaa ADP: n pitoisuuden kanssa mitokondrioissa. Tämä pitoisuus riippuu ADP-ATP-siirtäjistä, jotka ovat vastuussa adeniininukleotidien ja pYllyttää Sytosolista mitokondriaaliseen matriisiin.
Dekoplanttien edustajat
Oksidatiiviseen fosforylaatioon vaikuttavat tietyt kemialliset aineet, jotka sallivat elektronisen kuljetuksen jatkaa ilman ADP: n fosforylaatiota, energian tuotannon ja säilyttämisen irrottamisen.
Nämä aineet stimuloivat mitokondrioiden hapenkulutuskannun ilman ADP: tä, aiheuttaen myös ATP -hydrolyysin lisääntymisen. Ne toimivat poistamalla välittäjä tai rikkomalla energiatilan elektronikuljetinketjusta.
2,4-dinitrofenoli, heikko happo, joka kulkee mitokondriaalisten kalvojen läpi, on vastuussa protonien gradientin hajottamisesta, koska ne liittyvät heihin happamaan puoleen ja vapauttavat ne emäksisellä puolella.
Tätä yhdistettä käytettiin "laihtumispillerinä", koska havaittiin, että se tuotti hengityksen lisääntymisen, siksi aineenvaihdunnan nopeuden ja siihen liittyvän painonpudotuksen lisääntyminen. Osoitettiin kuitenkin, että sen kielteinen vaikutus voi jopa aiheuttaa kuolemaa.
Protonisen gradientin hajoaminen tuottaa lämpöä. Ruskeat rasvakudoksen solut käyttävät irrottamista, hormonaalisesti kontrolloituja, lämmön tuottamiseen. Hibernaattiset nisäkkäät ja vastasyntyneet, joilla ei ole hiuksia.
Estäjät
Estävät yhdisteet tai aineet estävät sekä tai2 (elektroninen kuljetus), kuten siihen liittyvä oksidatiivinen fosforylaatio. Nämä aineet välttävät ATP: n muodostumisen sähköisen kuljetuksen tuotetun energian avulla. Siksi kuljetusketju pysähtyy, koska sellaista energiankulutusta ei ole järjestetty.
Oligomisiinin antibiootti toimii fosforylaation estäjänä monissa bakteereissa, estäen ADP -stimulaation ATP -synteesistä.
On myös ionofotorisia aineita, jotka muodostavat rasvan liukoisia komplekseja kationien kanssa, kuten k+ ja na NA+, ja kulkea mitokondriaalikalvon läpi näiden kationien kanssa. Mitokondriat käyttävät sitten elektronisessa kuljetuksessa tuotettua energiaa pumppaamaan kationeja syntetisoinnin sijasta ATP: n syntetisoinnin sijasta.
Viitteet
- Alberts, b., Bray, D., Hopkin, k., Johnson, a., Lewis, J., Raff, m., Roberts, k. & Walter, P. (2004). Välttämätön solubiologia. New York: Garland Science.
- Cooper, G. M., Hausman, r. JA. & Wright, N. (2010). Solu. (PP. 397-402). Marbán.
- Devlin, t. M. (1992). Biokemian oppikirja: kliinisillä korrelaatioilla. John Wiley & Sons, Inc.
- Garrett, r. H., & Grisham, c. M. (2008). Biokemia. Thomson Brooks/Cole.
- Loodish, h., Darnell, J. JA., Berk, a., Kaiser, c. -Lla., Krieger, m., Scott, M. P., & Matsudaira, P. (2008). Mollecular -solusbiologia. Macmillan.
- Nelson, D. Lens., & Cox, M. M. (2006). Lehninger -biokemian periaatteet 4. painos. Ed Omega. Barcelona.
- Voet, D., & Voet, J. G. (2006). Biokemia. Ed. Pan -American Medical.
- « Euglenophyta -ominaisuudet, lisääntyminen, ravitsemus, luokittelu
- Glukosidien koulutus, toiminto ja tyypit/ryhmät »

