Cannizzaro -reaktioominaisuudet, mekanismit, esimerkit

- 1353
- 337
- Shawn Stanton II
Se Cannizzaro -reaktio Se on itse-xidation-pelkistys, jota kärsivät ei-enlazaalit aldehydit voimakkaasti perusympäristössä. Voidaan sanoa, että se on vaihtoehtoinen reaktio aldooliseen kondensaatioon ja on yleensä ei -toivottu orgaanisen synteesin suhteen, johon formaldehydi osallistuu.
Tämän reaktion löysi italialainen kemisti Stanislao Cannizzaro, joka vuonna 1853 sekoitettu bentsaldehydi PONASSA: n kanssa, k2Yhteistyö3, bentsyylialkoholin ja kaliumbentsoaatin saaminen. Sitten sama reaktio toistettiin, mutta käyttämällä vielä enemmän emäksiä aineita, kuten natrium- ja kaliumhydroksideja.
 Yhtälö ja mekanismi bentsaldehydin Cannizzaro -reaktiolle. Lähde: Krishnavedala / julkinen alue
Yhtälö ja mekanismi bentsaldehydin Cannizzaro -reaktiolle. Lähde: Krishnavedala / julkinen alue Ylivoimainen kuva näyttää bentsaldehydin Cannizzaro -reaktion, joka on yksinkertaisin kaikista aromaattisista aldehydeistä. Kaksi bentsaldehydi -molekyyliä suhteettomana voimakkaasti emäksisessä ympäristössä aiheuttamaan bentsoaatin ja bentsyyli -alkoholi -ionien seoksen. Toisin sanoen reaktio johtaa karboksyylihapposuolan ja primaarisen alkoholin seokseen.
Siksi periaatteessa reaktion saanto on 50%, koska puolet koostuu yhdestä suolasta ja toinen puoli vastaa alkoholia. Tämä 100% asteikon sato on kuitenkin ristiretken Cannizzaro -reaktio; Tämä on se, joka tapahtuu kahden erilaisen aldehydin välillä.
[TOC]
Ominaisuudet ja olosuhteet
Alfas -hydrogenssien puuttuminen
Niin, että Cannizzaro -reaktio on mahdollista, kyseisen aldehydin täytyy puuttua alfa -vety. Tämä tarkoittaa, että karbonyyliryhmän vieressä olevalla hiiliatomilla ei pitäisi olla yhteyttä vetyatomiin: r: R3C-C = O.
Jos havaitaan bentsaldehydin tapauksessa, jos C-kristi-sidos havaitaan, havaitaan tämän happahapon vedyn kokonaismäärä.
Voi palvella sinua: elastiset materiaalitPerusteetti
Cannizzaro -reaktio tapahtuu voimakkaasti emäksisissä väliaineissa, jotka yleensä tarjoavat natrium- ja kaliumhydroksidit vesipitoisissa tai alkoholiliuoksissa.
Lämpötila
Formaldehydin Cannizzaro -reaktio tapahtuu huoneenlämpötilassa. Kaikille muille aldehydeille on kuitenkin tarpeen lämmittää reaktioseos. Siten lämpötila voi vaihdella välillä 50-70 ° C liuoksesta ja aldehydistä riippuen.
Autoksidaation vähentäminen
Cannizzaro -reaktion aldehydi kärsii itsekyllytyksestä. Tämä tarkoittaa, että aldehydimolekyyli hapettuu itsensä vähentäen toista naapurin molekyyliä. Tuloksena on, että aldehydi -suhteettomana aiheuttaen suolaa karboksyylistä (hapettua) happoa ja primaarista (vähentynyttä) alkoholia (pelkistetty).
Mekanismit
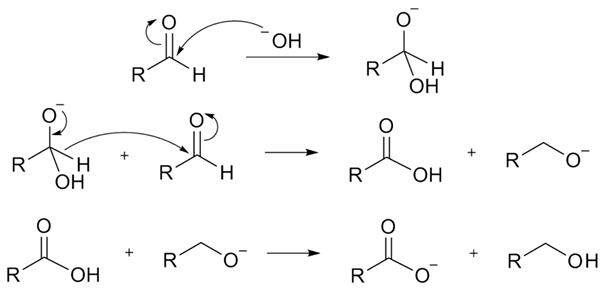 Cannizzaro -reaktion yleinen mekanismi. Lähde: Roshan220195 englanniksi Wikipedia / julkinen verkkotunnus
Cannizzaro -reaktion yleinen mekanismi. Lähde: Roshan220195 englanniksi Wikipedia / julkinen verkkotunnus Ensimmäisessä kuvassa bentsaldehydin Cannizzaro -reaktiota varten sen mekanismi osoitti. Tämä osa selittää tämän mekanismin kaksi olennaista vaihetta, joka perustuu kaikkien aldehydien reaktioon yleensä (ylivoimainen kuva).
Vaihe 1
OH -ionit- Perusympäristöstä he suorittavat nukleofiilisen hyökkäyksen aldehydimolekyylistä. Näin muodostetaan tetraedrinen välittäjä (ensimmäisen rivin oikea). Tämä ensimmäinen vaihe on palautuva, joten välittäjä voi päästä eroon alkuperäisistä reagensseista.
Vaihe 2
Mekanismin toinen vaihe sisältää ns. Autoksidaation vähentämisen. Vaiheen 1 välittäjässä linkki c = O muodostuu hydridi -ionin siirtymisen kustannuksella, H-, Toiselle aldehydimolekyylille. Siten ensimmäinen molekyyli hapettuu, kun taas toinen voittaa tämän h-, eli se on vähentynyt.
Voi palvella sinua: Useiden mittasuhteiden lakiTäällä meillä on jo karboksyylihappo ja alkoholi (oikea toinen rivi). Heidän joukossaan ioninvaihto hshes+, Karboksyylihappo ja alkoholi.
Siten meillä on karboksylaatti -anioni lopussa, joka on vuorovaikutuksessa emäskationin kanssa karboksyylihapposuolan muodostamiseksi. Ja meillä on myös ensisijainen alkoholi.
Ristiretki
Toistaiseksi on puhuttu Cannizzaro -reaktiosta saman aldehydin kahden molekyylin välillä. Tämä reaktio voi myös kulkea kahden erilaisen aldehydimolekyylin välillä; varsinkin jos yksi heistä koostuu formaldehydistä. Puhumme sitten Cruzada Cannizzaron reaktiosta, jonka yleinen kemiallinen yhtälö on alla:
Archo + hcho → kaari2Voi + hcoo-Naa+
Cruzada Cannizzaro -reaktio on aromaattisen aldehydin, kaarin välillä.
Alla on esimerkki Cruzada Cruzada del Anisaldehydin reaktiosta:
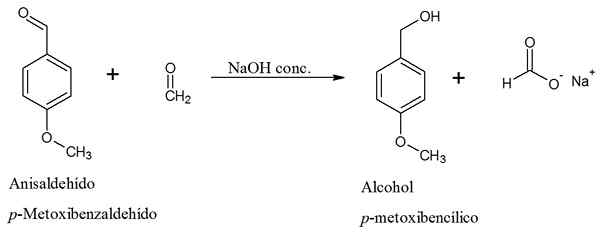 Yhtälö Cruzada Cruzada del Anisaldehydin reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta.
Yhtälö Cruzada Cruzada del Anisaldehydin reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta. Huomaa, että muodostuva ioni muodostuu aina, koska se johtuu muurahaishapoista, HCOOH: sta, heikoimmasta haposta ja siksi se, joka tapahtuu pääasiassa. Tämä reaktio edustaa synteettistä reittiä aromaattisten alkoholien syntetisoimiseksi aromaattisista aldehydeistä ilman tarvetta käyttää pelkistäviä aineita.
Esimerkit
Seuraava ja lopulta useita esimerkkejä Cannizzaro -reaktiosta esitetään.
Esimerkki 1
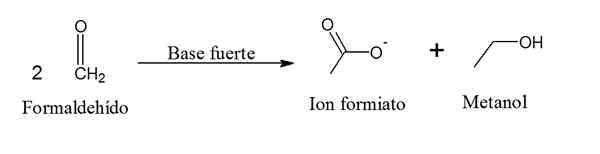 Kemiallinen yhtälö formaldehydin Cannizzaro -reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta.
Kemiallinen yhtälö formaldehydin Cannizzaro -reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta. Kaksi formaldehydi -molekyyliä ovat suhteettomia itse muodostuvan ja metanoli -ionin tuottamiseksi. Tämä reaktio tapahtuu huoneenlämpötilassa, joten formaldehydiä ei tule sekoittaa voimakkaasti emäksiseen liuokseen, jos se on tarkoitettu käytettäväksi synteesissä.
Voi palvella sinua: 10 esimerkkiä ei -polaarisista kovalenttisia linkkejäEsimerkki 2
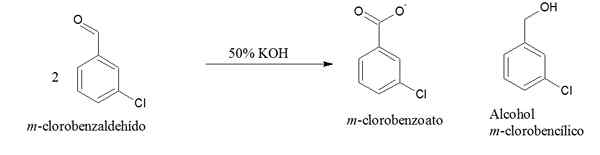 Yhtälö m-clorobentsaldehydin Cannizzaro-reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta.
Yhtälö m-clorobentsaldehydin Cannizzaro-reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta. Tässä reaktiossa kaksi molekyyliä m-Kloorobentsaldehydi ovat suhteettomia sekoituksessa m-Kloorobentsoaatti, karboksyylihapposuola ja alkoholi m-Kloorobentseeni, primaarinen alkoholi.
On odotettavissa, että tämä reaktio vaatii enemmän lämpötilaa ja vie vähän kauemmin, koska ne ovat suurempia molekyylejä kuin formaldehydin reaktio.
Esimerkki 3
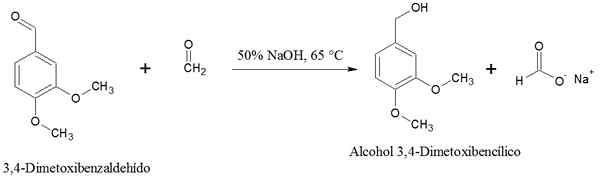 Yhtälö 3,4-dimetoksibentsaldehydin Cannizzaro-reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta.
Yhtälö 3,4-dimetoksibentsaldehydin Cannizzaro-reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta. 3,4-dimetoksibentsaldehydi. Huomaa, että tämä reaktio tarvitsee lämpötilan 65 ° C. Muista.
Esimerkki 4
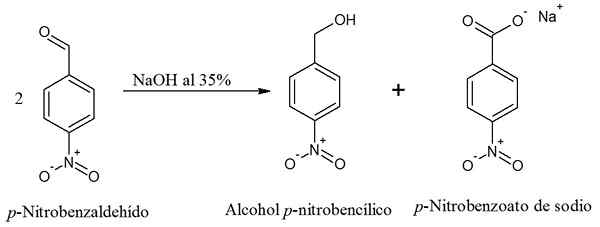 Yhtälö p-nitrobentsaldehydin Cannizzaro-reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta.
Yhtälö p-nitrobentsaldehydin Cannizzaro-reaktiolle. Lähde: Gabriel Bolívar Chemsketchin kautta. Kaksi molekyyliä p-Nitrobentsaldehydi ovat suhteettomia alkoholiseoksen perustamiseksi p-nitrobencyl ja suola p-Natriumnitrobentsoaatti. Jälleen tämä reaktio edustaa synteettistä reittiä mainitun aromaattisen primaarisen alkoholin saamiseksi.
Ensimmäinen esimerkki, bentsaldehydin, on tunnetuin orgaanisen kemian opetuslaboratorioissa, koska sitä käytetään Cannizzaron reaktion käsitteen esittelyyn opiskelijoille.
Voidaan kuitenkin nähdä, että mahdolliset esimerkit voivat olla lukemattomia, jos aromaattista aldehydiä harkitaan. Tai mikä tahansa muu aldehydi ilman hydrogens -alfas.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5ta Painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. (10thPainos.-A. Wiley Plus.
- Wikipedia. (2020). Canizzaro -reaktio. Haettu: vuonna.Wikipedia.org
- Laura Foist. (2020). Canizzaro -reaktio: Mekanismi ja esimerkki. Opiskelu. Toipunut: Opiskelu.com
- Elsevier B.V. (2020). Canizzaro -reaktio. Tiede. Haettu: ScienEdirect.com
- Helmestine, Anne Marie, PH.D -d. (11. helmikuuta 2020). Cannizzaro -reaktio orgaanisessa kemiassa. Toipunut: Admingco.com
- « Epoksi -nimikkeistö, hankkiminen, sovellukset, esimerkit
- Puolipyörä kuinka kehä, pinta -ala, keskikohdan, harjoitukset lasketaan »

